Ponto de congelamento da água
O processo de congelamento ocorre quando resfriado a zero graus na escala Celsius. Isso não se aplica a toda a água. As moléculas se ligam às impurezas, que são partículas de poeira, sal, etc. Portanto, a água pura ou destilada, sem a presença dessas mesmas impurezas, sob a influência de baixas temperaturas na coluna Celsius, pode permanecer em estado líquido por mais tempo que a água comum.
Também é interessante que, enquanto outras substâncias diminuem de volume ao congelar, a água, pelo contrário, aumenta. Isso ocorre porque a distância entre as moléculas se expande durante a transição para o estado sólido. Apesar de o volume aumentar, a massa não aumenta ao congelar e pesa tanto quanto a água morna.
Muitas pessoas se perguntam por que a água não congela sob uma espessa camada de gelo. Qualquer físico responderá que sob uma camada de gelo a água não congela, pois a superfície do gelo serve como isolante térmico.

Por que a água quente congela mais rápido que a água fria?
Sabe-se que a água quente ou morna congela mais rápido que a água fria. Inacreditável, mas verdadeiro. Esta descoberta foi feita por Erasto Mpemba. Ele conduziu experimentos usando a massa congelada e descobriu que, se a massa estiver quente, ela congelará mais rapidamente. A razão para isso, como os estudos mostraram, é a alta transferência de calor da água quente e morna.

O ponto de congelamento da água e a altitude estão relacionados?
Como você sabe, a pressão muda em altitude, então a temperatura de transição para o estado sólido de todas as soluções aquosas em altitude difere da temperatura em uma superfície normal.
Exemplos de mudanças de temperatura em altitude:
- altitude 500 m - o ponto de congelamento da água não é zero ° C, como em condições normais, mas na presença de já um ° C;
- altura 1500 m - a cristalização ocorre na presença de cerca de três ° C, etc.

Como a pressão afeta o processo de cristalização da água
Se você entender a relação entre pressão e cristalização da água, tudo é bastante simples.
Interessante! Quanto maior a pressão, menor a taxa de transformação da água em cristais de gelo e maior o ponto de ebulição!
Esse é todo o segredo e, se você pensar logicamente, com uma diminuição da pressão, todos os indicadores vão na direção oposta. Portanto, é difícil cozinhar algo nas montanhas, pois a temperatura em que a água ferve não chega a cem graus Celsius. Por outro lado, o gelo derrete mesmo em baixas temperaturas.
Temperatura de cristalização de soluções aquosas
A água é um bom solvente e, portanto, combina facilmente com outras substâncias. As soluções resultantes, é claro, congelarão sob diferentes condições. Considere algumas opções de critérios de temperatura para congelar diferentes soluções baseadas em água.
Água e álcool. Com uma grande quantidade de álcool na água, o processo de congelamento começará na presença de temperaturas muito baixas. Por exemplo, em uma proporção de 60% de água para 40% de álcool, a cristalização começará na presença de menos 22,5 ° C.
Água e sal. A temperatura na qual ocorre o congelamento está diretamente relacionada ao grau de salinidade da água. O princípio é que quanto mais sal na água, menor a temperatura de cristalização. Como a água do mar congela está diretamente relacionada ao teor de sal.
Água e refrigerante. A temperatura de cristalização da solução é de 44 por cento, mais 7°C.
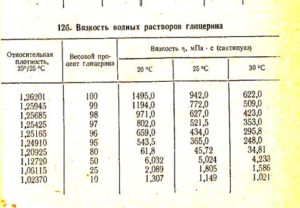
Água e glicerina, na proporção de 80% a 20%, onde 80 é glicerina e 20 é água, é necessária a presença de -20°C para congelar a solução.
Todos os valores de temperatura variam dependendo do grau de concentração de soluções estranhas ou outras substâncias na água.
Medindo a viscosidade de líquidos com um viscosímetro Ostwald
Para determinar o coeficiente de viscosidade ηhis do líquido investigado usando um viscosímetro capilar de Ostwald (Fig. 6), é necessário saber:
- η0 é a viscosidade da água,
- t0 é o tempo de fluxo de água entre as marcas a e b,
- tx é o tempo de escoamento do líquido investigado entre as marcas a e b,
- ρ0 é a densidade da água,
- ρx é a densidade do líquido investigado.
Arroz. 6. Viscosímetro capilar de Ostwald (a, b, d - marcas limitando o nível do líquido, c - capilar).
A viscosidade do líquido investigado é determinada pela fórmula (9).
Ordem de serviço
Tarefa 1. Determinar a viscosidade de soluções com diferentes concentrações.
-
Despeje água na perna do viscosímetro que não possui capilar (Fig. 6) até a marca d.
-
Com uma pêra, chupe o líquido pelo capilar para marcar a. Depois de retirar a pêra, feche o orifício do joelho esquerdo do viscosímetro (com a mão, uma rolha, um cotonete, etc.) (ver Fig. 6). Prepare e ligue o cronômetro, abrindo o orifício do joelho esquerdo, e desligue-o quando a marca b fluir, determinando assim t0 - o tempo de vazão da água entre as marcas a e b.
-
Repita as medições 4-5 vezes, encontre o tempo médio.
-
Execute as etapas 1-3 para todos os líquidos de teste.
-
Calcule os coeficientes de viscosidade dos líquidos estudados usando a fórmula (9).
-
Insira os dados na tabela 1.
tabela 1
| № | Concentração, % | t1 | t2 | t3 | t4 | t5 | | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 | ||||||||
| 5 | ||||||||
| 6 |
Tarefa 2. Determine a concentração de uma solução desconhecida.
-
Relação de viscosidade do gráfico vs concentração da solução
-
Conhecendo a viscosidade da solução desconhecida, determine sua concentração a partir do gráfico.
mesa 2
Densidade da água em diferentes temperaturas
| ρ, kg/m3 | t, 0C | ρ, kg/m3 | t, 0C |
| 999,13 | 15 | 998,02 | 21 |
| 998,97 | 16 | 997,80 | 22 |
| 998,80 | 17 | 997,57 | 23 |
| 998,43 | 19 | 997,32 | 24 |
| 998,23 | 20 | 997,07 | 25 |
Tabela 3
Viscosidade da água em diferentes temperaturas
| η, Pa.s | t, 0C | η, Pa.s | t, 0C |
| 0,00114 | 15 | 0,00098 | 21 |
| 0,00111 | 16 | 0,00096 | 22 |
| 0,00108 | 17 | 0,00093 | 23 |
| 0,00103 | 19 | 0,00091 | 24 |
| 0,00100 | 20 | 0,00089 | 25 |
Tabela 4
Densidade de soluções de glicerina de várias concentrações
| COM, % | ρ, kg/m3 | COM, % | ρ, kg/m3 |
| 5 | 1012,5 | 45 | 1112,5 |
| 10 | 1025,0 | 50 | 1125,0 |
| 15 | 1037,5 | 55 | 1137,5 |
| 20 | 1042,5 | 60 | 1150,0 |
| 25 | 1052,5 | 65 | 1162,5 |
| 30 | 1075,0 | 70 | 1175,0 |
| 35 | 1087,5 | 75 | 1187,5 |
| 40 | 1100,0 | 80 | 1200,0 |
Trabalho independente sobre o tema:
– solução de problemas situacionais;
- ouvir resumos
Controle final do conhecimento:
– resolução de problemas de tickets;
– respostas aos tickets de controle final;
- resumindo.
Lição de casa para entender o tópico da lição
Perguntas de controle sobre o tema da aula:
1. Como é chamada a viscosidade de um líquido?
2. Que tipo de fluxo de fluido é chamado de laminar?Turbulento?
3. O que caracteriza a fórmula de Reynolds?
4. Escreva a fórmula de Newton e explique o significado físico das quantidades nela incluídas?
5. Qual é o coeficiente de viscosidade dinâmica? Em que unidades é medido?
6. Quais fluidos são chamados newtonianos? O que determina seu coeficiente de viscosidade?
7. Quais líquidos são chamados não newtonianos?O que determina seu coeficiente de viscosidade?
8. Escreva a fórmula de Poiseuille, explique o significado físico das quantidades nela incluídas.
9. Quais métodos são usados para determinar a viscosidade de um líquido?
10. Fale sobre as propriedades reológicas do sangue e outros fluidos biológicos, sobre o uso de análises reológicas na medicina.
11. O que o gradiente de velocidade mostra? Mostrar graficamente.
12. Que fenômeno é chamado de atrito interno?
Tarefas de teste sobre o tema:
A APLICAÇÃO DE GLICERINA NO AQUECIMENTO É JUSTIFICADA?
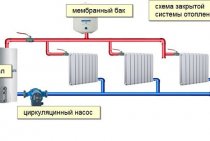
Requisitos bastante altos são impostos ao refrigerante para sistemas de aquecimento. Deve ser à prova de fogo e explosão, apresentar bom desempenho térmico e também não conter aditivos de uso proibido. O etilenoglicol ou propilenoglicol é usado como base para a produção de fluido de transferência de calor de alta qualidade, o que também garante respeito ao meio ambiente.
Recentemente, refrigerantes anticongelantes à base de glicerina apareceram no mercado. Este produto é promovido principalmente por empresas pequenas e pouco conhecidas no mercado de anticongelantes. Surge a pergunta: glicerina e refrigerante - sua união é adequada?
E, de fato, os primeiros anticongelantes que apareceram em nosso país nos anos vinte do século passado foram feitos à base de glicerina. Suas fraquezas eram fluidez insuficiente e viscosidade extremamente alta, que as bombas não podiam lidar. Eles tentaram resolver o problema com a ajuda do álcool, incluindo o álcool metílico. No entanto, juntamente com a melhoria da fluidez, muitos problemas apareceram. O fato é que o metanol é um forte veneno psicotrópico.Como resultado, o comportamento dos motoristas que cheiravam involuntariamente esse anticongelante às vezes desafiava qualquer lógica e representava um perigo para a saúde e a vida de outras pessoas. Além disso, o álcool metílico tem baixo ponto de ebulição e, ao evaporar, a viscosidade do produto aumenta imediatamente. O problema foi resolvido apenas quando o etilenoglicol se tornou a base do refrigerante. E no final dos anos trinta, início dos anos quarenta, os anticongelantes de etilenoglicol substituíram quase completamente os de glicerina-metanol.
Além disso, a glicerina é termicamente instável, se decompõe durante o aquecimento prolongado, com a formação de uma substância volátil venenosa - acroleína, que possui um odor desagradável acentuado que causa lacrimejamento. Os produtos de decomposição são tóxicos e a precipitação aumenta a atividade corrosiva do refrigerante. Como resultado, os requisitos para vedações e peças feitas de borrachas não polares e plásticos estão aumentando. Além da alta viscosidade, a glicerina também espuma muito, o que leva a arejar o sistema e a uma má dissipação de calor.
Os fabricantes de refrigerantes de glicerina estão tentando compensar todas as desvantagens acima adicionando vários aditivos, incluindo álcoois alifáticos - metanol, etanol, propanol. Esses álcoois podem reduzir significativamente a viscosidade ou densidade do líquido de arrefecimento anticongelante. Mas eles já fervem em temperaturas acima de 65 graus, o que leva a uma deterioração no desempenho térmico do refrigerante. Esses álcoois são capazes de dissolver borracha e polímeros e também são propensos à cavitação e forte evaporação. Além disso, o metanol é um veneno forte e seu uso é proibido na produção de líquidos anticongelantes.
Garantir a qualidade dos refrigerantes de glicerina, especialmente com metanol, requer a adição de pacotes de aditivos caros à mistura. E embora o custo da glicerina seja agora menor do que o custo dos glicóis, o pacote de aditivos para fazer fluidos de transferência de calor de glicerina de qualidade é mais caro do que o pacote de aditivos para anticongelante à base de etilenoglicol e propilenoglicol. E se o custo do anticongelante de glicerina no mercado for menor que o do glicol, significa que o fabricante simplesmente economizou na qualidade e não adicionou os aditivos caros necessários ao produto!
Portanto, a escolha cabe ao comprador: um refrigerante confiável e comprovado à base de glicóis ou um "porco em um puxão" de glicerina.
A escolha de nossa empresa, como a maioria dos principais fabricantes de anticongelantes, é fundamentalmente inequívoca - a glicerina não pode ser usada em sua forma pura, mas misturada com metanol é perigosa e criminosa!
O principal argumento que confirma nossa posição sobre esta questão é que em qualquer instalação importante e grande, o uso de glicerina em sistemas de aquecimento e refrigeração NÃO É PERMITIDO pelas normas existentes!
MEG
O etilenoglicol é um produto da hidratação do óxido de etileno na presença de ácido sulfúrico ou fosfórico. Refere-se a álcoois poli-hídricos. Não congela em baixas temperaturas e diminui o ponto de congelamento da água. Capaz de absorver água do ar.
É vendido em barris de metal e plástico, de até 227 litros. Bem como cubos de plástico 1000l.
É necessário armazenar a substância em um recipiente fechado de alumínio ou aço com proteção anticorrosiva em um armazém fechado sem aquecimento. O prazo de validade para o grau mais alto é de 12 meses, para o primeiro grau - 3 anos a partir da data de produção.
Nome do indicador Norma
Aspecto, odor Líquido límpido e incolor com textura oleosa. Sem cheiro.
Solúvel em água, álcoois, tolueno, benzeno
Densidade 1,112 g/cm?.
Ponto de fusão 12,9 graus Celsius
Ponto de ebulição 197,3 graus Celsius
Aplicativo
Devido à sua capacidade de baixar o ponto de congelamento, o monoetilenoglicol é utilizado na produção de anticongelante e fluido de freio para carros, bem como na fabricação de celofane e poliuretano. Em menor grau, é usado na produção de tintas e tintas de impressão.
Classe de Perigo
Refere-se a substâncias combustíveis. A auto-ignição ocorre a uma temperatura de 380 graus, um flash de vapor quando aquecido a 120 graus. Tóxico. A ingestão não é permitida. Os vapores são menos prejudiciais.
Glicerol
Fórmula química: HOCH2CH(OH)CH2OH
Nome internacional: Glicerina
Nº CAS: 56-81-5
Qualificação: Criança levada. "h", GOST 6259-75
Aparência: líquido claro e inodoro
Embalagem: Latas de 25 kg, tambores de 250 kg, 1500 cubos
Condições de armazenamento: em uma sala seca ventilada a uma temperatura baixa
Sinônimos: 1,2,3-trioxipropano
Oferecemos Glicerina em latas, barris, cubos a preços competitivos.
| Especificação | |
| Peso molecular | 92.10 |
| Substância básica, não inferior a | 99,5% (real 99,8%) |
| Conteúdo de cinzas, não mais | 0,01% (na verdade, menos de 0,1%) |
| Teor de água, não mais | 0,5% (na verdade 0,1%) |
| Teor de cloretos, não mais | 0,001 % |
| Teor de sulfato, não mais | 0,002 % |
| Metais pesados, não mais | 0,0005% (na verdade, menos de 0,00005%) |
| Compostos de cloro (como CL), não mais | 0,003 % |
| Arsênico, não mais | 0,00015% (real inferior a 0,00001%) |
| Cor (APHA), não mais | 20 (na verdade, menos de 10) |
A glicerina é um líquido incolor, higroscópico, viscoso, inodoro e de sabor adocicado. Miscível em qualquer proporção com água, etanol, metanol, acetona, insolúvel em clorofórmio e éter. Quando o glicerol é misturado com água, o calor é liberado e ocorre a contração (redução de volume). Quando o glicerol interage com ácidos hidro-hálicos ou haletos de fósforo, formam-se mono- ou di-halohidrinas; com ácidos inorgânicos e carboxílicos - ésteres completos e incompletos, com desidratação - acroleína. O glicerol pode ser oxidado e, dependendo das condições e da natureza do agente oxidante, pode-se obter gliceraldeído, ácido glicérico, ácido tartrônico, dihidroxiacetona, ácido mesoxálico. A glicerina é encontrada em gorduras e óleos naturais como triglicerídeos mistos de ácidos carboxílicos.
Aplicativo A glicerina é amplamente utilizada • na indústria farmacêutica, por exemplo, para a produção de nitroglicerina, pomadas medicinais; • na indústria alimentar, por exemplo na produção de licores, confeitaria; • na indústria cosmética, na fabricação de perfumes e cosméticos, • na produção de resinas glípticas; • como amaciante de tecidos, couro, papel; • como componente de emulsificantes, anticongelantes, lubrificantes, graxas para sapatos, sabões e adesivos, • como matéria-prima na produção de poliálcoois, que são utilizados em diversas espumas. • como plastificante para celofane, etc.
A que temperatura a água congela em tubos de aquecimento em um prédio residencial
Se a temperatura da casa permanecer -10 por vários dias e houver água nos canos, ela poderá congelar, o que levará à ruptura dos canos. Muitos provavelmente já viram baterias de aquecimento modernas com função de drenagem de água. Quase todas as baterias modernas estão equipadas com a capacidade de drenar água. Isso é feito para que, em caso de emergência, quando a temperatura da casa for -10, a água não congele e não rasgue os canos. Se a situação chegou a isso, simpatizamos muito com você, provavelmente você terá que trocar as baterias, pois durante o congelamento da água, provavelmente ocorreram microfissuras que tornam a operação dessas baterias perigosa.
Por que a água pode congelar nos canos? Se durante a estação de aquecimento, apenas quando as baterias estão enchendo com água, ocorre uma avaria e a água é resfriada, e a temperatura cai rapidamente lá fora, isso pode levar ao congelamento dos tubos.
Já respondemos à pergunta em que temperatura a água congela, como experimento, pegue um copo pequeno, encha-o até a metade com água e coloque-o no freezer por várias horas, duas horas são suficientes para que a água se transforme parcialmente em gelo.
A água é uma das substâncias mais essenciais do nosso planeta. Tem muitas propriedades que o tornam, até certo ponto, único. Uma das propriedades mais famosas que até uma criança pequena conhece é o congelamento da água.Sabe-se que 0 graus Celsius é a temperatura de cristalização da água. Mas nem tudo é tão simples. Consideraremos mais algumas das sutilezas desse processo.

Densidade da solução de glicerina a 25
A média aritmética das densidades de álcool e glicerol.
209.4. 1.047. 25.265.0. 1.060. ... Veja qual é a densidade de soluções aquosas de glicerina em outros dicionários E236 Arquivo Formic acid.svg Fórmula estrutural do ácido fórmico Ácido fórmico O ácido metanóico é o primeiro ...
Qual é a densidade da glicerina a 17 graus Celsius?
8
Densidade a 25 C, g cm. ... Uma solução de glicerina na concentração de 25% ou mais não expõe a contaminação microbiana; em soluções mais diluídas, os microrganismos se multiplicam bem nela.
3,14
Qual líquido tem maior densidade, glicerina ou álcool? explique
Ssss
TK-abril no site em toda a Rússia. Concentração, densidade e índice de refração de soluções de glicerol 15 С. … 1,0594. 1,3633. 25.1.0620.
Calcule a massa molar de ambas as substâncias. Para álcool, é menor (92 g/mol versus 46 g/mol para álcool), e a densidade é correspondentemente menor. Quando se trata de álcool etílico.
Qual é o ponto de tais perguntas? A informação é encontrada nos motores de busca
A média aritmética das densidades dos componentes da mistura.
Determine que massa de glicerol com densidade de 1,26 g ml deve ser tomada para preparar uma solução aquosa c.42. ... 111 g de anidrido ftálico e 46 g de glicerina com densidade de 28 V são colocados em um béquer de vidro com capacidade de 0,25 l.
Como calcular a densidade e a viscosidade de um líquido contendo água, álcool e glicerina?
Para isso, são vendidos reômetros. você não precisa contar nada. apenas congelar.
trietilenoglicol. propileno glicol. Glicerol. … propilenoglicol 40%. -25 C. ... A densidade de soluções aquosas de etileno glicol em várias temperaturas.
Você precisa saber a porcentagem de todos os componentes da mistura (pelo menos!)
Sem chance. É, procure dados recebidos por alguém.
Por favor, ajude, um pedaço de gelo flutua na gasolina, querosene, glicerina? porque?
Será em glicerina, não flutua em uísque - a densidade é aproximadamente a mesma da gasolina
Também aumenta a densidade da solução acabada e melhora a qualidade das bolhas. ... Solução de glicerina garrafa de 25gTula Pharmaceutical Factory LLC. … Solução de tetraborato de sódio em frasco de glicerina 20% 30g, Samara FF, Samara Rússia.
O gelo é menos denso que o óleo, então será.
Compare a densidade do gelo com a densidade desses líquidos. se a densidade do gelo for menor, ele flutuará; se for maior, ele afundará.
Não sei. depende de qual peça. se houver ar suficiente no gelo para mantê-lo na superfície, ele flutuará, e se não houver, então não. tente você mesmo. querosene é barato.
Dependendo de qual temperatura este gelo é resfriado a
O ponto de ebulição das soluções aquosas de glicerina diminui com a diminuição da concentração de glicerol com um teor de 5% de água, o ponto de ebulição é 160-161, sua densidade é 1,26362 g cm3. … 25 25 C . ZnCl2.
Eu nunca vi gelo flutuando no tanque de gasolina e na vasilha. E ele certamente é))). Então ele provavelmente está no fundo. Eu vi glicerina apenas em um frasco e no calor))).
Oi!
X quantidade de glicerol diluído, g Uma densidade de glicerol destilado, g ml ... Soluções de glicerol a uma concentração de 25% e acima não estão sujeitas a contaminação microbiana, soluções mais diluídas são ...
Um pedaço de gelo flutuará na gasolina, querosene, glicerina?
Descubra a densidade e pronto!
Densidade de soluções aquosas de álcoois. As densidades de soluções aquosas g cm3 a 20 C são dadas para as seguintes substâncias: etanol, 1-propanol, 2-propanol, etilenoglicol, glicerol, D-manitol.
Sim)))
Se a densidade do gelo for menor que a densidade do líquido, então o gelo flutuará
Qual é a densidade da glicerina a uma temperatura de 24 gr. COM?
Glicerina Graus Celsius020406080100120140169180Densidade g/cm3126712591250123812241208118811631126
Para uma temperatura de 24 graus = determinar por interpolação entre 20 e 40 graus
Calcule o ponto de ebulição de uma solução a 8% de glicerol C3H6O3 em acetona. A resposta é 57,7oC. 4.Uma solução, da qual 100 ml contém 2,3 g... Tome a densidade da solução igual a um. Resposta 608 Pa. Bilhete 14 25 1. Quantos gramas de BaCl2 2H2O ...
Perguntas sobre Química))) e Física. Qual líquido é mais denso que a água e também conduz eletricidade, mas não o metal?
Glicerina, etilenoglicóis, formamidas, butirolactona, quase todos os ácidos, aminas. e muito mais.
Concentração de ácido sulfúrico, % em massa. Densidade a 25 C, g cm. ... 25,60-0,1950 0,000 8 - umidade relativa,% - índice de refração de uma solução aquosa de glicerol a 25 C para linha D sódio - temperatura da solução, C ...