Експлоатација

Код ванадијумских проточних батерија, обе референтне електроде су додатно повезане са резервоарима за складиштење и пумпама тако да веома велике количине електролита могу да циркулишу кроз ћелију. Циркулација течног електролита је донекле отежана и ограничава употребу ванадијумских батерија у индустријама које захтевају мобилност, што их чини ефикасним у великим стационарним зградама.
Када се ванадијумска батерија напуни, јони ВО2+ у позитивно наелектрисаној референтној електроди претварају се у јоне ВО2+ када се електрони одвоје од позитивног терминала батерије. Слично, у негативној референтној електроди, електрони претварају јоне В3+ у В2+. Током пражњења, овај процес је обрнут, што резултира напоном отвореног кола од 1,41 В на 25°Ц.
Остала корисна својства ванадијумских проточних батерија укључују веома брз одговор на промене оптерећења и изузетно висок капацитет преоптерећења. Истраживање на Универзитету Новог Јужног Велса показало је да могу постићи време одзива мање од пола милисекунди при промени оптерећења од 100% и да издрже 400% преоптерећења више од 10 секунди. Време одзива је у већини случајева ограничено електричном опремом. Ванадијумске батерије на бази сумпорне киселине раде само на температурама од 10-40Ц. Ако је температура испод овог опсега, јони сумпорне киселине кристалишу. Ефикасност повратног кретања у свакодневној употреби остаје на нивоу од 65-75%.
Карактеристике пуњења и пражњења
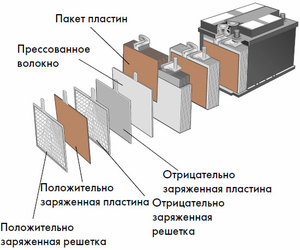
Алгоритми пуњења директно зависе од тога како је батерија распоређена и којој врсти припада. На пример, неке батерије могу безбедно да допуне свој капацитет из извора константног напона. Други раде само са подесивим извором струје који може да мења параметре у зависности од нивоа напуњености.
Неправилно организован процес пуњења може оштетити батерију. У екстремним случајевима, батерија се може запалити или експлодирати. Постоје паметне батерије опремљене уређајима за праћење напона. Главни параметри које треба узети у обзир при раду реверзибилних галванских батерија су:
- Животни век. Чак и уз правилно руковање, број циклуса пуњења батерије је ограничен. Различити системи батерија се не троше увек из истих разлога. Али генерално, век трајања батерије је првенствено ограничен бројем циклуса пуњења-пражњења, а друго, пројектованим радним веком без обзира на интензитет употребе.
- Време пуњења. Основни дизајн батерије не подразумева пуњење произвољно великом брзином: унутрашњи отпор галванске ћелије ће довести до претварања вишка струје пуњења у топлоту, што може неповратно оштетити уређај. Са физичке тачке гледишта, време пуњења је ограничено максималном брзином дифузије активног материјала кроз електролит.Поједностављено, можемо претпоставити да је обнављање пуног капацитета за сат времена добар показатељ.
- Дубина пражњења. Наведен као проценат називне снаге. Описује употребљиви капацитет. За различите типове батерија, препоручени радни ниво пражњења може да варира. Због промена у раду или старења, индикатор максималне дубине губи своју првобитну вредност.
процес дифузије.
Због процеса дифузије, поравнања густине електролита у шупљини кућишта батерије и у порама активне масе плоча, поларизација електрода се може одржати у батерији када је екстерно коло искључено.
Брзина дифузије директно зависи од температуре електролита, што је температура виша, то се процес одвија брже и може значајно да варира у времену, од два сата до једног дана. Присуство две компоненте електродног потенцијала у прелазним условима довело је до поделе на равнотежни и неравнотежни ЕМФ батерије. На равнотежни ЕМФ батерије утичу садржај и концентрација јона активних супстанци у електролиту, као и хемијска и физичка својства активних супстанци. Главну улогу у величини ЕМФ-а игра густина електролита и температура практично не утиче на то. Зависност ЕМФ од густине може се изразити формулом:
ЕМФ батерије није једнак напону батерије, што зависи од присуства или одсуства оптерећења на његовим терминалима.
админ25/07/2011
Коментар
име *
Сајт
Овај сајт користи Акисмет за борбу против нежељене поште. Сазнајте како се обрађују подаци о вашим коментарима.
« Механички тахометар
Напон батерије »
Ознаке
ВАЗ, ВАЗ кварови Сензори Паљење Ињектор Уређаји Стартер Шеме Електрични аутомобили Напајање ваз 2110 газела газела пословни регистри поправка аутомобила
Недавни уноси
- Сензори у аутомобилу: врсте и намена
- Највећи електрични аутомобил на свету ЕДумпер,
- Ласерска светла.
- Предности и мане халогених сијалица
- Уређај и принцип рада паркинг сензора
Арцхивес
Архива Изаберите септембар 2019. августа 2017. јула 2017. јун 2017. маја 2017. априла 2017. март 2017. октобар 2016. новембар 2016. октобар 2016. јул 2016. јун 2016. маја 20. фебруара 20. новембар 20. март 20.15. августа 2015. године 20. фебруара 20. јула 2015. године 20. маја 20. фебруара 20. маја 20. јун 20. маја 20. јун 20. маја 20. јун 20. маја 2015. године. јануар 2015. децембар 2014. новембар 2014. октобар 2014. септембар 2014. август 2014. јул 2014. јун 2014. мај 2014. април 2014. фебруар 2014. јануар 2014. 2012, 2012, 2011, 2012, 2011, 2012, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, Септембар 2012, 2011, 2011, 2011, 2011, 2011, 2011
Категорије
- Акумулаторска батерија
- Видео
- Генератор
- Сензори
- Дијагностика
- Паљење
- вести
- Опрема
- Уређаји
- Репаир
- Свећица
- Стартер
- Шема
- Уређаји
- електрични аутомобили
- Напајање
Налазимо се на друштвеним мрежама
Ауто електричар@ Сва права задржана. Када копирате материјале сајта, морате да наведете везу до сајта.
Уређај и принцип рада
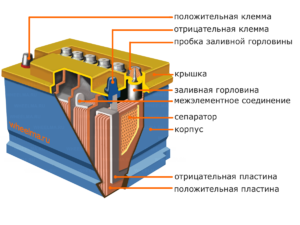
Свака таква ћелија има катоду (позитивну електроду) и аноду (негативну). Ове електроде су одвојене електролитом који обезбеђује размену јона између њих. Материјали електрода и састав електролита се бирају тако да обезбеде довољну електромоторну силу између терминала батерије.
Пошто електроде садрже ограничен потенцијал хемијске енергије, батерија ће се испразнити током рада. Тип галванских ћелија, који је прилагођен за допуну након делимичног или потпуног пражњења, назива се батерија. Склоп таквих међусобно повезаних ћелија је батерија.Рад батерије укључује цикличну промену два стања:
- Пуњење - батерија ради као пријемник електричне енергије, унутар ћелија се електрична енергија остварује у хемијским променама.
- Пражњење – уређај функционише као извор електричне струје претварајући енергију хемијских реакција у електричну енергију.
Области употребе
Карактеристика ултрависоког капацитета ванадијум редокс батерија чини их погодним за употребу у индустријама које захтевају високо складиштење енергије. На пример, помагање у балансирању обима производње таквих извора енергије као што су ветар или соларна енергија, или помоћ генераторима да апсорбују велике таласе енергије када је то потребно, или балансирање понуде и потражње за енергијом за удаљена подручја.
Ограничене карактеристике самопражњења ванадијум редокс батерија чине их корисним у индустријама у којима се батерије морају складиштити током дугог временског периода уз минимално одржавање и спремност. То је довело до њихове употребе у неким врстама војне електронике, на пример, у сензорима рударског система ГАТОР. Њихова способност да круже и остану на нули чини их погодним за соларне апликације и индустрије у којима батерије морају започети дан празне и пунити се на основу оптерећења и временских прилика. На пример, литијум-јонске батерије се често оштећују када им се дозволи да се испразне испод 20% своје запремине, тако да најчешће раде у опсегу од 20 до 100%, што значи да могу да искористе само 20% свог номиналног капацитета.
Њихово изузетно брзо време одзива их такође чини практично незаменљивим за непрекидно напајање, где се могу користити уместо оловних батерија, па чак и дизел генератора. Такође, брзо време одзива их чини погодним за контролу фреквенције. У овом тренутку, ни УПС ни мере управљања фреквенцијом нису ефикасне саме по себи, али је вероватно да ће батерија моћи да нађе примену у овим индустријама када се капитализује из различитих извора финансирања. Поред тога, ове могућности чине ванадијум редокс батерије ефикасним „једноделним“ решењем за мале електричне мреже које зависе од поузданог рада, контроле фреквенције и потреба за пребацивањем оптерећења (као што је велика пенетрација обновљивих извора енергије, веома флуктуирајућа оптерећења или жеља да се оптимизовати ефикасност генератора са померањем времена одзива).
Највеће радне ванадијум редокс батерије
Подстаница "Минами Хиакита":
- Датум лансирања: децембар 2015
- Енергија: 60 МВх
- Снага: 15 МВ
- Радно време: 4 сата
- Држава: Јапан
Стинки, провинција Лиаонинг
- Датум лансирања: Н/А
- Енергија: 10 МВх
- Снага: 5 МВ
- Радно време: 2 сата
- Земља: Кина
Ветроелектрана Томамае
- Датум лансирања: 2005
- Енергија: 6 МВх
- Снага: 4 МВ
- Радно време: 1 сат 30 минута
- Држава: Јапан
Зхангбеи Пројецт
- Датум лансирања 2016
- Енергија: 8 МВх
- Снага: 2 МВ
- Радно време: 4 сата.
- Земља: Кина
Пројекат СноПУД МЕСА 2
- Датум лансирања: март 2017
- Енергија: 8 МВх
- Снага: 2 МВ
- Радно време: 4 сата.
- Држава: САД
Подстаница у Ескондиду
- Датум лансирања: 2017
- Енергија: 8 МВх
- Снага: 2 МВ
- Радно време: 4 сата.
- Држава: САД
Подстаница у Пуллману, Вашингтон
- Датум лансирања: април 2015
- Енергија: 4 МВх
- Снага: 1 МВ
- Радно време: 4 сата
- Држава: САД
Очекује се да ће до 2018. године у Кини бити завршен развој ванадијум редокс батерије. Његова енергија ће бити 800 МВх, снага - 200 МВ, а време рада - 4 сата.
Услови
- Секвенцијални - елементи следе један за другим.
- Електромоторна сила (ЕМФ) је напон који генерише батерија или магнетна сила у складу са Фарадејевим законом.
- Паралелно - Електричне компоненте су распоређене тако да струја тече дуж два или више пута.
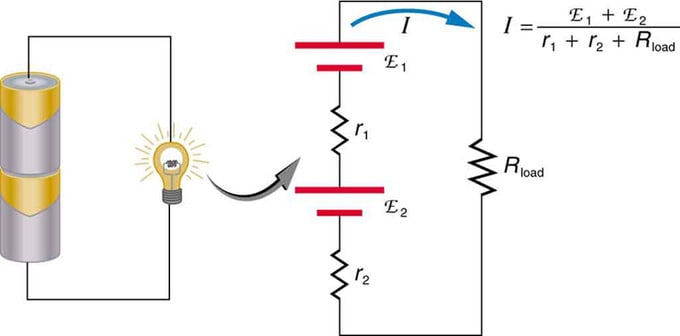
Ако користите више извора напона, они могу бити повезани серијски или паралелно. Са серијском верзијом, они су подешени у истом правцу, унутрашњи отпор је увећан, а електромоторна сила се додаје алгебарски. Слични типови су уобичајени у батеријским лампама, играчкама и разним другим уређајима. Ћелије се постављају у серију да би се повећала укупна емф.
Серијско повезивање два извора напона у истом правцу. На дијаграму је приказан фењер са две ћелије и једном лампом
Батерија - вишеструко повезивање волтних елемената. Али постоји један недостатак у серијској вези, јер се додају унутрашњи отпори. Понекад ово ствара проблеме. Рецимо да имате две батерије од 6В које сте убацили уместо уобичајених 12В. Као резултат тога, додали сте не само ЕМФ, већ и унутрашњи отпор сваке батерије.
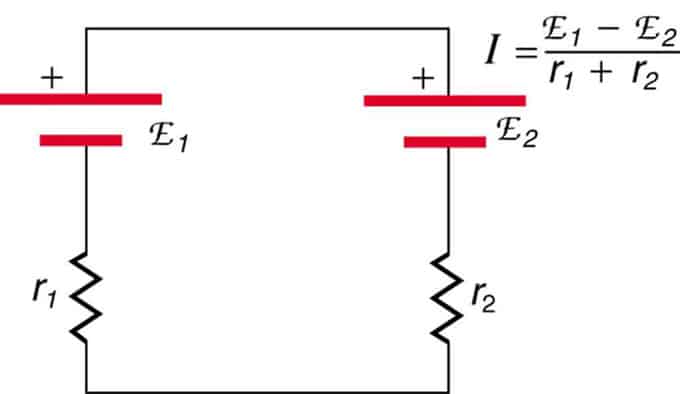
Ако се ћелије налазе у опозицији (једна се налази иза друге), онда ће се укупни ЕМФ смањити.
То су два извора напона повезана у серију са супротним емисијама. Струја тече у правцу веће ЕМФ и ограничена је збиром унутрашњих отпора. Пример је пуњач. Мора да има више емф од батерије
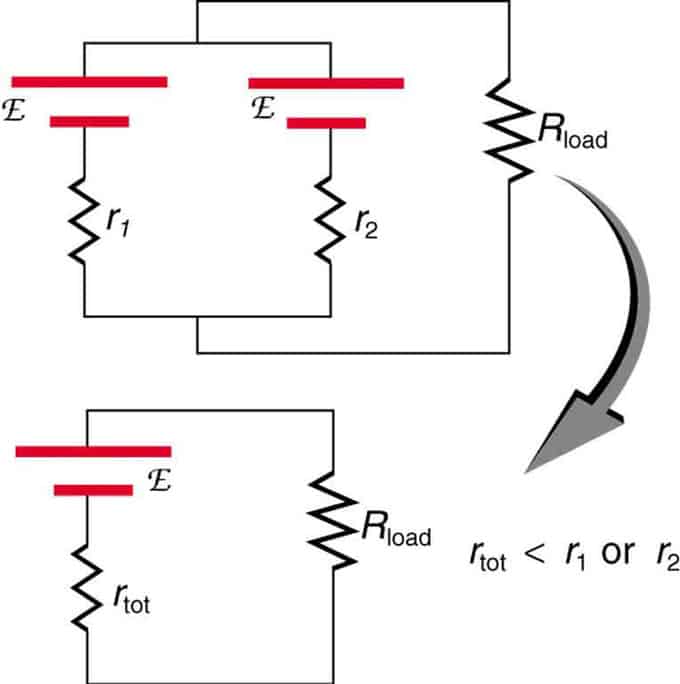
Ако се два извора са истом електромоторном силом налазе паралелно и споје на отпор оптерећења, онда укупна ЕМФ остаје иста као и појединачни. Међутим, укупни унутрашњи отпор ће бити смањен. Испоставило се да паралелна верзија може да генерише више струје.
Два извора напона са једним ЕМФ су комбиновани у паралелној вези. Они формирају један ЕМФ, али имају мањи укупни отпор него појединачно. Сличне комбинације се користе ако треба да постигнете више струје.
| Преглед |
|
| Паралелно и серијско повезивање отпорника |
|
| Кирхофова правила |
|
| Волтметри и амперметри |
|
| РЦ Цирцуитс |
|
Историјски преглед
За развој прве галванске ћелије заслужан је италијански физичар Алесандро Волта. Извео је низ експеримената са електрохемијским појавама током 1790-их и око 1800. године створио је прву батерију, коју су његови савременици назвали „волтаични стуб“. Уређај се састојао од наизменичних дискова цинка и сребра одвојених слојевима папира или тканине који су били натопљени раствором натријум хидроксида.
Ови експерименти су постали основа за рад Мајкла Фарадаја о квантитативним законима електрохемије. Он је описао принцип рада батерије и на основу рада научника створене су прве комерцијалне електричне ћелије. Даља еволуција је изгледала овако:
- Британски хемичар Џон Данијел је 1836. године представио побољшани модел ћелије, који се састоји од бакарних и цинканих електрода уроњених у хлороводоничну киселину. Даниелов елемент је могао да обезбеди константан напон неупоредиво ефикасније од Волтових уређаја.
- 1839. године Даљи напредак направио је физичар Грове са својом двотечном ћелијом, која се састојала од цинка уроњеног у разблажену сумпорну киселину у порозној посуди. Потоњи је одвојио сумпорну киселину из посуде која садржи азотну киселину са платинском катодом постављеном у њој. Азотна киселина је служила као оксидационо средство за спречавање губитка напона услед акумулације водоника на катоди.Немачки хемичар Роберт Бунсен заменио је платину јефтиним угљеником у Грове ћелији и тиме промовисао широко прихватање ове врсте батерија.
- Године 1859. Гастон Планте је изумео ћелију са оловном киселином, претечу модерног акумулатора за аутомобиле. Плантеов уређај је био у стању да произведе необично велику струју, али је скоро две деценије коришћен само за експерименте у лабораторијама.
- 1895-1905 године. Проналазак никл-кадмијум и никл-гвожђе алкалних елемената. Ово је омогућило стварање система са значајним бројем циклуса пуњења-пражњења.
- Од 1930-их година почиње развој сребро-цинк и живино-цинк алкалних батерија, које су давале високу густину енергије по јединици тежине и запремине.
- Од средине 20. века, напредак у технологији производње и појава нових материјала довели су до још моћнијих и компактнијих батерија. Најзначајније је било увођење никл-метал хидридних и литијум батерија на тржиште.
Пуњење батерија
Главни чланак: пуњач
Како се хемијска енергија троши, напон и струја опадају, а батерија престаје да функционише. Можете пунити батерију (батерију батерија) из било ког извора једносмерне струје са вишим напоном док ограничавате струју. Најчешћа је струја пуњења (у амперима), пропорционална 1/10 условног називног капацитета батерије (у ампер сатима).
Међутим, на основу техничког описа који дистрибуирају произвођачи електричних батерија које се широко користе (НиМХ, НиЦд), може се претпоставити да је овај начин пуњења, који се обично назива стандардне, обрачунава се на основу трајања осмочасовног радног дана, када се батерија, испражњена на крају радног дана, прикључи на мрежни пуњач пре почетка новог радног дана. Употреба таквог режима пуњења за ове врсте батерија са систематском употребом омогућава вам да одржите равнотежу квалитета и трошкова у раду производа. Дакле, на предлог произвођача, овај режим се може користити само за никл-кадмијум и никл-метал хидридне батерије.
Многе врсте батерија имају различита ограничења која се морају узети у обзир током пуњења и накнадне употребе, на пример, НиМХ батерије су осетљиве на прекомерно пуњење, литијумске батерије су осетљиве на прекомерно пражњење, напон и температуру. НиЦд и НиМХ батерије имају такозвани меморијски ефекат, који се састоји у смањењу капацитета када се пуњење врши када батерија није потпуно испражњена. Такође, ове врсте батерија имају приметно самопражњење, односно постепено губе напуњеност без повезивања са оптерећењем. За борбу против овог ефекта може се користити кап по кап.
Методе пуњења батерије
За пуњење батерија користи се неколико метода; Генерално, начин пуњења зависи од типа батерије.
- Споро ДЦ пуњење
Пуните једносмерном струјом пропорционалном 0,1-0,2 условног називног капацитета К око 15-7 сати, респективно.
Најдужи и најсигурнији начин пуњења. Погодно за већину типова батерија.
- брзо пуњење
Пуните једносмерном струјом пропорционалном 1/3 К око 3-5 сати.
- Убрзано или "делта-В" пуњење
Пуњење са почетном струјом пуњења пропорционалном називном називном капацитету батерије, при чему се напон батерије константно мери и пуњење се завршава након што се батерија потпуно напуни. Време пуњења је око сат и по. Батерија се може прегрејати, па чак и уништити.
- обрнути пуњење
Изводи се наизменичним дугим импулсима пуњења са кратким импулсима пражњења. Обрнути метод је најкориснији за пуњење НиЦд и НиМХ батерија које се одликују тзв.н. „ефекат меморије“.