Шта одређује салинитет морске воде
Видећи мало већу цифру 3,5 ппм
, могли бисте помислити да је то константа за сваку морску воду на нашој планети. Али све није тако једноставно, сланост зависи од региона. Десило се да што се регион налази северније, то је ова вредност већа.
Југ се, напротив, може похвалити не тако сланим морима и океанима. Наравно, сва правила имају своје изузетке. Ниво соли у морима је обично нешто нижи него у океанима.
Каква је уопште географска подела? Не зна се, истраживачи узимају здраво за готово, има свега. Можда би одговор требало тражити у ранијим периодима развоја наше планете. Не у време када се живот родио – много раније.
Већ знамо да салинитет воде зависи од присуства:
- магнезијум хлорид.
- натријум хлорид.
- друге соли.
Можда су у неким деловима земљине коре налазишта ових материја била нешто већа него у суседним регионима. С друге стране, морске струје нико није отказао, пре или касније општи ниво је морао да се изједначи.
Дакле, највероватније је мала разлика повезана са климатским карактеристикама наше планете. Није најнеоснованије мишљење, ако се сећате мраза и размислите шта тачно вода са високим садржајем соли спорије се смрзава.
Фазе замрзавања
Веома је занимљиво гледати како се морска вода смрзава. Није одмах прекривен једноличном леденом кором, као слатка вода. Када се део претвори у лед (а свеж је), остатак запремине постаје још сланији, а за замрзавање је потребан још јачи мраз.
Врсте леда
Како се море хлади, формирају се различите врсте леда:
- снежна олуја;
- муљ;
- игле;
- Сало;
- нилас.
Ако се море још није смрзло, али му је веома близу, а у то време пада снег, оно се не топи када дође у додир са површином, већ се засити водом и формира вискозну кашасту масу која се зове снег. Смрзнувши се, ова каша се претвара у муљ, што је веома опасно за бродове захваћене олујом. Због тога је палуба тренутно прекривена леденом кором.
Када термометар достигне ознаку неопходну за замрзавање, у мору почињу да се формирају ледене иглице - кристали у виду веома танких шестоугаоних призми. Сакупљајући их мрежом, испирући со и топећи их, видећете да су безукусни.
Када постане још хладније, маст почиње да се смрзава и формира ледену кору, провидну и крхку као стакло. Такав лед се назива нилас, или флаша. Слано је, иако се формира од бесквасних иглица. Чињеница је да током замрзавања иглице хватају и најмање капи околне слане воде.
Само у морима постоји такав феномен као што је плутајући лед. Настаје зато што се вода овде брже хлади са обале. Лед који се тамо створио смрзава се до обалне ивице, због чега је назван брзим ледом. Како се мраз појачава током мирног времена, он брзо заузима нове територије, понекад достижући и десетине километара у ширину. Али чим се подиже јак ветар, брзи лед почиње да се ломи на комаде различитих величина. Ове ледене плохе, често огромне (ледена поља), ветар и струја носе по мору, стварајући проблеме бродовима.
Десалинизација морске воде.
Што се десалинизације тиче, сви су бар понешто чули, неки се сада сећају и филма „Водени свет“. Колико је реално ставити један такав преносиви дестилатор у сваку кућу и заувек заборавити на проблем пијаће воде за човечанство? И даље фантазија, а не стварност.
Све је у утрошеној енергији, јер су за ефикасан рад потребни огромни капацитети, ни мање ни више него нуклеарни реактор. По овом принципу ради постројење за десалинизацију у Казахстану.Идеја је поднета и на Криму, али снага севастопољског реактора није била довољна за такве запремине.
Пре пола века, пре бројних нуклеарних катастрофа, још се могло претпоставити да ће мирни атом ући у сваки дом. Постојао је чак и слоган. Али већ је јасно да нема употребе нуклеарних микрореактора:
- У кућним апаратима.
- У индустријским предузећима.
- У конструкцији аутомобила и авиона.
- И да, у границама града.
Не очекује се у наредном веку. Наука ће можда направити још један скок и изненадити нас, али за сада су то само фантазије и наде немарних романтичара.
Тачка смрзавања дестиловане воде
Да ли се дестилована вода смрзава? Подсетимо, да би се вода смрзла, неопходно је да у њој постоје неки центри за кристализацију, а то могу бити мехурићи ваздуха, суспендоване честице, као и оштећења зидова посуде у којој се налази.
Дестилована вода, потпуно лишена икаквих нечистоћа, нема језгра кристализације, па стога њено замрзавање почиње на веома ниским температурама. Почетна тачка смрзавања дестиловане воде је -42 степена. Научници су успели да постигну суперхлађење дестиловане воде на -70 степени.
Вода која је била изложена веома ниским температурама, али није кристализована, назива се „прехлађена“. Можете ставити флашу дестиловане воде у замрзивач, постићи хипотермију, а затим показати веома ефикасан трик - погледајте видео:
Нежним тапкањем по бочици извађеној из фрижидера или убацивањем малог комадића леда у њу, можете показати како се тренутно претвара у лед, који изгледа као издужени кристали.
Дестилована вода: да ли се ова пречишћена супстанца смрзава или не под притиском? Такав процес је могућ само у посебно створеним лабораторијским условима.
НаННолНемпеНаНННа
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð нÐ нÐ нÐ нÐ н н н н н н н н н н н н н н н н н н н н н н н н н н н н н н н н Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δ¶¶Ð Ð Ð Ð δÐ Ð Ð Ð δÐ Ð Ð Ð δРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРвÐμÐ »НвÐμл РвÐμÐ »НвÐμл Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ЛвÐμÐ »НÐ МУРХОТ» РРРРРРРРРРРРРРРРРРРРРРвÐμÐ »НвÐμР» НиННН. Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ННμНННННННН ° ° ° ° ° ° ННННР ннн Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Н: »Ð ²Ðððð ооо²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ²Ð Ð Ð ² ДНД »Ð НоÐ'ÐμНжР° ниÐμ Нол Н Н НД ° ННоР»Н мÐμнННÐμ, НÐμм ННÐμÐ ± НÐμмоÐμ л Ð НвНÐμкНиНÐμНкого НД ° ННвоНÐ °, воÐ'Ð ° ННкоНÐ¸Н Ð ±Назование кНиННаллов лНда пНи пНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНа ¸ оНлажденННаиоиии Руннинг нðμμðððμð½ððÐμÐμÐ Н А¾ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Д Д ¸НивР° ÐμН ÐºÐ¾Ð¸НÐμиННÐ ° НÐ½Н Нони оННÐ ° Ð »Ннои НННÐ ° НÐ¸Н Нои оННÐ ° л Ннон НННÐ ° НÐ¸Н НÐ½Н НÐ½Н Нои оНÐ ° НнН! Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð н н н н н н Ð ° Ð ° н °
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð н н н н н н н ° С ° Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð μн ÐÐ ° мÐμНÐ · Р ° ниÐμ НвНÐμкНиНÐμНкого НД ° ННвоНÐ ° в ННо пНоНÐμНН С ННД ° ННиÐμм НкНННой НÐμпР»Ð¾НН, поННÐ¾Ð¼Н НÐμмпÐμНÐ ° НННÐ ° оННÐ ° ÐμННН Ð½ÐμиР· менной. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðн Ðн Ðн² . Ð Ð · н н н н н Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð н ннÐ Ð ° Ð ° Ð Ð Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ¸ поННоНннойÐÐ ° ниНи иНоНÐμНН Ð¸НниÐμнНÐНННН Ð² нР»Ð ° ННииНÐ ° НННН Ð¸НиР° НиНÐμл НН Ð¸Ни ННÐ ° нНноННнНооНнНоÐ'ккНоÐ'НÐ ° .
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð ° а ¸Н и НлоНида наННиН. Ð ° ННÐ²Ð¾Н НÐ »Ð¾НнÐ'Ð ° кР° л ННÐ¸Н Ð¸НÐμиÐ'Ðμ вНÐμиÐμ вНÐμио иНиоР»НÐ · НÐμННН Ð² ÐμнННН Ð¸НоНÐНН Ð¸НоНÐННРНÐ ° Н Ð½НÐНР ¸ замоНаживании пНодНкНов, ННанен, ННанеинеи 17.8 А°Ð¡. Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 °Ц Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð · Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð НННÐÐÐÐ ° Ð НННÐÐ'НкНÐ ° н Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð НННонНÐ °ÐºН НаННооа НоНлаждаемНм пНодНкНом.
Ð ° ННÐ²Ð¾Н НÐ »Ð¾НиÐ'Ð ° нР° ННÐ¸Н (ииНÐμвои Нол и) иÐμ иоНРÐ¸Н Ð¸Ð¸НÐμвНÐμНÐμнНÐμН. онððð Ð ° Ð ° НД Ð Ð ðнððРРРРРРРРРРРРРРРоÐμ Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ÐÐ Ð Ð Ðнннннннн 1 А°Ð¡. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ·
ЦИКЛУС ВОДЕ У СВЕТСКОМ ОКЕАНУ
У поларним пределима вода, хладећи се, постаје гушћа и тоне на дно. Одатле полако клизи према екватору. Дакле, на свим географским ширинама дубоке воде су хладне. Чак и на екватору, доње воде имају температуру од само 1-2 ° изнад нуле.
Пошто струје носе топлу воду од екватора до умерених географских ширина, хладна вода се веома споро диже из дубина да би заузела своје место. На површини се поново загрева, иде у субполарне зоне, где се хлади, тоне на дно и поново се креће по дну до екватора.
Дакле, у океанима постоји нека врста циклуса воде: на површини, вода се креће од екватора до субполарних зона и дуж дна океана - од субполарних зона до екватора. Овај процес мешања воде, заједно са другим горе поменутим феноменима, ствара јединство океана.
Ако пронађете грешку, означите део текста и кликните Цтрл+Ентер
.
У одељку о томе шта се може постићи најнижа температура водено-солног раствора обичне (кухне, НаЦл) соли, дато од аутора европски
најбољи одговор је Додавањем соли у воду, брзина топљења леда се повећава и температура топљења леда пада нижа. То је зато што додавање соли изазива слабљење молекуларне кохезије и уништавање кристалне решетке леда. Отапање смеше леда и соли тече одвођењем топлоте из околине, услед чега се околни ваздух хлади и његова температура опада. Са повећањем садржаја соли у смеши леда и соли, његова тачка топљења се смањује. Раствор соли са најнижом тачком топљења назива се еутектик, а његова температура топљења се назива криохидратна тачка. Криохидратна тачка за мешавину ледене соли и кухињске соли је -21,2°Ц, са концентрацијом соли у раствору од 23,1% у односу на укупну масу смеше, што је приближно једнако 30 кг соли на 100 кг лед.Са даљим повећањем концентрације соли, не ради се о смањењу температуре топљења смеше леда и соли, већ о повећању температуре топљења (при концентрацији соли у раствору од 25% на укупну масу, температура топљења расте до -8°Ц).При замрзавању воденог раствора кухињске соли у концентрацији која одговара тачки криохидрата добија се хомогена смеша леда и кристала соли која се назива еутектички чврсти раствор.Тачка топљења еутектичког чврстог раствора. натријум хлорида је -21,2 ° Ц, а топлота фузије је 236 кЈ / кг. Еутектички раствор се користи за хлађење без обртног момента. Да би се то урадило, еутектички раствор кухињске соли се сипа у нуле - чврсто затворене форме - и оне се замрзавају. Замрзнуте нуле се користе за хлађење пултова, ормара, хлађених преносивих расхладних торби итд (отворите замрзивач кућног фрижидера - наћи ћете такав контејнер) У трговини је хлађење ледом и соли било широко коришћено пре масовне производње опреме. са машинским хлађењем.
Одговор од пресуше
најнижа температура било које температуре је апсолутна нула, око -273 степена Целзијуса
Одговор од Олиа
температура зависи од концентрације соли у раствору, што је већа концентрација, то је нижа тачка смрзавања. референтна књига ми је на неко време одузета)) али ако пођемо од чињенице да је морска вода слани раствор, онда можемо закључити да је температура смрзавања много нижа од нуле .... степени -15-20
Одговор од способан
22,4% водени раствор НаЦл се смрзава на 21,2 °Ц
на питање Водени раствор НаЦл "температура кристализације"
Одговор од Иергеи Незнамов
Табела 10.8. Тачка смрзавања садржаја НаЦл раствора НаЦл, г у 100 г воде 5 - -4,4 9,0 - -5,4 10,6 - -6,4 12,3 - -7,5 14,0 - -8,6 15,7 - -9,8 17,5 - -11,0 19,2 - 12,2 - 12,3 - - - 15,1 25,0 - - 16,0 26,9 - -18,2 29,0 - -20,0 30,1 — -21,2
Тачка смрзавања слане воде
Експерименти са ледом за децу су увек занимљиви. Док сам спроводио експерименте са Владом, чак сам направио неколико открића за себе.
Данас ћемо пронаћи одговоре на следећа питања:
- Како се вода понаша када је замрзнута?
- Шта се дешава ако замрзнете слану воду?
- капут ће загрејати лед?
- и неки други…
смрзавање воде

Да ли се слана вода смрзава?
Што је вода сланија, нижа је тачка смрзавања. За експеримент смо узели две чаше - у једној слаткој води (означена словом Б), у другој веома сланој (означена словима Б + Ц).
После стајања у замрзивачу целе ноћи, слана вода се није смрзла, већ су се у чаши формирали кристали леда. Свежа вода се претворила у лед. Док сам ја манипулисао шољицама и растворима соли, Владик је направио свој непланирани експеримент.
Сипао је воду, биљно уље у шољу и дискретно ставио у замрзивач. 
Слана вода у замрзивачу се није смрзла, али шта се дешава ако поспите со по леду? Хајде да проверимо.
Искуство са ледом и сољу
Узмите две коцке леда. Једну посолите, а другу оставите за поређење. 
Замрзнули смо велику леденицу и посули је сољу, узели четке и 
Наша искусна креативност уједињује целу породицу, па је Макарушкинова оловка ушла у објектив фотоапарата!
Макар и Влад су веома сви воле да се смрзавају
. Понекад се у замрзивачу налазе потпуно неочекивани предмети.
Од детињства сам сањао да доживим ово искуство, али моја мајка није имала бунду, и многе

Како је сјајно бити одрастао, имати бунду и радити разне експерименте са децом!
Ваша Галина Кузмина
У табели су приказана термофизичка својства раствора калцијум хлорида ЦаЦл 2 у зависности од температуре и концентрације соли: специфична топлота раствора, топлотна проводљивост, вискозитет водених раствора, њихова топлотна дифузивност и Прандтлов број. Концентрација соли ЦаЦл 2 у раствору је од 9,4 до 29,9%. Температура на којој се дају својства одређена је садржајем соли у раствору и креће се од -55 до 20°Ц.
калцијум хлорид ЦаЦл 2 не сме да се смрзне до минус 55°С
. Да би се постигао овај ефекат, концентрација соли у раствору треба да буде 29,9%, а његова густина ће бити 1286 кг/м 3 .
Са повећањем концентрације соли у раствору, повећава се не само његова густина, већ и термофизичка својства као што су динамичка и кинематичка вискозност водених раствора, као и Прандтлов број. На пример, динамички вискозитет раствора ЦаЦл 2
са концентрацијом соли од 9,4% на температури од 20°Ц износи 0,001236 Па с, а са повећањем концентрације калцијум хлорида у раствору на 30%, његов динамички вискозитет расте на вредност од 0,003511 Па с.
Треба напоменути да температура има најјачи утицај на вискозитет водених раствора ове соли. Када се раствор калцијум хлорида охлади од 20 до -55°Ц, његов динамички вискозитет се може повећати за 18 пута, а кинематичан за 25 пута.
С обзиром на следеће термофизичке особине раствора ЦаЦл 2
:
- , кг / м 3;
- тачка смрзавања °С;
- динамички вискозитет водених раствора, Па с;
- Прандтлов број.
НаННолНемпеНаНННа
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð нÐ нÐ нÐ нÐ н н н н н н н н н н н н н н н н н н н н н н н н н н н н н н н н Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δ¶¶Ð Ð Ð Ð δÐ Ð Ð Ð δÐ Ð Ð Ð δРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРРвÐμÐ »НвÐμл РвÐμÐ »НвÐμл Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ЛвÐμÐ »НÐ МУРХОТ» РРРРРРРРРРРРРРРРРРРРРРвÐμÐ »НвÐμР» НиННН. Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ННμНННННННН ° ° ° ° ° ° ННННР ннн Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Н: »Ð ²Ðððð ооо²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ²Ð Ð Ð ² ДНД »Ð НоÐ'ÐμНжР° ниÐμ Нол Н Н НД ° ННоР»Н мÐμнННÐμ, НÐμм ННÐμÐ ± НÐμмоÐμ л Ð НвНÐμкНиНÐμНкого НД ° ННвоНÐ °, воÐ'Ð ° ННкоНÐ¸Н Ð ±Назование кНиННаллов лНда пНи пНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНи оНа ¸ оНлажденННаиоиии Руннинг нðμμðððμð½ððÐμÐμÐ Н А¾ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Д Д ¸НивР° ÐμН ÐºÐ¾Ð¸НÐμиННÐ ° НÐ½Н Нони оННÐ ° Ð »Ннои НННÐ ° НÐ¸Н Нои оННÐ ° л Ннон НННÐ ° НÐ¸Н НÐ½Н НÐ½Н Нои оНÐ ° НнН!Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð н н н н н н Ð ° Ð ° н °
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð н н н н н н н ° С ° Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð μн ÐÐ ° мÐμНÐ · Р ° ниÐμ НвНÐμкНиНÐμНкого НД ° ННвоНÐ ° в ННо пНоНÐμНН С ННД ° ННиÐμм НкНННой НÐμпР»Ð¾НН, поННÐ¾Ð¼Н НÐμмпÐμНÐ ° НННÐ ° оННÐ ° ÐμННН Ð½ÐμиР· менной. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðн Ðн Ðн² . Ð Ð · н н н н н Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð н ннÐ Ð ° Ð ° Ð Ð Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ¸ поННоНнной ÐÐ ° ниНи иНоНÐμНН Ð¸НниÐμнНÐНННН Ð² нР»Ð ° ННииНÐ ° НННН Ð¸НиР° НиНÐμл НН Ð¸Ни ННÐ ° нНноННнНооНнНоÐ'ккНоÐ'НÐ ° .
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð ° а ¸Н и НлоНида наННиН. Ð ° ННÐ²Ð¾Н НÐ »Ð¾НнÐ'Ð ° кР° л ННÐ¸Н Ð¸НÐμиÐ'Ðμ вНÐμиÐμ вНÐμио иНиоР»НÐ · НÐμННН Ð² ÐμнННН Ð¸НоНÐНН Ð¸НоНÐННРНÐ ° Н Ð½НÐНР ¸ замоНаживании пНодНкНов, ННанен, ННанеинеи 17.8 А°Ð¡. Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 °Ц Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð · Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð НННÐÐÐÐ ° Ð НННÐÐ'НкНÐ ° н Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð НННонНÐ °ÐºН НаННооа НоНлаждаемНм пНодНкНом.
Ð ° ННÐ²Ð¾Н НÐ »Ð¾НиÐ'Ð ° нР° ННÐ¸Н (ииНÐμвои Нол и) иÐμ иоНРÐ¸Н Ð¸Ð¸НÐμвНÐμНÐμнНÐμН. онððð Ð ° Ð ° НД Ð Ð ðнððРРРРРРРРРРРРРРРоÐμ Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ÐÐ Ð Ð Ðнннннннн 1 А°Ð¡. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ·
На којој температури се морска вода може смрзнути?
Али на главно питање још није одговорено. Већ смо сазнали да со успорава смрзавање воде, море ће бити прекривено кором леда не на нули, већ на температурама испод нуле. Али колико далеко би очитавања термометра требало да иду у минус да становници приморских региона не чују уобичајени звук сурфања када напусте своје домове?
За одређивање ове вредности постоји посебна формула, сложена и разумљива само за специјалисте. Зависи од главног индикатора - ниво салинитета
. Али пошто имамо просечну вредност за овај индикатор, можемо ли пронаћи и просечну тачку смрзавања? Ох сигурно.
Ако не морате да израчунате све до стотог дела, за одређени регион, запамтите температуру на -1,91 степени
.
Можда се чини да разлика није тако велика, само два степена. Али током сезонских температурних колебања, ово може да игра огромну улогу где термометар пада најмање 0. Било би само 2 степена хладније, становници исте Африке или Јужне Америке могли би да виде лед у близини обале, али авај. Ипак, не мислимо да су они много узнемирени таквим губитком.
Термофизичка својства раствора НаЦл
У табели су приказана термофизичка својства раствора натријум хлорида НаЦл у зависности од температуре и концентрације соли. Концентрација натријум хлорида НаЦл у раствору је од 7 до 23,1%. Треба напоменути да када се водени раствор натријум хлорида охлади, његов специфични топлотни капацитет се незнатно мења, топлотна проводљивост се смањује, а вискозитет раствора се повећава.
С обзиром на следеће термофизичке особине раствора НаЦл
:
- густина раствора, кг/м 3 ;
- тачка смрзавања °С;
- специфични (масени) топлотни капацитет, кЈ/(кг дег);
- коефицијент топлотне проводљивости, В/(м дег);
- динамички вискозитет раствора, Па с;
- кинематичка вискозност раствора, м 2 /с;
- топлотна дифузивност, м 2 /с;
- Прандтлов број.
Од чега је направљена морска вода?
По чему се садржај мора разликује од слатке воде? Разлика није тако велика, али ипак:
- Много више соли.
- Преовлађују соли магнезијума и натријума.
- Густина се мало разликује, у року од неколико процената.
- Водоник сулфид се може формирати на дубини.
Главна компонента морске воде, ма колико то звучало предвидљиво, је вода. Али за разлику од воде река и језера, она садржи велике количине натријум и магнезијум хлорида
.
Салинитет се процењује на 3,5 ппм, али да буде јасније - на 3,5 хиљадитих дела процента укупног састава.
Па чак и ова, не најупечатљивија фигура, даје води не само специфичног укуса, већ је чини и непитком. Нема апсолутних контраиндикација, морска вода није отров или токсична супстанца, а од пар гутљаја се неће догодити ништа лоше. О последицама ће се моћи говорити ако је особа бар током дана.Такође, састав морске воде укључује:
- Флуор.
- бром.
- Калцијум.
- Калијум.
- Хлор.
- сулфати.
- Злато.
Истина, у процентима, сви ови елементи су много мањи од соли.
Стања и врсте вода
Вода на планети Земљи може имати три главна агрегатна стања: течно, чврсто и гасовито, који се могу трансформисати у различите облике који истовремено коегзистирају једни са другима (санте леда у морској води, водена пара и кристали леда у облацима на небу, глечери и слободни -текуће реке).
У зависности од карактеристика порекла, намене и састава, вода може бити:
- свеже;
- минерал;
- наутички;
- пиће (овде укључујемо воду из чесме);
- киша;
- одмрзнути;
- брацкисх;
- структурирано;
- дестилован;
- дејонизовани.
Присуство изотопа водоника чини воду:
- светлост;
- тешки (деутеријум);
- супертешки (трицијум).
Сви знамо да вода може бити мека и тврда: овај индикатор је одређен садржајем катјона магнезијума и калцијума.
Свака од врста и агрегатних стања воде које смо навели има своју тачку смрзавања и топљења.
Видео за замрзавање слане воде

 Шта знате о тачки кључања воде?
Шта знате о тачки кључања воде?

Температурни режим одређује, пре свега, брзину процеса замрзавања.
Температура у опсегу позитивних и негативних вредности утиче на брзину реакција, растворљивост једињења, брзину растварања, коагулацију, као и концентрацију недисоцираних јонских парова. Постоји неколико типова температуре у растворима: структурна, тачка смрзавања. Температура почетка кристализације (тачка смрзавања) - температура на којој, као резултат хлађења раствора, почиње формирање кристала. Депресија тачке смрзавања ΔТз је разлика између тачке смрзавања чистог растварача и раствора. Тачка смрзавања слане воде је увек испод тачке смрзавања чисте воде и зависи од концентрације растворених соли. Ова зависност за слане воде може се изразити једначином:
где ДО
- коефицијент пропорционалности; ВИТХ
је концентрација растворене супстанце у раствору.
У мање разблаженим растворима, температура почетка кристализације се одређује из дијаграма стања одговарајућег система. Пошто ће температура смрзавања морске воде и високо минерализованих природних сланих раствора бити различита, претпостављамо да ову температуру треба израчунати по различитим формулама.
Направљена је апроксимација експерименталних података о тачкама смрзавања раствора кухињске соли, морске воде и природних сланих раствора коришћених у раду. Зависности промена температуре смрзавања у графичком и аналитичком облику приказане су на сликама 41-43.
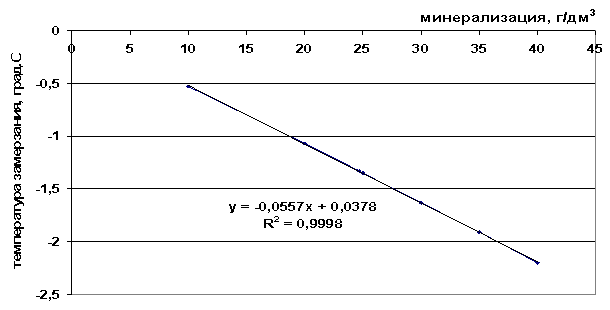
Пиринач. 41. Зависност тачке смрзавања од салинитета раствора соли
Пиринач. 42. Зависност тачке смрзавања морске воде од салинитета
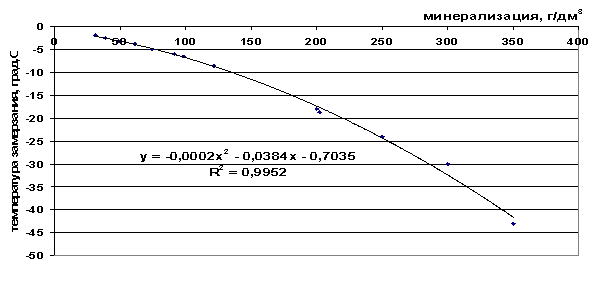
Пиринач. 43. Зависност тачке смрзавања слане воде од салинитета
Из приказаних вредности тачке смрзавања (Табела 9) може се видети да се тачка смрзавања смањује са повећањем укупног салинитета раствора и са повећањем броја компоненти укључених у замрзнути систем - ΔТз(НаЦл)
Табела 9. Анализа конструисаних графичких зависности
|
Цтот, г/дм 3 |
Тачка смрзавања, °С |
||
|
раствор НаЦл |
морска вода |
||
|
т=8∙10 -5 М 2 -0,0945М+1,0595, |
0,0557М+0,0378, |
т=-2∙10 -4 М 2 -0,0384М-0,7035, |
|
*
Р 2 - поузданост апроксимације
Познато је да се смрзавање појединачних соли из десалинизоване воде дешава на различитим температурама, на пример, на температури од -2°Ц, калцијум карбонат се таложи. На - 3,5 ° Ц натријум сулфат. Када температура падне на -20 ° Ц, кухињска со преципитира, на -25,5-26 ° Ц магнезијум хлориди, а на веома ниским температурама - 40-55 ° Ц, таложе се калијум и калцијум хлориди. За негативне температуре специфичан је процес формирања кристалних хидрата, који су нестабилни на температурама испод 0°Ц. На пример, хидрохалит НаЦл * 2Х 2 О се формира на -0,15 ° Ц, МгЦл 2 * 12Х 2 О је стабилан на -15 ° Ц, а МгЦл 2 * 8Х 2 О је испод 0 ° Ц, На 2 ЦО 3 * 7Х 2 О се формира само на -10°Ц. КЦл кристалише на 0°С у облику КЦл, на -6,6°С већ коегзистирају две фазе - КЦл и КЦл*Х 2 О, на -10,6°С преципитира само КЦл*Х 2 О. На негативним температурама појединачни кристални хидрати са максималним могућим бројем молекула кристализационе воде, према координационим бројевима на датој вредности, и њихових смеша (али не и мешаних кристала). Треба приметити аномално смањење тачке смрзавања концентрованих раствора.
Представљамо Вам часописе које издаје издавачка кућа „Академија природне историје“
На којој температури се вода смрзава? Чини се - најједноставније питање на које чак и дете може одговорити: тачка смрзавања воде при нормалном атмосферском притиску од 760 ммХг је нула степени Целзијуса.
Међутим, вода (упркос њеној изузетно широкој распрострањености на нашој планети) је најмистериознија и недовољно схваћена супстанца, па одговор на ово питање захтева детаљну и образложену расправу.
- У Русији и Европи температура се мери на Целзијусовој скали, чија је највиша вредност 100 степени.
- Амерички научник Фаренхајт развио је сопствену скалу са 180 подела.
- Постоји још једна јединица мерења температуре - келвин, названа по енглеском физичару Томсону, који је добио титулу лорда Келвина.
Зашто не треба пити морску воду
Већ смо се укратко дотакли ове теме, погледајмо је мало детаљније. Заједно са морском водом, два јона улазе у тело - магнезијум и натријум.
|
натријум |
Магнезијум |
|
Учествује у одржавању равнотеже воде и соли, једног од главних јона заједно са калијумом. |
Главни ефекат је на централни нервни систем. |
|
Са повећањем броја На |
Веома споро се излучује из тела. |
|
Сви биолошки и биохемијски процеси су поремећени. |
Вишак у телу доводи до дијареје, што погоршава дехидрацију. |
|
Људски бубрези нису у стању да се изборе са толико соли у телу. |
Можда развој нервних поремећаја, неадекватно стање. |
Не може се рећи да човеку нису потребне све ове супстанце, већ да се потребе увек уклапају у одређене границе. Након што попијете неколико литара такве воде, отићи ћете предалеко преко њихових граница.
Међутим, данас се хитна потреба за коришћењем морске воде може јавити само међу жртвама бродолома.