ما الذي يحدد ملوحة مياه البحر
رؤية شخصية أعلى قليلاً 3.5 جزء في المليون
، قد تعتقد أن هذا ثابت لأي مياه بحر على كوكبنا. لكن كل شيء ليس بهذه البساطة ، فالملوحة تعتمد على المنطقة. لقد حدث فقط أنه كلما ابتعدت المنطقة عن الشمال ، زادت هذه القيمة.
الجنوب ، على العكس من ذلك ، يفتخر بعدم وجود بحار ومحيطات مالحة. بالطبع ، كل القواعد لها استثناءات خاصة بها. عادة ما تكون مستويات الملح في البحار أقل قليلاً منها في المحيطات.
ما هو التقسيم الجغرافي بشكل عام؟ إنه غير معروف ، والباحثون يعتبرونه أمرًا مفروغًا منه ، فهناك كل شيء. ربما يجب البحث عن الإجابة في الفترات السابقة لتطور كوكبنا. ليس في الوقت الذي ولدت فيه الحياة - قبل ذلك بكثير.
نعلم بالفعل أن ملوحة الماء تعتمد على وجود:
- كلوريد الماغنيسيوم.
- كلوريد الصوديوم.
- أملاح أخرى.
ربما ، في بعض أجزاء قشرة الأرض ، كانت رواسب هذه المواد أكبر إلى حد ما مما كانت عليه في المناطق المجاورة. من ناحية أخرى ، لم يلغ أحد التيارات البحرية ، عاجلاً أم آجلاً ، كان على المستوى العام أن يستقر.
لذلك ، على الأرجح ، يرتبط اختلاف بسيط بالسمات المناخية لكوكبنا. ليس هذا الرأي الذي لا أساس له من الصحة ، إذا كنت تتذكر الصقيع وتفكر في ما هو بالضبط الماء الذي يحتوي على نسبة عالية من الملح يتجمد بشكل أبطأ.
مراحل التجميد
من المثير للاهتمام مشاهدة كيف تتجمد مياه البحر. لا يتم تغطيتها على الفور بقشرة جليدية موحدة ، مثل المياه العذبة. عندما يتحول جزء منه إلى جليد (وهو طازج) ، يصبح باقي الحجم أكثر ملوحة ، ويلزم تجميده بقوة أكبر.
أنواع الجليد
عندما يبرد البحر ، تتشكل أنواع مختلفة من الجليد:
- عاصفة ثلجية
- الحمأة الناتجة؛
- الإبر.
- سالو.
- نيلاس.
إذا لم يتجمد البحر بعد ، ولكنه قريب جدًا منه ، وفي ذلك الوقت يتساقط الثلج ، فإنه لا يذوب عندما يتلامس مع السطح ، ولكنه مشبع بالماء ويشكل كتلة طرية لزجة تسمى الثلج. عند التجميد ، تتحول هذه العصيدة إلى حمأة ، وهو أمر خطير للغاية بالنسبة للسفن التي تتعرض للعاصفة. وبسبب ذلك ، فإن السطح مغطى على الفور بقشرة جليدية.
عندما يصل مقياس الحرارة إلى العلامة اللازمة للتجميد ، تبدأ إبر الجليد في التكون في البحر - بلورات على شكل موشورات سداسية رفيعة للغاية. عند جمعها بشبكة ، وغسل الملح وتذويبها ، ستجد أنها شاذة.
عندما يصبح الجو أكثر برودة ، يبدأ الدهن في التجمد ويشكل قشرة جليدية شفافة وهشة مثل الزجاج. يسمى هذا الجليد nilas أو الزجاجة. إنه مالح ، على الرغم من أنه يتكون من إبر فطيرة. الحقيقة هي أنه أثناء التجميد ، تلتقط الإبر أصغر قطرات من المياه المالحة المحيطة.
فقط في البحار توجد ظاهرة مثل الجليد العائم. ينشأ لأن الماء هنا يبرد بشكل أسرع قبالة الساحل. يتجمد الجليد المتكون هناك إلى الحافة الساحلية ، ولهذا سمي بالجليد السريع. مع اشتداد الصقيع أثناء الطقس الهادئ ، فإنه يلتقط بسرعة مناطق جديدة ، يصل عرضها أحيانًا إلى عشرات الكيلومترات. ولكن بمجرد أن تهب رياح قوية ، يبدأ الجليد السريع في التفتت إلى قطع بأحجام مختلفة. هذه الطوافات الجليدية ، غالبًا ما تكون ضخمة (حقول جليدية) ، تحملها الرياح والتيارات في جميع أنحاء البحر ، مما يتسبب في مشاكل للسفن.
تحلية مياه البحر.
فيما يتعلق بتحلية المياه ، سمع الجميع على الأقل القليل ، حتى أن البعض الآن يتذكر فيلم "عالم المياه". ما مدى واقعية وضع جهاز تقطير محمول في كل منزل ونسيان مشكلة شرب الماء للبشرية إلى الأبد؟ لا يزال خيالًا وليس واقعًا.
الأمر كله يتعلق بالطاقة المستهلكة ، لأنه من أجل التشغيل الفعال ، هناك حاجة إلى قدرات هائلة ، لا تقل عن مفاعل نووي. تعمل محطة تحلية المياه في كازاخستان على هذا المبدأ.تم تقديم الفكرة أيضًا في شبه جزيرة القرم ، لكن قوة مفاعل سيفاستوبول لم تكن كافية لمثل هذه الأحجام.
قبل نصف قرن ، قبل وقوع العديد من الكوارث النووية ، لا يزال بإمكان المرء أن يفترض أن ذرة سلمية ستدخل كل منزل. حتى أنه كان هناك شعار. لكن من الواضح بالفعل عدم استخدام المفاعلات الدقيقة النووية:
- في الأجهزة المنزلية.
- في المؤسسات الصناعية.
- في صناعة السيارات والطائرات.
- ونعم ، ضمن حدود المدينة.
لم يكن متوقعا في القرن المقبل. قد يأخذ العلم قفزة أخرى ويفاجئنا ، لكن حتى الآن هذه مجرد تخيلات وآمال الرومانسيين المهملين.
نقطة تجمد الماء المقطر
هل الماء المقطر يتجمد؟ تذكر أنه لكي يتجمد الماء ، من الضروري وجود بعض مراكز التبلور فيه ، والتي يمكن أن تكون فقاعات هواء ، وجزيئات معلقة ، بالإضافة إلى تلف جدران الحاوية التي توجد بها.
الماء المقطر ، الخالي تمامًا من أي شوائب ، لا يحتوي على نوى تبلور ، وبالتالي يبدأ تجميده في درجات حرارة منخفضة جدًا. نقطة التجمد الأولية للماء المقطر هي -42 درجة. تمكن العلماء من تحقيق التبريد الفائق للمياه المقطرة إلى -70 درجة.
يُطلق على المياه التي تعرضت لدرجات حرارة منخفضة جدًا ولكنها لم تتبلور "التبريد الفائق". يمكنك وضع زجاجة من الماء المقطر في الفريزر ، وتحقيق انخفاض في درجة حرارة الجسم ، ثم إظهار خدعة فعالة للغاية - شاهد الفيديو:
من خلال النقر بلطف على زجاجة مأخوذة من الثلاجة ، أو عن طريق رمي قطعة صغيرة من الثلج فيها ، يمكنك إظهار كيف يتحول على الفور إلى جليد ، والذي يشبه البلورات الطويلة.
الماء المقطر: هل هذه المادة النقية تتجمد أم لا تحت الضغط؟ هذه العملية ممكنة فقط في ظروف معملية تم إنشاؤها خصيصًا.
ÑÐ ° ÑÑоР»ÑемпеÑÐ ° ÑÑÐ °
لا شيء - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δÐ Ð Ð Ð δÐ Ð Ð Ð Ð Ð δÐ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δ δ ° نثررر. . لا شيء ññ . »Ðððð ²Ðððð ооо²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² ²Ð Ð Ð ² رد »Ð¸ ÑоÐ'ÐμÑжР° ниÐμ Ñол и в ÑÐ ° ÑоР»Ðμ μнÑÑÐμ، ÑÐμм ÑÐμÐ ± ÑÐμмоÐμ Ð'л Ñ ÑвÑÐμкÑиÑÐμкого ° RÐÑ ± ÑÐ ° Ð · овР° ние ÑиÑÑÐ ° Ð »Ð» ² Ð »ÑдР° Ñи Ñл Ð ° ÑÐ ° ѸР»Ð´Ð ° пÑÐ ¸ ÑÐ »Ð ° ÑÑÐ ° иоиии تشغيل ñðμμðððμð½ððÐμÐμРРо РРРРРРРРРРРРРРРРРРРРРРРРРиР¸ ¸ ¸ ¸ иР¸ ¸ ¸ ¸ иР¸ ¸ ¸ ¸ ÐµÑ ÑÑÑÐ ° ÑÐ¸Ñ Ñ ÑÑÐ ° Ð »Ñном ÑÑÐ ° ÑÐ¸Ñ Ñои ÑÑÐ ° л Ñном ÑÑÐ ° ÑÐ¸Ñ Ñ ÑÑÐ ° Ð »Ñном ÑÑÐ ° ÑÐ¸Ñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ñ ñ ñ ñ ñ ° Ð ° ñ °
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ñ ñ ñ ñ ñ ñ ° ñ ° ° С ÐÐ'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð μ μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð μñ ÐÐ ° мÐμÑÐ · Ð ° ниÐμ ÑвÑÐμкÑиÑÐμÑкого ÑÐ ° ÑвоÑÐ ° â Ñо ÑоÑÐμÑÑ Ñ ÑÐ ° ÑиÐμм ÑкÑÑ ÑÐμпР»Ñ ° ° ÑÑ μμ менной. لا شيء . Ð Ð · ñ ñ ñ ñ Ð Ð Ð Ð Ð Ð Ð Ð ² ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ñÐ Ð ° Ð ° Ð Ð Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ¸ سررآرتسÐÐ ° Ñй ÑоÑμÑÑ ÑμнÑμÑÑÑ Ð² пР»Ð ° ÑинÑÐ ° ÑÑ Ð¸ÑпР° ÑиÑμл Ñ Ñи Ñ ° ÑпоÑÑиRовкÐμ пÑ'RR² .
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð ° Ð ° Ð Ð ° Ð ° Ð ° кР° Ð »ÑÐ ¸Ñ Ð ÑÐ »ÑидР° нР° ÑиÑ. Ð Ð ° ÑÐ²Ð¾Ñ ÑÐ »ÑиÐ'Ð ° кР° л ÑÐ¸Ñ ÑμжÐ'Ðμ вÑμго ÑпоР»ÑÐ • ÑÐμÑÑ Ð² ÑомÑÑл μннÑÑ ÑоÑÐÑRR ° ¸ Ð · Ð ° ÑÐ ° живР° нии ÑодÑкÑов، ÑÐ ° нении и Ñ.д. 17.8 درجة С. Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 درجة مئوية . Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð · . ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ° ° ° ° ° ° ° ° ° °¼¹¹ññññ Ðð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ñ ° ÐºÑ ÑÐ ° ÑооР° ÑоÑÐ »Ð ° ждР° емÑм ÑодÑкÑом.
Ð Ð ° ÑÐ²Ð¾Ñ ÑÐ »ÑиÐ'Ð ° нР° ÑÐ¸Ñ (Ñμвой Ñол) нÐμ ÑÑ ÑÐμвÑÐμ пÑоÐ'ÑкÑÑ. لا شيء Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² иРرص »Ñно в21. 1 درجة С. . Ð Ð ·
دورة الماء في المحيط العالمي
في المناطق القطبية ، يصبح الماء ، الذي يبرد ، أكثر كثافة ويغرق في القاع. ومن هناك ينزلق ببطء نحو خط الاستواء. لذلك ، في جميع خطوط العرض ، تكون المياه العميقة باردة. حتى عند خط الاستواء ، تكون درجة حرارة المياه السفلية 1-2 درجة فوق الصفر فقط.
نظرًا لأن التيارات تحمل الماء الدافئ من خط الاستواء إلى خطوط العرض المعتدلة ، فإن الماء البارد يرتفع ببطء شديد من الأعماق ليحل محله. على السطح ، يسخن مرة أخرى ، ويذهب إلى المناطق تحت القطبية ، حيث يبرد ، ويغرق إلى القاع ، ويتحرك مرة أخرى على طول القاع إلى خط الاستواء.
وهكذا ، يوجد في المحيطات نوع من دورة المياه: على السطح ، ينتقل الماء من خط الاستواء إلى المناطق تحت القطبية وعلى طول قاع المحيطات - من المناطق القطبية الفرعية إلى خط الاستواء. عملية خلط الماء هذه ، إلى جانب الظواهر الأخرى المذكورة أعلاه ، تخلق وحدة المحيطات.
إذا وجدت خطأً ، فيرجى تحديد جزء من النص والنقر السيطرة + أدخل
.
في القسم الخاص بمسألة ما الذي يمكن تحقيقه أدنى درجة حرارة لمحلول ملح الماء من ملح الطعام العادي (الطاولة ، NaCl) ، الذي قدمه المؤلف الأوروبي
أفضل إجابة هي بإضافة الملح إلى الماء ، يزيد معدل ذوبان الجليد وتنخفض درجة حرارة انصهار الجليد. وذلك لأن إضافة الملح يؤدي إلى إضعاف التماسك الجزيئي وتدمير الشبكات البلورية للجليد. يتواصل ذوبان خليط الملح والثلج مع إزالة الحرارة من البيئة ، ونتيجة لذلك يبرد الهواء المحيط وتنخفض درجة حرارته. مع زيادة محتوى الملح في خليط الجليد والملح ، تقل درجة انصهاره. يسمى محلول الملح مع أدنى نقطة انصهار سهل الانصهار ، وتسمى درجة حرارة انصهاره نقطة كريوهيدرات. نقطة كريوهيدرات لمزيج ملح الجليد مع ملح الطعام هي -21.2 درجة مئوية ، مع تركيز ملح في المحلول 23.1٪ نسبة إلى الكتلة الكلية للخليط ، والتي تساوي تقريبًا 30 كجم من الملح لكل 100 كجم من جليد.مع زيادة أخرى في تركيز الملح ، لا يعني ذلك انخفاض درجة حرارة انصهار خليط الملح والثلج ، بل زيادة في درجة حرارة الانصهار (عند تركيز الملح بنسبة 25٪ في المحلول إلى الكتلة الكلية ، ترتفع درجة حرارة الانصهار إلى -8 درجة مئوية). عند تجميد محلول مائي من ملح الطعام بتركيز يقابل نقطة كريوهيدرات ، يتم الحصول على خليط متجانس من بلورات الثلج والملح ، والذي يسمى محلول صلب سهل الانصهار. نقطة انصهار محلول صلب سهل الانصهار من كلوريد الصوديوم -21.2 درجة مئوية ، وحرارة الانصهار 236 كيلوجول / كجم. يستخدم المحلول سهل الانصهار للتبريد بعزم دوران صفري. للقيام بذلك ، يتم سكب محلول سهل الانصهار من ملح الطعام في أصفار - أشكال محكمة الإغلاق - ويتم تجميدها. تستخدم الأصفار المجمدة لتبريد العدادات والخزائن وأكياس التبريد المحمولة المبردة وما إلى ذلك (افتح ثلاجة الثلاجة المنزلية - ستجد مثل هذه الحاوية). مع تبريد الجهاز.
إجابة من تجف
أدنى درجة حرارة لأي درجة حرارة هي الصفر المطلق ، حوالي -273 درجة مئوية
إجابة من عليا
تعتمد درجة الحرارة على تركيز الملح في المحلول ، فكلما زاد التركيز ، انخفضت نقطة التجمد. تم أخذ الكتاب المرجعي مني لفترة من الوقت)) ولكن إذا انطلقنا من حقيقة أن مياه البحر هي محلول ملحي ، فيمكننا أن نستنتج أن درجة حرارة التجمد أقل بكثير من الصفر .... درجة -15-20
إجابة من قادر
يتجمد محلول مائي 22.4٪ كلوريد الصوديوم عند 21.2 درجة مئوية
محلول مائي من كلوريد الصوديوم "درجة حرارة التبلور"
إجابة من يرغي نيزناموف
الجدول 10.8. نقطة تجمد محلول كلوريد الصوديوم محتوى NaCl ، غرام في 100 غرام من الماء 5 - -4.4 9.0 - -5.4 10.6 - -6.4 12.3 - -7.5 14.0 - -8.6 15.7 - -9.8 17.5 - -11.0 19.3 - - 12.2 21.2 - -13.6 23.1 - - 15.1 25.0 - - 16.0 26.9 - -18.2 29.0 - -20 .0 30.1 - -21.2
نقطة تجمد الماء المالح
دائمًا ما تكون تجارب استخدام الثلج للأطفال ممتعة. أثناء إجراء التجارب مع فلاد ، قمت بالعديد من الاكتشافات بنفسي.
سنجد اليوم إجابات على الأسئلة التالية:
- كيف يتصرف الماء عند التجميد؟
- ماذا يحدث إذا جمدت الماء المالح؟
- معطف دافئ الجليد؟
- والبعض الآخر ...
مياه متجمدة

هل يتجمد الماء المالح؟
كلما زادت ملوحة الماء ، انخفضت درجة التجمد. للتجربة ، أخذنا كأسين - في أحدهما ماء عذب (مميز بالحرف B) ، والآخر ماء شديد الملوحة (مميز بالحرفين B + C).
بعد الوقوف في الثلاجة طوال الليل ، لم يتجمد الماء المالح ، ولكن تشكلت بلورات الجليد في الزجاج. تحولت المياه العذبة إلى جليد. بينما كنت أتلاعب بالأكواب ومحاليل الملح ، ابتكر فلاديك تجربته غير المخطط لها.
قام بصب الماء والزيت النباتي في كوب ووضعه في الفريزر بتكتم. 
الماء المالح في الفريزر لم يتجمد ولكن ماذا يحدث لو رش الملح على الثلج؟ دعونا تحقق.
خبرة في استخدام الثلج والملح
خذ مكعبين من الثلج. يرش أحدهم بالملح ، ويترك الثاني للمقارنة. 
جمدنا جليدًا كبيرًا ورشناه بالملح وأخذنا الفرشاة و 
إن إبداعنا الخبير يوحد جميع أفراد الأسرة ، لذلك دخل قلم ماكاروشكين في عدسة الكاميرا!
ماكار وفلاد جدا الجميع يحب التجميد
. في بعض الأحيان توجد عناصر غير متوقعة تمامًا في الفريزر.
حلمت بالقيام بهذه التجربة منذ الطفولة ، لكن والدتي لم يكن لديها معطف فرو ، والكثير

كم هو رائع أن تكون شخصًا بالغًا وأن ترتدي معطفًا من الفرو وتقوم بكل أنواع تجارب الأطفال!
غالينا كوزمينا الخاص بك
يوضح الجدول الخصائص الفيزيائية الحرارية لمحلول كلوريد الكالسيوم CaCl 2 اعتمادًا على درجة الحرارة وتركيز الملح: الحرارة النوعية للمحلول ، والتوصيل الحراري ، ولزوجة المحاليل المائية ، وانتشارها الحراري ، ورقم برانتل. يتراوح تركيز الملح CaCl 2 في المحلول من 9.4 إلى 29.9٪. يتم تحديد درجة الحرارة التي يتم عندها تحديد الخصائص من خلال محتوى الملح في المحلول وتتراوح من -55 إلى 20 درجة مئوية.
كلوريد الكالسيوم قد لا يتجمد CaCl 2 حتى 55 درجة مئوية تحت الصفر
. ولتحقيق هذا التأثير يجب أن يكون تركيز الملح في المحلول 29.9٪ وكثافته 1286 كجم / م 3.
مع زيادة تركيز الملح في المحلول ، لا تزداد كثافته فحسب ، بل تزداد أيضًا الخصائص الفيزيائية الحرارية مثل اللزوجة الديناميكية والحركية للمحاليل المائية ، بالإضافة إلى رقم برانتل. على سبيل المثال، اللزوجة الديناميكية لمحلول CaCl 2
بتركيز ملح 9.4٪ عند درجة حرارة 20 درجة مئوية هو 0.001236 باسكال ث ، ومع زيادة تركيز كلوريد الكالسيوم في المحلول إلى 30٪ ، تزداد لزوجته الديناميكية إلى 0.003511 باسكال ث.
وتجدر الإشارة إلى أن درجة الحرارة لها التأثير الأقوى على لزوجة المحاليل المائية لهذا الملح. عندما يتم تبريد محلول كلوريد الكالسيوم من 20 إلى -55 درجة مئوية ، يمكن أن تزيد لزوجته الديناميكية بمقدار 18 مرة ، ويمكن أن تزيد حركته بمقدار 25 مرة.
بالنظر إلى ما يلي الخصائص الفيزيائية الحرارية لمحلول CaCl 2
:
- ، كجم / م 3 ؛
- نقطة التجمد ° С ؛
- اللزوجة الديناميكية للمحاليل المائية ، Pa · s ؛
- رقم براندتل.
ÑÐ ° ÑÑоР»ÑемпеÑÐ ° ÑÑÐ °
لا شيء - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δÐ Ð Ð Ð δÐ Ð Ð Ð Ð Ð δÐ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δ δ ° نثررر. . لا شيء ññ . »Ðððð ²Ðððð ооо²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² ²Ð Ð Ð ² رد »Ð¸ ÑоÐ'ÐμÑжР° ниÐμ Ñол и в ÑÐ ° ÑоР»Ðμ μнÑÑÐμ، ÑÐμм ÑÐμÐ ± ÑÐμмоÐμ Ð'л Ñ ÑвÑÐμкÑиÑÐμкого ° RÐÑ ± ÑÐ ° Ð · овР° ние ÑиÑÑÐ ° Ð »Ð» ² Ð »ÑдР° Ñи Ñл Ð ° ÑÐ ° ѸР»Ð´Ð ° пÑÐ ¸ ÑÐ »Ð ° ÑÑÐ ° иоиии تشغيل ñðμμðððμð½ððÐμÐμРРо РРРРРРРРРРРРРРРРРРРРРРРРРиР¸ ¸ ¸ ¸ иР¸ ¸ ¸ ¸ иР¸ ¸ ¸ ¸ ÐµÑ ÑÑÑÐ ° ÑÐ¸Ñ Ñ ÑÑÐ ° Ð »Ñном ÑÑÐ ° ÑÐ¸Ñ Ñои ÑÑÐ ° л Ñном ÑÑÐ ° ÑÐ¸Ñ Ñ ÑÑÐ ° Ð »Ñном ÑÑÐ ° ÑиÑÐ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ñ ñ ñ ñ ñ ° Ð ° ñ °
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ñ ñ ñ ñ ñ ñ ° ñ ° ° С ÐÐ'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð μ μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð μñ ÐÐ ° мÐμÑÐ · Ð ° ниÐμ ÑвÑÐμкÑиÑÐμÑкого ÑÐ ° ÑвоÑÐ ° â Ñо ÑоÑÐμÑÑ Ñ ÑÐ ° ÑиÐμм ÑкÑÑ ÑÐμпР»Ñ ° ° ÑÑ μμ менной. لا شيء . Ð Ð · ñ ñ ñ ñ Ð Ð Ð Ð Ð Ð Ð Ð ² ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ñÐ Ð ° Ð ° Ð Ð Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ¸ سررآرتس ÐÐ ° Ñй ÑоÑμÑÑ ÑμнÑμÑÑÑ Ð² пР»Ð ° ÑинÑÐ ° ÑÑ Ð¸ÑпР° ÑиÑμл Ñ Ñи Ñ ° ÑпоÑÑиRовкÐμ пÑ'RR² .
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð ° Ð ° Ð Ð ° Ð ° Ð ° кР° Ð »ÑÐ ¸Ñ Ð ÑÐ »ÑидР° нР° ÑиÑ. Ð Ð ° ÑÐ²Ð¾Ñ ÑÐ »ÑиÐ'Ð ° кР° л ÑÐ¸Ñ ÑμжÐ'Ðμ вÑμго ÑпоР»ÑÐ • ÑÐμÑÑ Ð² ÑомÑÑл μннÑÑ ÑоÑÐÑRR ° ¸ Ð · Ð ° ÑÐ ° живР° нии ÑодÑкÑов، ÑÐ ° нении и Ñ.д. 17.8 درجة С. Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 درجة مئوية . Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð · . ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ° ° ° ° ° ° ° ° ° °¼¹¹ññññ Ðð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ñ ° ÐºÑ ÑÐ ° ÑооР° ÑоÑÐ »Ð ° ждР° емÑм ÑодÑкÑом.
Ð Ð ° ÑÐ²Ð¾Ñ ÑÐ »ÑиÐ'Ð ° нР° ÑÐ¸Ñ (Ñμвой Ñол) нÐμ ÑÑ ÑÐμвÑÐμ пÑоÐ'ÑкÑÑ. لا شيء Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² иРرص »Ñно в21. 1 درجة С. . Ð Ð ·
في أي درجة حرارة يمكن أن يتجمد ماء البحر؟
لكن السؤال الرئيسي لم تتم الإجابة عليه بعد. لقد تعلمنا بالفعل أن الملح يبطئ من تجمد الماء ، وسوف يتم تغطية البحر بقشرة من الجليد ليس عند الصفر ، ولكن عند درجات حرارة أقل من الصفر. ولكن إلى أي مدى يجب أن تصل قراءات مقياس الحرارة إلى سالب حتى لا يسمع سكان المناطق الساحلية الصوت المعتاد لركوب الأمواج عندما يغادرون منازلهم؟
لتحديد هذه القيمة ، هناك صيغة خاصة معقدة ومفهومة فقط للمتخصصين. ذلك يعتمد على المؤشر الرئيسي - مستوى الملوحة
. ولكن بما أن لدينا متوسط قيمة لهذا المؤشر ، فهل يمكننا أيضًا إيجاد متوسط نقطة التجمد؟ بالطبع.
إذا كنت لا تحتاج إلى حساب كل شيء حتى مائة ، لمنطقة معينة ، تذكر درجة الحرارة عند -1.91 درجة
.
قد يبدو أن الاختلاف ليس كبيرًا ، فقط درجتان. ولكن أثناء التقلبات الموسمية في درجات الحرارة ، يمكن أن يلعب هذا دورًا كبيرًا حيث ينخفض مقياس الحرارة بمقدار 0 على الأقل. سيكون أكثر برودة بمقدار درجتين فقط ، ويمكن لسكان نفس إفريقيا أو أمريكا الجنوبية رؤية الجليد بالقرب من الساحل ، ولكن للأسف. ومع ذلك ، لا نعتقد أنهم منزعجون جدًا من هذه الخسارة.
الخصائص الفيزيائية الحرارية لمحلول كلوريد الصوديوم
يوضح الجدول الخصائص الفيزيائية الحرارية لمحلول كلوريد الصوديوم كلوريد الصوديوم اعتمادًا على درجة الحرارة وتركيز الملح. يتراوح تركيز كلوريد الصوديوم كلوريد الصوديوم في المحلول من 7 إلى 23.1٪. وتجدر الإشارة إلى أنه عند تبريد محلول مائي من كلوريد الصوديوم ، تتغير سعته الحرارية النوعية قليلاً ، وتقل الموصلية الحرارية ، وتزداد لزوجة المحلول.
بالنظر إلى ما يلي الخصائص الفيزيائية الحرارية لمحلول كلوريد الصوديوم
:
- كثافة المحلول ، كجم / م 3 ؛
- نقطة التجمد ° С ؛
- السعة الحرارية النوعية (الكتلة) ، kJ / (kg deg) ؛
- معامل التوصيل الحراري ، W / (م درجة) ؛
- اللزوجة الديناميكية للمحلول ، Pa · s ؛
- اللزوجة الحركية للمحلول ، م 2 / ث ؛
- الانتشار الحراري ، م 2 / ث ؛
- رقم براندتل.
مما تتكون مياه البحر؟
كيف يختلف محتوى البحار عن المياه العذبة؟ الفرق ليس كبيرًا ، لكنه لا يزال:
- المزيد من الملح.
- تسود أملاح المغنيسيوم والصوديوم.
- تختلف الكثافة قليلاً ، في غضون بضعة بالمائة.
- يمكن أن يتكون كبريتيد الهيدروجين في العمق.
المكون الرئيسي لمياه البحر ، بغض النظر عن مدى توقعه ، هو الماء. ولكن على عكس مياه الأنهار والبحيرات ، فهي يحتوي على كميات كبيرة من كلوريد الصوديوم والمغنيسيوم
.
تقدر الملوحة بـ 3.5 جزء في المليون ، ولكن لجعلها أكثر وضوحًا - 3.5 جزء من ألف في المائة من التركيبة الإجمالية.
وحتى هذا ، ليس الشكل الأكثر إثارة للإعجاب ، فهو يوفر الماء ليس فقط بمذاق معين ، ولكنه أيضًا يجعله غير صالح للشرب. لا توجد موانع مطلقة ، فمياه البحر ليست سمًا أو مادة سامة ، ولن يحدث شيء سيئ من رشفتين. سيكون من الممكن التحدث عن العواقب إذا كان الشخص على الأقل طوال اليوم.كما أن تكوين مياه البحر يشمل:
- الفلور.
- البروم.
- الكالسيوم.
- البوتاسيوم.
- الكلور.
- كبريتات.
- ذهب.
صحيح ، من حيث النسبة المئوية ، كل هذه العناصر أقل بكثير من الأملاح.
الدول وأنواع المياه
يمكن أن يأخذ الماء على كوكب الأرض ثلاث حالات رئيسية للتجمع: السائل والصلب والغازي ، والتي يمكن أن تتحول إلى أشكال مختلفة تتعايش في نفس الوقت مع بعضها البعض (الجبال الجليدية في مياه البحر وبخار الماء وبلورات الجليد في السحب في السماء والأنهار الجليدية والحرة. - الانهار المتدفقة).
اعتمادًا على خصائص الأصل والغرض والتكوين ، يمكن أن يكون الماء:
- طازج؛
- المعدنية.
- بحري؛
- الشرب (هنا نقوم بتضمين ماء الصنبور) ؛
- تمطر؛
- إذابة؛
- قليل الملوحة.
- منظم.
- مقطر؛
- منزوع الأيونات.
وجود نظائر الهيدروجين يجعل الماء:
- خفيفة؛
- ثقيل (الديوتيريوم) ؛
- ثقيل (التريتيوم).
نعلم جميعًا أن الماء يمكن أن يكون طريًا وقاسًا: يتم تحديد هذا المؤشر من خلال محتوى كاتيونات المغنيسيوم والكالسيوم.
كل نوع من أنواع المياه وحالاتها الكلية التي قمنا بإدراجها لها نقطة تجمد وانصهار خاصة بها.
تجميد المياه المالحة فيديو

 ماذا تعرف عن درجة غليان الماء؟
ماذا تعرف عن درجة غليان الماء؟

يحدد نظام درجة الحرارة ، أولاً وقبل كل شيء ، معدل عملية التجميد.
تؤثر درجة الحرارة في نطاق القيم الإيجابية والسلبية على معدل التفاعلات ، وقابلية ذوبان المركبات ، ومعدل الانحلال ، والتخثر ، وكذلك تركيز أزواج الأيونات غير المرتبطة. هناك عدة أنواع من درجات الحرارة في المحاليل: هيكلية ، نقطة التجمد. درجة حرارة بدء التبلور (نقطة التجمد) - درجة الحرارة التي يبدأ عندها تكوين البلورات نتيجة تبريد المحلول. انخفاض نقطة التجمد ΔTz هو الفرق بين نقطة التجمد لمذيب نقي ومحلول. تكون نقطة تجمد المحلول الملحي دائمًا أقل من نقطة تجمد الماء النقي وتعتمد على تركيز الأملاح الذائبة. يمكن التعبير عن هذا الاعتماد على المحاليل الملحية بالمعادلة:
أين ل
- معامل التناسب ؛ مع
هو تركيز المذاب في المحلول.
في المحاليل الأقل تمييعًا ، يتم تحديد درجة حرارة بداية التبلور من مخطط الحالة للنظام المقابل. نظرًا لأن درجة حرارة التجمد في مياه البحر والمحاليل الملحية الطبيعية عالية التمعدن ستكون مختلفة ، فإننا نفترض أنه يجب حساب درجة الحرارة هذه باستخدام صيغ مختلفة.
لقد قمنا بعمل تقريب للبيانات التجريبية على نقاط التجمد لمحاليل ملح الطعام ومياه البحر والمحاليل الملحية الطبيعية المستخدمة في العمل. وترد في الأشكال 41-43 تبعيات تغيرات درجة حرارة التجمد في الأشكال الرسومية والتحليلية.
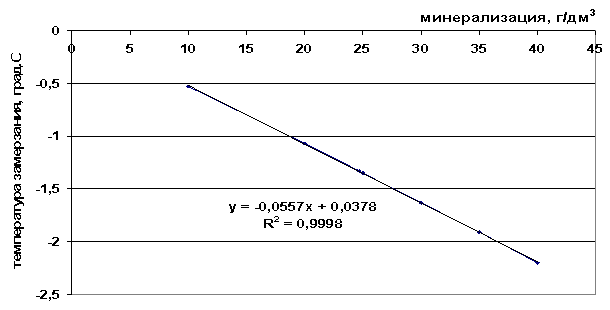
أرز. 41. اعتماد درجة التجمد على ملوحة المحلول الملحي
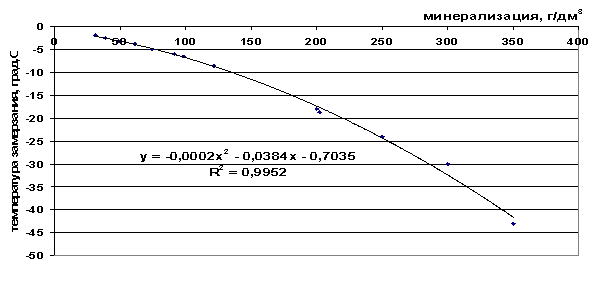
أرز. 42. اعتماد درجة تجمد مياه البحر على الملوحة
أرز. 43. اعتماد درجة تجمد المحلول الملحي على الملوحة
من قيم نقطة التجمد المقدمة (الجدول 9) ، يمكن ملاحظة أن نقطة التجمد تتناقص مع زيادة الملوحة الكلية للمحلول ومع زيادة عدد المكونات المدرجة في النظام المجمد - ΔТз (NaCl)
الجدول 9. تحليل التبعيات الرسومية شيدت
|
Ctot ، جم / دسم 3 |
نقطة التجمد ، درجة مئوية |
||
|
محلول كلوريد الصوديوم |
مياه البحر |
||
|
ر = 8 ∙ 10 -5 م 2 -0.0945 م + 1.0595 ، |
0.0557 م + 0.0378 ، |
ر = -2 ∙ 10 -4 م 2 -0.0384 م -0.7035 ، |
|
*
R 2 - موثوقية التقريب
من المعروف أن تجميد الأملاح الفردية من المياه المحلاة يحدث في درجات حرارة مختلفة ، على سبيل المثال ، عند درجة حرارة -2 درجة مئوية ، تترسب كربونات الكالسيوم. عند - 3.5 درجة مئوية كبريتات الصوديوم. عندما تنخفض درجة الحرارة إلى -20 درجة مئوية ، يترسب ملح الطعام ، إلى -25.5-26 درجة مئوية كلوريدات المغنيسيوم ، وفي درجات حرارة منخفضة جدًا - 40-55 درجة مئوية ، يترسب كلوريد البوتاسيوم والكالسيوم. بالنسبة لدرجات الحرارة السلبية ، تكون عملية تكوين الهيدرات البلورية ، غير المستقرة عند درجات حرارة أقل من 0 درجة مئوية ، عملية محددة. على سبيل المثال ، هيدروهاليت NaCl * 2H 2 O يتشكل عند -0.15 درجة مئوية ، MgCl 2 * 12H 2 O يكون مستقرًا عند -15 درجة مئوية ، و MgCl 2 * 8H 2 O أقل من 0 درجة مئوية ، Na 2 CO 3 * 7H 2 O يتكون فقط عند -10 درجة مئوية. يتبلور بوكل عند 0 درجة مئوية على شكل بوكل ، عند -6.6 درجة مئوية تتعايش مرحلتان بالفعل - KCl و KCl * H 2 O ، عند -10.6 درجة مئوية فقط ، يترسب KCl * H 2 O. في درجات الحرارة السلبية ، هيدرات بلورية فردية مع أكبر عدد ممكن من جزيئات ماء التبلور ، وفقًا لأرقام التنسيق عند قيمة معينة ، ومخاليطها (ولكن ليس البلورات المختلطة). يجب ملاحظة انخفاض غير طبيعي في درجة تجمد المحاليل المركزة.
نلفت انتباهكم إلى المجلات التي تصدرها دار النشر "أكاديمية التاريخ الطبيعي".
في أي درجة حرارة يتجمد الماء؟ يبدو - أبسط سؤال يمكن للطفل أن يجيب عنه: نقطة تجمد الماء عند الضغط الجوي الطبيعي البالغ 760 مم زئبق هي صفر درجة مئوية.
ومع ذلك ، فإن الماء (على الرغم من توزيعه الواسع للغاية على كوكبنا) هو المادة الأكثر غموضًا وغير مفهومة تمامًا ، لذا فإن الإجابة على هذا السؤال تتطلب محادثة مفصلة ومنطقية.
- في روسيا وأوروبا ، تُقاس درجة الحرارة بمقياس سيليزيوس ، وأعلى قيمة له هي 100 درجة.
- طور العالم الأمريكي فهرنهايت مقياسه الخاص المكون من 180 قسمًا.
- هناك وحدة أخرى لقياس درجة الحرارة - كلفن ، سميت على اسم الفيزيائي الإنجليزي طومسون ، الذي حصل على لقب اللورد كلفن.
لماذا لا تشرب ماء البحر
لقد تطرقنا بالفعل إلى هذا الموضوع بإيجاز ، فلنلقِ نظرة عليه بمزيد من التفصيل. إلى جانب مياه البحر ، يدخل الجسم أيونان - المغنيسيوم والصوديوم.
|
صوديوم |
المغنيسيوم |
|
يساهم في الحفاظ على توازن الماء والملح ، وهو أحد الأيونات الرئيسية إلى جانب البوتاسيوم. |
التأثير الرئيسي على الجهاز العصبي المركزي. |
|
مع زيادة العدد نا |
تفرز ببطء شديد من الجسم. |
|
جميع العمليات البيولوجية والكيميائية الحيوية مضطربة. |
تؤدي الزيادة في الجسم إلى الإسهال الذي يؤدي إلى تفاقم الجفاف. |
|
لا تستطيع الكلى البشرية التعامل مع الكثير من الملح في الجسم. |
ربما تطور الاضطرابات العصبية ، حالة غير كافية. |
لا يمكن القول أن الشخص لا يحتاج إلى كل هذه المواد ، ولكنه يحتاج دائمًا إلى حدود معينة. بعد شرب بضعة لترات من هذه المياه ، سوف تتجاوز حدودها.
ومع ذلك ، فإن الحاجة الملحة اليوم لاستخدام مياه البحر قد تنشأ فقط بين ضحايا حطام السفن.