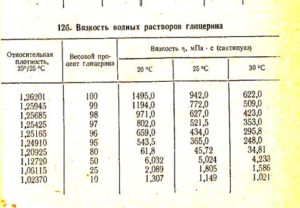
Vandets frysepunkt
Indfrysningsprocessen finder sted når den er kølet ned til nul grader på Celsius-skalaen. Dette gælder ikke alt vand. Molekyler binder sig til urenheder, som er partikler af støv, salt osv. Derfor kan rent eller destilleret vand, uden tilstedeværelsen af netop disse urenheder, under påvirkning af lave temperaturer i Celsius-søjlen, forblive i flydende tilstand længere end almindeligt vand.
Det er også interessant, at mens andre stoffer falder i volumen ved frysning, øges vand tværtimod. Dette skyldes, at afstanden mellem molekylerne udvider sig under overgangen til fast tilstand. På trods af at volumen stiger, stiger massen ikke ved frysning og vejer lige så meget som varmt vand.
Mange undrer sig over, hvorfor vand ikke fryser under et tykt lag is. Enhver fysiker vil svare, at under et islag fryser vand ikke, da isens overflade fungerer som en varmeisolator.

Hvorfor fryser varmt vand hurtigere end koldt vand?
Det er kendt, at varmt eller varmt vand fryser hurtigere end koldt vand. Utroligt men sandt. Denne opdagelse blev gjort af Erasto Mpemba. Han udførte forsøg med den frosne masse, og fandt ud af, at hvis massen er varm, så fryser den hurtigere. Årsagen til dette, som undersøgelser har vist, er den høje varmeoverførsel af varmt og varmt vand.

Er frysepunktet for vand og højde relateret?
Som bekendt ændres trykket i højden, så temperaturen ved overgangen til fast tilstand af alle vandige opløsninger i højden adskiller sig fra temperaturen på en normal overflade.
Eksempler på temperaturændringer i højden:
- højde 500 m - vandets frysepunkt er ikke nul ° C, som under normale forhold, men i nærværelse af allerede en ° C;
- højde 1500 m - krystallisation sker i nærværelse af omkring tre ° C osv.

Hvordan tryk påvirker processen med vandkrystallisation
Hvis du forstår forholdet mellem tryk og krystallisation af vand, så er alt ret simpelt.
Interessant! Jo højere tryk, jo lavere omdannelseshastighed af vand til iskrystaller, og jo højere kogepunkt!
Det er hele hemmeligheden, og hvis du tænker logisk, så går alle indikatorer med et fald i trykket i den modsatte retning. Derfor er det svært at tilberede noget i bjergene, da temperaturen, ved hvilken vandet koger, ikke når hundrede grader Celsius. Omvendt smelter is selv ved lave temperaturer.
Krystallisationstemperatur af vandige opløsninger
Vand er et godt opløsningsmiddel og kan derfor nemt kombineres med andre stoffer. De resulterende opløsninger vil selvfølgelig fryse under forskellige forhold. Overvej et par muligheder for temperaturkriterier for frysning af forskellige løsninger baseret på vand.
Vand og alkohol. Med en stor mængde alkohol i vandet vil frysningsprocessen begynde ved tilstedeværelse af meget lave temperaturer. For eksempel, ved et forhold på 60% vand til 40% alkohol, vil krystallisation begynde i nærværelse af minus 22,5 ° C.
Vand og salt. Temperaturen, hvor der opstår frysning, er direkte relateret til vandets saltholdighedsgrad. Princippet er, at jo mere salt der er i vandet, jo lavere er krystallisationstemperaturen. Hvordan havvand fryser er direkte relateret til saltindholdet.
Vand og sodavand. Opløsningens krystallisationstemperatur er 44 procent plus 7°C.
Vand og glycerin, i et forhold på 80% til 20%, hvor 80 er glycerin, og 20 er vand, er tilstedeværelsen af -20 ° C påkrævet for at fryse opløsningen.
Alle temperaturværdier svinger afhængigt af graden af koncentration af fremmede opløsninger eller andre stoffer i vandet.
Måling af væskers viskositet med et Ostwald-viskosimeter
For at bestemme viskositetskoefficienten ηhis af den undersøgte væske ved hjælp af et Ostwald kapillærviskosimeter (fig. 6), er det nødvendigt at vide:
- η0 er viskositeten af vand,
- t0 er tiden for vandstrømmen mellem mærkerne a og b,
- tx er strømningstidspunktet for den undersøgte væske mellem mærkerne a og b,
- ρ0 er densiteten af vand,
- ρx er densiteten af den undersøgte væske.
Ris. 6. Ostwald kapillær viskosimeter (a, b, d - mærker, der begrænser væskeniveauet, c - kapillær).
Viskositeten af den undersøgte væske bestemmes af formlen (9).
Arbejdsordre
Opgave 1. Bestem viskositeten af opløsninger med forskellige koncentrationer.
-
Hæld vand i benet på viskosimeteret, der ikke har kapillar (fig. 6) op til mærket d.
-
Med en pære suges væsken gennem kapillæren for at markere en. Efter at have fjernet pæren lukkes hullet i venstre knæ på viskosimeteret (med en hånd, en prop, en vatpind osv.) (se fig. 6). Forbered og tænd stopuret, åbn hullet i venstre knæ, og sluk det, når mærke b flyder, og bestemme t0 - tidspunktet for vandgennemstrømning mellem mærkerne a og b.
-
Gentag målingerne 4-5 gange, find den gennemsnitlige tid.
-
Udfør trin 1-3 for alle testvæsker.
-
Beregn viskositetskoefficienterne for de undersøgte væsker ved hjælp af formel (9).
-
Indtast data i tabel 1.
tabel 1
| № | Koncentration, % | t1 | t2 | t3 | t4 | t5 | | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 | ||||||||
| 5 | ||||||||
| 6 |
Opgave 2. Bestem koncentrationen af en ukendt opløsning.
-
Plot viskositetsforhold vs opløsningskoncentration
-
Ved at kende viskositeten af den ukendte opløsning, bestemme dens koncentration fra grafen.
Tabel 2
Densitet af vand ved forskellige temperaturer
| ρ, kg/m3 | t, 0C | ρ, kg/m3 | t, 0C |
| 999,13 | 15 | 998,02 | 21 |
| 998,97 | 16 | 997,80 | 22 |
| 998,80 | 17 | 997,57 | 23 |
| 998,43 | 19 | 997,32 | 24 |
| 998,23 | 20 | 997,07 | 25 |
Tabel 3
Viskositet af vand ved forskellige temperaturer
| η, Pa.s | t, 0C | η, Pa.s | t, 0C |
| 0,00114 | 15 | 0,00098 | 21 |
| 0,00111 | 16 | 0,00096 | 22 |
| 0,00108 | 17 | 0,00093 | 23 |
| 0,00103 | 19 | 0,00091 | 24 |
| 0,00100 | 20 | 0,00089 | 25 |
Tabel 4
Densitet af glycerinopløsninger af forskellige koncentrationer
| MED, % | ρ, kg/m3 | MED, % | ρ, kg/m3 |
| 5 | 1012,5 | 45 | 1112,5 |
| 10 | 1025,0 | 50 | 1125,0 |
| 15 | 1037,5 | 55 | 1137,5 |
| 20 | 1042,5 | 60 | 1150,0 |
| 25 | 1052,5 | 65 | 1162,5 |
| 30 | 1075,0 | 70 | 1175,0 |
| 35 | 1087,5 | 75 | 1187,5 |
| 40 | 1100,0 | 80 | 1200,0 |
Selvstændigt arbejde med emnet:
– løsning af situationsproblemer;
- lytte til abstracts
Endelig kontrol af viden:
– løse problemer med billetter;
– svar på endelige kontrolbilletter;
- opsummerende.
Hjemmearbejde for at forstå lektionens emne
Kontrolspørgsmål om lektionens emne:
1. Hvad kaldes en væskes viskositet?
2. Hvilken slags væskestrøm kaldes laminær?Turbulent?
3. Hvad kendetegner Reynolds formlen?
4. Skriv Newtons formel og forklar den fysiske betydning af de mængder, der indgår i den?
5. Hvad er koefficienten for dynamisk viskositet? I hvilke enheder måles det?
6. Hvilke væsker kaldes newtonsk? Hvad bestemmer deres viskositetskoefficient?
7. Hvilke væsker kaldes ikke-newtonske Hvad bestemmer deres viskositetskoefficient?
8. Skriv Poiseuille-formlen, forklar den fysiske betydning af de mængder, der indgår i den.
9. Hvilke metoder bruges til at bestemme en væskes viskositet?
10. Fortæl om blods og andre biologiske væskers rheologiske egenskaber, om brugen af rheologiske analyser i medicin.
11. Hvad viser hastighedsgradienten? Vis grafisk.
12. Hvilket fænomen kaldes intern friktion?
Testopgaver om emnet:
ER ANVENDELSE AF GLYCERIN TIL OPVARMNING BEMÆRKET?
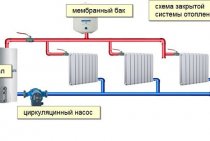
Der stilles ret høje krav til kølevæsken til varmesystemer. Det skal være brand- og eksplosionssikkert, give god termisk ydeevne og heller ikke indeholde tilsætningsstoffer, der er forbudt at bruge. Ethylenglycol eller propylenglycol bruges som grundlag for produktion af højkvalitets varmeoverførselsvæske, som også sikrer miljøvenlighed.
For nylig er glycerin-baserede frostvæsker dukket op på markedet. Dette produkt promoveres hovedsageligt af små, lidet kendte firmaer på frostvæskemarkedet. Spørgsmålet opstår: glycerin og kølevæske - er deres forening passende?
Og faktisk blev de første frostvæsker, der dukkede op i vores land i tyverne af det sidste århundrede, lavet på basis af glycerin. Deres svagheder var utilstrækkelig fluiditet og ekstrem høj viskositet, som pumperne ikke kunne klare. De forsøgte at løse problemet ved hjælp af alkohol, herunder methylalkohol. Men sammen med forbedringen i fluiditeten dukkede mange problemer op. Faktum er, at methanol er en stærk psykotrop gift.Som følge heraf trodsede adfærden hos chauffører, der ufrivilligt snusede sådan frostvæske, nogle gange enhver logik og udgjorde en fare for andres helbred og liv. Derudover har methylalkohol et lavt kogepunkt, og når det fordamper, øges produktets viskositet med det samme. Problemet blev først løst, da ethylenglycol blev grundlaget for kølevæsken. Og i slutningen af 30'erne, begyndelsen af 40'erne, erstattede ethylenglycol frostvæsker næsten fuldstændigt glycerin-methanol.
Derudover er glycerin termisk ustabil, nedbrydes under langvarig opvarmning med dannelsen af et giftigt flygtigt stof - acrolein, som har en skarp ubehagelig lugt, der forårsager rivning. Nedbrydningsprodukter er giftige, og udfældning øger kølevæskens ætsende aktivitet. Som følge heraf er kravene til tætninger og dele fremstillet af ikke-polære gummier og plastik stigende. Udover høj viskositet skummer glycerin også kraftigt, hvilket fører til udluftning af systemet og dårlig varmeafledning.
Producenter af glycerinkølemidler forsøger at kompensere for alle ovennævnte ulemper ved at tilføje forskellige tilsætningsstoffer, herunder alifatiske alkoholer - methanol, ethanol, propanol. Disse alkoholer kan reducere viskositeten eller densiteten af frostvæsken betydeligt. Men de koger allerede ved temperaturer over 65 grader, hvilket fører til en forringelse af kølevæskens termiske ydeevne. Disse alkoholer er i stand til at opløse gummi og polymerer og er også tilbøjelige til kavitation og kraftig fordampning. Derudover er methanol en stærk gift og er forbudt at bruge til fremstilling af frostvæsker.
At sikre kvaliteten af glycerin-kølevæsker, især med methanol, kræver tilsætning af dyre additivpakker til blandingen. Og selvom prisen på glycerin nu er lavere end prisen på glycoler, er additivpakken til fremstilling af kvalitetsglycerin varmeoverførselsvæsker dyrere end additivpakken til frostvæske baseret på ethylenglycol og propylenglycol. Og hvis prisen på glycerin frostvæske på markedet er lavere end for glycol, betyder det, at producenten simpelthen sparede på kvaliteten og ikke tilføjede de nødvendige dyre tilsætningsstoffer til produktet!
Så valget er op til køberen: enten en pålidelig og gennemprøvet kølevæske baseret på glykoler eller en glycerin "gris i en poke".
Valget af vores virksomhed, som de fleste af de førende producenter af frostvæsker, er grundlæggende entydigt - glycerin kan ikke bruges i sin rene form, men blandet med methanol er farligt og kriminelt!
Hovedargumentet, der bekræfter vores holdning til dette spørgsmål, er, at i enhver vigtig og stor facilitet er brugen af glycerin i varme- og kølesystemer IKKE TILLADET af eksisterende standarder!
MEG
Ethylenglycol er et produkt af ethylenoxidhydrering i nærværelse af svovlsyre eller fosforsyre. Henviser til polyvalente alkoholer. Fryser ikke ved lave temperaturer og sænker frysepunktet for vand. I stand til at absorbere vand fra luften.
Den sælges i metal- og plastiktønder, op til 227 liter. Samt plastik terninger 1000l.
Det er nødvendigt at opbevare stoffet i en forseglet beholder lavet af aluminium eller stål med anti-korrosionsbeskyttelse i et lukket lager uden opvarmning. Holdbarheden for den højeste kvalitet er 12 måneder, for den første klasse - 3 år fra produktionsdatoen.
Navn på indikator Norm
Udseende, lugt Klar, farveløs væske med en olieagtig tekstur. Uden lugt.
Opløseligt i vand, alkoholer, toluen, benzen
Massefylde 1,112 g/cm?.
Smeltepunkt 12,9 grader Celsius
Kogepunkt 197,3 grader Celsius
Ansøgning
På grund af sin evne til at reducere frysepunktet, bruges monoethylenglycol til fremstilling af frostvæske og bremsevæske til biler samt til fremstilling af cellofan og polyurethan. I mindre grad bruges det til fremstilling af blæk og trykfarver.
Fareklasse
Henviser til brændbare stoffer. Selvantændelse sker ved en temperatur på 380 grader, et glimt af damp ved opvarmning til 120 grader. Giftig. Indtagelse er ikke tilladt. Dampe er mindre skadelige.
Glycerol
Kemisk formel: HOCH2CH(OH)CH2OH
Internationalt navn: Glycerin
CAS NR: 56-81-5
Kvalifikation: Imp. "h", GOST 6259-75
Udseende: klar, lugtfri væske
Pakning: 25 kg dåser, 250 kg tromler, 1500 terninger
Opbevaringsbetingelser: i et ventileret tørt rum ved lav temperatur
Synonymer: 1,2,3-trioxypropan
Vi tilbyder Glycerin i dåser, tønder, terninger til konkurrencedygtige priser.
| Specifikation | |
| Molekylær vægt | 92.10 |
| Grundstof, ikke mindre end | 99,5 % (faktisk 99,8 %) |
| Askeindhold, ikke mere | 0,01 % (faktisk mindre end 0,1 %) |
| Vandindhold, ikke mere | 0,5 % (faktisk 0,1 %) |
| Indhold af klorider, ikke mere | 0,001 % |
| Sulfatindhold, ikke mere | 0,002 % |
| Tungmetaller, ikke mere | 0,0005% (faktisk mindre end 0,00005%) |
| Klorforbindelser (som CL), ikke mere | 0,003 % |
| Arsen, ikke mere | 0,00015 % (faktisk mindre end 0,00001 %) |
| Farve (APHA), ikke mere | 20 (faktisk mindre end 10) |
Glycerin er en farveløs, hygroskopisk, tyktflydende, lugtfri, sødtsmagende væske. Blandbar i ethvert forhold med vand, ethanol, methanol, acetone, uopløseligt i chloroform og ether. Når glycerol blandes med vand, frigives varme, og der opstår sammentrækning (volumenreduktion). Når glycerol interagerer med hydrogenhalogenider eller phosphorhalogenider, dannes mono- eller dihalogenhydriner; med uorganiske og carboxylsyrer - komplette og ufuldstændige estere, med dehydrering - acrolein. Glycerol kan oxideres, og afhængigt af oxidationsmidlets betingelser og natur kan glyceraldehyd, glycerinsyre, tartronsyre, dihydroxyacetone, mesoxalsyre opnås. Glycerin findes i naturlige fedtstoffer og olier som blandede triglycerider af carboxylsyrer.
Ansøgning Glycerin er meget udbredt • i den farmaceutiske industri, for eksempel til fremstilling af nitroglycerin, medicinske salver; • i fødevareindustrien, for eksempel i produktion af likører, konfekture; • i kosmetikindustrien, i fremstillingen af parfume og kosmetik • i fremstillingen af glyptalharpikser; • som blødgøringsmiddel til stoffer, læder, papir; • som en del af emulgatorer, frostvæsker, smøremidler, skosværte, sæber og klæbemidler, • som råmateriale ved fremstilling af polyalkoholer, som anvendes i forskellige skum. • som blødgører til cellofan mv.
Ved hvilken temperatur fryser vand i varmerør i en boligbygning
Hvis temperaturen i huset forbliver -10 i flere dage, og der er vand i rørene, kan det fryse, hvilket vil føre til brud på rørene. Mange har sikkert set moderne varmebatterier med vandafløbsfunktion. Næsten alle moderne batterier er udstyret med evnen til at dræne vand. Dette gøres for, at vandet i nødstilfælde, når temperaturen i huset er -10, ikke fryser og river ikke rørene. Hvis situationen er kommet til dette, sympatiserer vi meget med dig, højst sandsynligt bliver du nødt til at skifte batterierne, da der under frysning af vand sandsynligvis er opstået mikrorevner, der gør den videre drift af disse batterier farlig.
Hvorfor kan vand fryse i rør? Hvis der i fyringssæsonen, netop når batterierne er fyldt med vand, opstår et nedbrud og vandet køles ned, og temperaturen falder hurtigt udenfor, kan det føre til frysning af rørene.
Vi har allerede besvaret spørgsmålet ved hvilken temperatur vand fryser, som et eksperiment, tag et lille glas, fyld det halvt med vand og sæt det i fryseren i flere timer, to timer er nok til, at vandet delvist bliver til is.
Vand er et af de vigtigste stoffer på vores planet. Den har en masse egenskaber, der gør den til en vis grad unik. En af de mest berømte egenskaber, som selv et lille barn kender til, er frysning af vand.Det er kendt, at 0 grader Celsius er vandets krystallisationstemperatur. Men ikke alt er så simpelt. Vi vil overveje nogle af subtiliteterne i denne proces yderligere.

Densitet af glycerinopløsning ved 25
Det aritmetiske gennemsnit af tæthederne af alkohol og glycerol.
209,4. 1.047. 25.265.0. 1.060. ... Se hvad er massefylden af vandige opløsninger af glycerin i andre ordbøger E236 Fil Myresyre.svg Strukturformel for myresyre Myresyre methansyre er den første ...
Hvad er tætheden af glycerin ved 17 grader Celsius?
8
Massefylde ved 25 C, g cm. ... En opløsning af glycerin i en koncentration på 25 % eller mere udsætter ikke mikrobiel forurening, i mere fortyndede opløsninger formerer mikroorganismer sig godt i den.
3,14
Hvilken væske har en højere densitet, glycerin eller alkohol? forklare
Ssss
TK-april på siden i hele Rusland. Koncentration, tæthed og brydningsindeks for opløsninger af glycerol 15 С. … 1,0594. 1,3633. 25.1.0620.
Beregn molmassen af begge stoffer. For alkohol er det mindre (92 g/mol mod 46 g/mol for alkohol), og massefylden er tilsvarende lavere. Når det kommer til ethylalkohol.
Hvad er meningen med sådanne spørgsmål? Information findes i søgemaskiner
Det aritmetiske gennemsnit af tæthederne af blandingens komponenter.
Bestem, hvilken masse glycerol med en densitet på 1,26 g ml der skal tages for at fremstille en vandig opløsning c.42. ... 111 g phthalsyreanhydrid og 46 g glycerin med en densitet på 28 V anbringes i et glasbæger med en kapacitet på 0,25 l.
Hvordan beregner man tætheden og viskositeten af en væske, der indeholder vand, alkohol og glycerin?
Hertil sælges rheometre. du behøver ikke at tælle noget. bare fryse.
triethylenglycol. propylenglycol. Glycerol. … propylenglycol 40%. -25 C. ... Densiteten af vandige opløsninger af ethylenglycol ved forskellige temperaturer.
Du skal kende procentdelen af alle komponenter i blandingen (mindst!)
Ingen måde. Er, se efter data modtaget af nogen.
Hjælp venligst, vil et stykke is flyde i benzin, petroleum, glycerin? hvorfor?
Det vil være i glycerin, det flyder ikke i whisky - massefylden er omtrent det samme som benzin
Det øger også tætheden af den færdige opløsning og forbedrer kvaliteten af boblerne. ... Glycerinopløsning 25g flaskeTula Pharmaceutical Factory LLC. … Natriumtetraboratopløsning i glycerinhætteglas 20% 30g, Samara FF Samara Rusland.
Is er mindre tæt end olie, så det bliver det.
Sammenlign tætheden af is med tætheden af disse væsker. hvis tætheden af is er mindre, så vil den flyde, hvis den er mere, vil den synke.
Ved ikke. afhænger af hvilket stykke. hvis der er nok luft i isen til at holde den på overfladen, vil den flyde, og hvis ikke, så vil den ikke. prøv det selv. petroleum er billigt.
Afhængig af hvilken temperatur denne is afkøles til
Kogepunktet for vandige opløsninger af glycerin falder med et fald i koncentrationen af glycerol med et indhold på 5% vand, kogepunktet er 160-161, dens massefylde er 1,26362 g cm3. … 25 25 C . ZnCl2.
Jeg har aldrig set is flyde i benzintanken og dunken. Og det er han bestemt))). Så han er nok i bunden. Jeg så kun glycerin i et hætteglas og i varme))).
Hov!
X mængde fortyndet glycerol, g En massefylde af destilleret glycerol, g ml ... Opløsninger af glycerol i en koncentration på 25% og derover er ikke udsat for mikrobiel kontaminering, mere fortyndede opløsninger er ...
Vil et stykke is flyde i benzin, petroleum, glycerin?
Find ud af tætheden og det er det!
Densitet af vandige opløsninger af alkoholer. Densiteter af vandige opløsninger g cm3 ved 20 C er angivet for følgende stoffer: ethanol, 1-propanol, 2-propanol, ethylenglycol, glycerol, D-mannitol.
Ja)))
Hvis isens tæthed er mindre end væskens densitet, vil isen flyde
Hvad er densiteten af glycerin ved en temperatur på 24 gr. MED?
Glycerin grader Celsius020406080100120140169180Tæthed g/cm3126712591250123812241208118811631126
For en temperatur på 24 grader = bestemmes ved interpolation mellem 20 og 40 grader
Beregn kogepunktet for en 8% opløsning af glycerol C3H6O3 i acetone. Svaret er 57,7oC. 4.En opløsning, hvoraf 100 ml indeholder 2,3 g ... Tag densiteten af opløsningen lig med én. Svar 608 Pa. Billet 14 25 1. Hvor mange gram BaCl2 2H2O ...
Spørgsmål om kemi))) Og fysik. Hvilken væske er tættere end vand og leder også elektricitet, men ikke metal?
Glycerin, ethylenglycoler, formamider, butyrolacton, næsten alle syrer, aminer. og meget mere.
Svovlsyrekoncentration, vægtprocent. Massefylde ved 25 C, g cm ... 25,60-0,1950 0,000 8 - relativ fugtighed, % - brydningsindeks for en vandig opløsning af glycerol ved 25 C for linje D natrium - opløsningstemperatur, C ...