Gefrierpunkt von Wasser
Der Gefriervorgang findet statt bei Abkühlung auf null Grad auf der Celsius-Skala. Dies gilt nicht für alle Gewässer. Moleküle lagern sich an Verunreinigungen an, bei denen es sich um Staub-, Salzpartikel usw. handelt. Daher kann reines oder destilliertes Wasser ohne das Vorhandensein dieser Verunreinigungen unter dem Einfluss niedriger Temperaturen in der Celsius-Säule länger in flüssigem Zustand bleiben als gewöhnliches Wasser.
Interessant ist auch, dass während andere Stoffe beim Gefrieren an Volumen abnehmen, Wasser dagegen zunimmt. Denn beim Übergang in den Festkörper vergrößert sich der Abstand zwischen den Molekülen. Obwohl das Volumen zunimmt, nimmt die Masse beim Einfrieren nicht zu und wiegt so viel wie warmes Wasser.
Viele Menschen fragen sich, warum Wasser unter einer dicken Eisschicht nicht gefriert. Jeder Physiker wird antworten, dass Wasser unter einer Eisschicht nicht gefriert, da die Eisoberfläche als Wärmeisolator dient.

Warum gefriert heißes Wasser schneller als kaltes Wasser?
Es ist bekannt, dass heißes oder warmes Wasser schneller gefriert als kaltes Wasser. Unglaublich aber wahr. Diese Entdeckung wurde von Erasto Mpemba gemacht. Er führte Experimente mit der gefrorenen Masse durch und stellte fest, dass die Masse schneller gefriert, wenn sie warm ist. Der Grund dafür ist, wie Untersuchungen gezeigt haben, die hohe Wärmeübertragung von heißem und warmem Wasser.

Hängen der Gefrierpunkt von Wasser und die Höhe zusammen?
Wie Sie wissen, ändert sich der Druck in der Höhe, daher unterscheidet sich die Temperatur beim Übergang in den festen Zustand aller wässrigen Lösungen in der Höhe von der Temperatur auf einer normalen Oberfläche.
Beispiele für Temperaturänderungen in der Höhe:
- Höhe 500 m - der Gefrierpunkt von Wasser ist nicht wie unter normalen Bedingungen null ° C, sondern bei Vorhandensein von bereits 1 ° C;
- Höhe 1500 m - Kristallisation erfolgt in Gegenwart von etwa drei ° C usw.

Wie Druck den Prozess der Wasserkristallisation beeinflusst
Wenn Sie den Zusammenhang zwischen Druck und Kristallisation von Wasser verstehen, ist alles ganz einfach.
Interessant! Je höher der Druck, desto geringer die Umwandlungsgeschwindigkeit von Wasser in Eiskristalle und desto höher der Siedepunkt!
Das ist das ganze Geheimnis, und wenn Sie logisch denken, gehen mit abnehmendem Druck alle Indikatoren in die entgegengesetzte Richtung. Daher ist es schwierig, in den Bergen etwas zu kochen, da die Temperatur, bei der Wasser kocht, keine hundert Grad Celsius erreicht. Umgekehrt schmilzt Eis auch bei niedrigen Temperaturen.
Kristallisationstemperatur wässriger Lösungen
Wasser ist ein gutes Lösungsmittel und verbindet sich daher leicht mit anderen Stoffen. Die resultierenden Lösungen gefrieren natürlich unter anderen Bedingungen. Betrachten Sie einige Optionen für Temperaturkriterien zum Einfrieren verschiedener Lösungen auf Wasserbasis.
Wasser und Alkohol. Bei einer großen Menge Alkohol im Wasser beginnt der Gefrierprozess bei sehr niedrigen Temperaturen. Beispielsweise beginnt bei einem Verhältnis von 60 % Wasser zu 40 % Alkohol die Kristallisation bei minus 22,5 °C.
Wasser und Salz. Die Temperatur, bei der das Gefrieren auftritt, steht in direktem Zusammenhang mit dem Salzgehalt des Wassers. Das Prinzip lautet: Je mehr Salz im Wasser, desto niedriger die Kristallisationstemperatur. Wie Meerwasser gefriert, hängt direkt mit dem Salzgehalt zusammen.
Wasser und Soda. Die Kristallisationstemperatur der Lösung beträgt 44 Prozent plus 7°C.
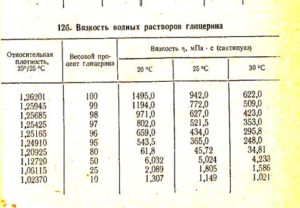
Wasser und Glycerin in einem Verhältnis von 80 % zu 20 %, wobei 80 Glycerin und 20 Wasser ist, ist das Vorhandensein von –20 °C erforderlich, um die Lösung einzufrieren.
Alle Temperaturwerte schwanken je nach Konzentrationsgrad von Fremdlösungen oder anderen Stoffen im Wasser.
Messung der Viskosität von Flüssigkeiten mit einem Ostwald-Viskosimeter
Um den Viskositätskoeffizienten ηhis der untersuchten Flüssigkeit mit einem Ostwald-Kapillarviskosimeter (Abb. 6) zu bestimmen, muss man wissen:
- η0 ist die Viskosität von Wasser,
- t0 ist die Zeit des Wasserflusses zwischen den Markierungen a und b,
- tx ist die Fließzeit der untersuchten Flüssigkeit zwischen den Markierungen a und b,
- ρ0 ist die Dichte von Wasser,
- ρx ist die Dichte der untersuchten Flüssigkeit.
Reis. 6. Ostwald-Kapillarviskosimeter (a, b, d - Markierungen, die den Flüssigkeitsstand begrenzen, c - Kapillare).
Die Viskosität der untersuchten Flüssigkeit wird durch die Formel (9) bestimmt.
Arbeitsauftrag
Aufgabe 1. Bestimmen Sie die Viskosität von Lösungen mit unterschiedlichen Konzentrationen.
-
Gießen Sie Wasser in den Schenkel des Viskosimeters, der keine Kapillare hat (Abb. 6), bis zur Markierung d.
-
Saugen Sie mit einer Birne die Flüssigkeit durch die Kapillare bis zur Markierung a. Nachdem Sie die Birne entfernt haben, schließen Sie das Loch des linken Knies des Viskosimeters (mit einer Hand, einem Korken, einem Tupfer usw.) (siehe Abb. 6). Bereiten Sie die Stoppuhr vor und schalten Sie sie ein, öffnen Sie das Loch des linken Knies und schalten Sie sie aus, wenn die Markierung b fließt, und bestimmen Sie so t0 - die Zeit des Wasserflusses zwischen den Markierungen a und b.
-
Wiederholen Sie die Messungen 4-5 Mal, ermitteln Sie die durchschnittliche Zeit.
-
Führen Sie die Schritte 1-3 für alle Testflüssigkeiten durch.
-
Berechnen Sie die Viskositätskoeffizienten der untersuchten Flüssigkeiten mit Formel (9).
-
Tragen Sie die Daten in Tabelle 1 ein.
Tabelle 1
| № | Konzentration, % | t1 | t2 | t3 | t4 | t5 | | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 | ||||||||
| 5 | ||||||||
| 6 |
Aufgabe 2. Bestimmen Sie die Konzentration einer unbekannten Lösung.
-
Auftragen des Viskositätsverhältnisses gegen die Lösungskonzentration
-
Wenn Sie die Viskosität der unbekannten Lösung kennen, bestimmen Sie ihre Konzentration aus dem Diagramm.
Tabelle 2
Dichte von Wasser bei verschiedenen Temperaturen
| ρ, kg/m3 | t, 0C | ρ, kg/m3 | t, 0C |
| 999,13 | 15 | 998,02 | 21 |
| 998,97 | 16 | 997,80 | 22 |
| 998,80 | 17 | 997,57 | 23 |
| 998,43 | 19 | 997,32 | 24 |
| 998,23 | 20 | 997,07 | 25 |
Tisch 3
Viskosität von Wasser bei verschiedenen Temperaturen
| η, Pa.s | t, 0C | η, Pa.s | t, 0C |
| 0,00114 | 15 | 0,00098 | 21 |
| 0,00111 | 16 | 0,00096 | 22 |
| 0,00108 | 17 | 0,00093 | 23 |
| 0,00103 | 19 | 0,00091 | 24 |
| 0,00100 | 20 | 0,00089 | 25 |
Tabelle 4
Dichte von Glycerinlösungen verschiedener Konzentrationen
| MIT, % | ρ, kg/m3 | MIT, % | ρ, kg/m3 |
| 5 | 1012,5 | 45 | 1112,5 |
| 10 | 1025,0 | 50 | 1125,0 |
| 15 | 1037,5 | 55 | 1137,5 |
| 20 | 1042,5 | 60 | 1150,0 |
| 25 | 1052,5 | 65 | 1162,5 |
| 30 | 1075,0 | 70 | 1175,0 |
| 35 | 1087,5 | 75 | 1187,5 |
| 40 | 1100,0 | 80 | 1200,0 |
Eigenständiges Arbeiten zum Thema:
– Lösung situativer Probleme;
- Abstracts anhören
Endkontrolle des Wissens:
– Lösen von Problemen für Tickets;
– Antworten auf Endkontrolltickets;
- zusammenfassend.
Hausaufgaben zum Verständnis des Unterrichtsthemas
Kontrollfragen zum Unterrichtsthema:
1. Wie nennt man die Viskosität einer Flüssigkeit?
2. Welche Art von Flüssigkeitsströmung wird als laminar oder turbulent bezeichnet?
3. Was charakterisiert die Reynolds-Formel?
4. Schreiben Sie die Newtonsche Formel und erklären Sie die physikalische Bedeutung der darin enthaltenen Größen?
5. Was ist der Koeffizient der dynamischen Viskosität? In welchen Einheiten wird gemessen?
6. Welche Flüssigkeiten werden Newtonsche genannt? Was bestimmt ihren Viskositätskoeffizienten?
7. Welche Flüssigkeiten werden nicht-newtonsche Flüssigkeiten genannt und was bestimmt ihren Viskositätskoeffizienten?
8. Schreiben Sie die Poiseuille-Formel auf, erklären Sie die physikalische Bedeutung der darin enthaltenen Größen.
9. Mit welchen Methoden wird die Viskosität einer Flüssigkeit bestimmt?
10. Erzählen Sie von den rheologischen Eigenschaften von Blut und anderen biologischen Flüssigkeiten, von der Anwendung rheologischer Analysen in der Medizin.
11. Was zeigt der Geschwindigkeitsgradient? Grafisch darstellen.
12. Welches Phänomen nennt man innere Reibung?
Testaufgaben zum Thema:
IST DIE ANWENDUNG VON GLYCERIN IN DER HEIZUNG GERECHTFERTIGT?
An das Kühlmittel für Heizungsanlagen werden recht hohe Anforderungen gestellt. Es muss feuer- und explosionssicher sein, eine gute thermische Leistung erbringen und darf auch keine verbotenen Zusatzstoffe enthalten. Als Basis für die Herstellung von hochwertigen Wärmeträgerflüssigkeiten wird Ethylenglykol oder Propylenglykol verwendet, was auch für Umweltfreundlichkeit sorgt.
Kürzlich sind Frostschutzmittel auf Glyzerinbasis auf dem Markt erschienen. Dieses Produkt wird hauptsächlich von kleinen, wenig bekannten Firmen auf dem Frostschutzmarkt beworben. Es stellt sich die Frage: Glyzerin und Kühlmittel - ist ihre Vereinigung angemessen?
Und tatsächlich wurden die ersten Frostschutzmittel, die in den zwanziger Jahren des letzten Jahrhunderts in unserem Land auftauchten, auf der Basis von Glycerin hergestellt. Ihre Schwächen waren eine unzureichende Fließfähigkeit und eine extrem hohe Viskosität, mit der die Pumpen nicht umgehen konnten. Sie versuchten, das Problem mit Hilfe von Alkohol, einschließlich Methylalkohol, zu lösen. Jedoch traten zusammen mit der Verbesserung der Fließfähigkeit viele Probleme auf. Tatsache ist, dass Methanol ein starkes psychotropes Gift ist.Das Verhalten von Autofahrern, die solches Frostschutzmittel unfreiwillig schnüffelten, widersprach daher manchmal jeder Logik und stellte eine Gefahr für die Gesundheit und das Leben anderer dar. Außerdem hat Methylalkohol einen niedrigen Siedepunkt und wenn er verdunstet, steigt die Viskosität des Produkts sofort an. Das Problem wurde erst gelöst, als Ethylenglykol die Basis des Kühlmittels wurde. Und Ende der dreißiger, Anfang der vierziger Jahre ersetzten Ethylenglykol-Frostschutzmittel fast vollständig die Glycerin-Methanol-Frostschutzmittel.
Darüber hinaus ist Glycerin thermisch instabil, zersetzt sich bei längerem Erhitzen unter Bildung einer giftigen flüchtigen Substanz - Acrolein, das einen scharfen unangenehmen Geruch hat, der zum Reißen führt. Zersetzungsprodukte sind giftig und ausfallende erhöhen die korrosive Aktivität des Kühlmittels. Dadurch steigen die Anforderungen an Dichtungen und Teile aus unpolaren Gummis und Kunststoffen. Neben der hohen Viskosität schäumt Glycerin auch stark, was zu einer Belüftung des Systems und einer schlechten Wärmeabfuhr führt.
Hersteller von Glyzerin-Kühlmitteln versuchen, alle oben genannten Nachteile auszugleichen, indem sie verschiedene Additive hinzufügen, darunter aliphatische Alkohole - Methanol, Ethanol, Propanol. Diese Alkohole können die Viskosität oder Dichte des Frostschutzmittels erheblich verringern. Sie sieden jedoch bereits bei Temperaturen über 65 Grad, was zu einer Verschlechterung der thermischen Leistung des Kühlmittels führt. Diese Alkohole sind in der Lage, Gummi und Polymere aufzulösen und neigen außerdem zu Kavitation und starker Verdunstung. Außerdem ist Methanol ein starkes Gift und darf nicht zur Herstellung von Frostschutzmitteln verwendet werden.
Um die Qualität von Glyzerin-Kühlmitteln sicherzustellen, insbesondere bei Methanol, müssen der Mischung teure Additivpakete hinzugefügt werden. Und obwohl die Kosten für Glycerin jetzt niedriger sind als die Kosten für Glykole, ist das Additivpaket zur Herstellung hochwertiger Glyzerin-Wärmeübertragungsflüssigkeiten teurer als das Additivpaket für Frostschutzmittel auf Basis von Ethylenglykol und Propylenglykol. Und wenn die Kosten für Glycerin-Frostschutzmittel auf dem Markt niedriger sind als die für Glykol, bedeutet dies, dass der Hersteller einfach an der Qualität gespart und dem Produkt nicht die notwendigen teuren Zusatzstoffe hinzugefügt hat!
Der Käufer hat also die Wahl: Entweder ein zuverlässiges und bewährtes Kühlmittel auf Glykolbasis oder die Glyzerin-„Katze im Sack“.
Die Wahl unseres Unternehmens ist, wie die meisten führenden Hersteller von Frostschutzmitteln, grundsätzlich eindeutig - Glycerin kann nicht in reiner Form verwendet werden, aber gemischt mit Methanol ist gefährlich und kriminell!
Das Hauptargument, das unsere Position zu diesem Thema bestätigt, ist, dass in allen wichtigen und großen Anlagen die Verwendung von Glyzerin in Heiz- und Kühlsystemen nach bestehenden Standards NICHT ERLAUBT ist!
MEG
Ethylenglycol ist ein Produkt der Ethylenoxid-Hydratation in Gegenwart von Schwefel- oder Phosphorsäure. Bezieht sich auf mehrwertige Alkohole. Friert nicht bei niedrigen Temperaturen und senkt den Gefrierpunkt von Wasser. Kann Wasser aus der Luft aufnehmen.
Es wird in Metall- und Kunststofffässern mit einem Fassungsvermögen von bis zu 227 Litern verkauft. Sowie Plastikwürfel 1000l.
Der Stoff muss in einem verschlossenen Behälter aus Aluminium oder Stahl mit Korrosionsschutz in einem geschlossenen Lager ohne Heizung gelagert werden. Die Haltbarkeit für die höchste Sorte beträgt 12 Monate, für die erste Sorte 3 Jahre ab Herstellungsdatum.
Name des Indikators Norm
Aussehen, Geruch Klare, farblose Flüssigkeit mit öliger Textur. Ohne Geruch.
Löslich in Wasser, Alkoholen, Toluol, Benzol
Dichte 1,112 g/cm?.
Schmelzpunkt 12,9 Grad Celsius
Siedepunkt 197,3 Grad Celsius
Anwendung
Aufgrund seiner Fähigkeit, den Gefrierpunkt zu senken, wird Monoethylenglykol bei der Herstellung von Frostschutzmitteln und Bremsflüssigkeiten für Autos sowie bei der Herstellung von Zellophan und Polyurethan verwendet. In geringerem Umfang wird es bei der Herstellung von Tinten und Druckfarben verwendet.
Gefahrenklasse
Bezieht sich auf brennbare Stoffe. Selbstentzündung tritt bei einer Temperatur von 380 Grad auf, ein Dampfblitz bei Erwärmung auf 120 Grad. Giftig. Verschlucken ist nicht erlaubt. Dämpfe sind weniger schädlich.
Glycerin
Chemische Formel: HOCH2CH(OH)CH2OH
Internationaler Name: Glyzerin
CAS-NR: 56-81-5
Qualifikation: Kobold "h", GOST 6259-75
Aussehen: klare, geruchlose Flüssigkeit
Verpackung: 25 kg Kanister, 250 kg Fässer, 1500 Würfel
Lagerbedingungen: in einem belüfteten trockenen Raum bei niedriger Temperatur
Synonyme: 1,2,3-Trioxypropan
Wir bieten Glycerin in Dosen, Fässern und Würfeln zu wettbewerbsfähigen Preisen an.
| Spezifikation | |
| Molekulargewicht | 92.10 |
| Grundsubstanz, nicht weniger als | 99,5 % (tatsächlich 99,8 %) |
| Aschegehalt, nicht mehr | 0,01 % (eigentlich weniger als 0,1 %) |
| Wassergehalt, nicht mehr | 0,5 % (eigentlich 0,1 %) |
| Gehalt an Chloriden, nicht mehr | 0,001 % |
| Sulfatgehalt, nicht mehr | 0,002 % |
| Schwermetalle, nicht mehr | 0,0005 % (eigentlich weniger als 0,00005 %) |
| Chlorverbindungen (als CL), nicht mehr | 0,003 % |
| Arsen, nicht mehr | 0,00015 % (tatsächlich weniger als 0,00001 %) |
| Farbe (APHA), nicht mehr | 20 (eigentlich weniger als 10) |
Glycerin ist eine farblose, hygroskopische, viskose, geruchlose, süß schmeckende Flüssigkeit. In jedem Verhältnis mischbar mit Wasser, Ethanol, Methanol, Aceton, unlöslich in Chloroform und Ether. Beim Mischen von Glycerin mit Wasser wird Wärme freigesetzt und es kommt zur Kontraktion (Volumenreduktion). Wenn Glycerin mit Halogenwasserstoffsäuren oder Phosphorhalogeniden in Wechselwirkung tritt, werden Mono- oder Dihalogenhydrine gebildet; mit anorganischen und Carbonsäuren - vollständige und unvollständige Ester, mit Dehydratisierung - Acrolein. Glycerin kann oxidiert werden, und abhängig von den Bedingungen und der Art des Oxidationsmittels können Glycerinaldehyd, Glycerinsäure, Tartronsäure, Dihydroxyaceton, Mesoxalsäure erhalten werden. Glycerin kommt in natürlichen Fetten und Ölen als gemischte Triglyceride von Carbonsäuren vor.
Anwendung Glycerin ist weit verbreitet • in der pharmazeutischen Industrie, zum Beispiel zur Herstellung von Nitroglycerin, medizinischen Salben; • in der Lebensmittelindustrie, zB bei der Herstellung von Likören, Süßwaren; • in der Kosmetikindustrie, bei der Herstellung von Parfums und Kosmetika • bei der Herstellung von Glyptalharzen; • als Weichmacher für Stoffe, Leder, Papier; • als Bestandteil von Emulgatoren, Frostschutzmitteln, Schmiermitteln, Schuhcremes, Seifen und Klebstoffen, • als Rohstoff bei der Herstellung von Polyalkoholen, die in verschiedenen Schäumen Verwendung finden. • als Weichmacher für Zellophan etc.
Bei welcher Temperatur gefriert Wasser in Heizungsrohren in einem Wohngebäude?
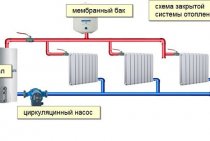
Wenn die Temperatur im Haus mehrere Tage lang -10 bleibt und sich Wasser in den Rohren befindet, kann es gefrieren, was zum Bruch der Rohre führt. Moderne Heizbatterien mit Wasserablauffunktion haben sicher viele schon gesehen. Fast alle modernen Batterien sind mit der Fähigkeit ausgestattet, Wasser abzulassen. Dies geschieht, damit im Notfall, wenn die Temperatur im Haus -10 beträgt, das Wasser nicht gefriert und die Rohre nicht zerreißen. Wenn es dazu gekommen ist, haben wir großes Verständnis für Sie, höchstwahrscheinlich müssen Sie die Batterien wechseln, da beim Gefrieren von Wasser wahrscheinlich Mikrorisse aufgetreten sind, die den weiteren Betrieb dieser Batterien gefährlich machen.
Warum kann Wasser in Rohren gefrieren. Wenn während der Heizperiode, gerade wenn sich die Batterien mit Wasser füllen, ein Ausfall auftritt und das Wasser abgekühlt wird und die Außentemperatur schnell abfällt, kann dies zum Einfrieren der Rohre führen.
Die Frage, bei welcher Temperatur Wasser gefriert, haben wir bereits beantwortet, nehmen Sie als Experiment ein kleines Glas, füllen Sie es zur Hälfte mit Wasser und stellen Sie es für mehrere Stunden in den Gefrierschrank, zwei Stunden reichen aus, damit sich das Wasser teilweise in Eis verwandelt.
Wasser ist einer der wichtigsten Stoffe auf unserem Planeten. Es hat viele Eigenschaften, die es zu einem gewissen Grad einzigartig machen. Eine der berühmtesten Eigenschaften, die schon ein kleines Kind kennt, ist das Gefrieren von Wasser.Es ist bekannt, dass 0 Grad Celsius die Kristallisationstemperatur von Wasser ist. Aber nicht alles ist so einfach. Wir werden einige der Feinheiten dieses Prozesses weiter betrachten.

Dichte der Glycerinlösung bei 25
Das arithmetische Mittel der Dichten von Alkohol und Glycerin.
209.4. 1.047. 25.265.0. 1.060. ... Sehen Sie, was die Dichte von wässrigen Lösungen von Glycerin in anderen Wörterbüchern ist E236-Datei Ameisensäure.svg Strukturformel von Ameisensäure Ameisensäure Methansäure ist die erste ...
Welche Dichte hat Glycerin bei 17 Grad Celsius?
8
Dichte bei 25 C, g cm. ... Eine Glycerinlösung mit einer Konzentration von 25% oder mehr zeigt keine mikrobielle Kontamination, in verdünnteren Lösungen vermehren sich Mikroorganismen gut darin.
3,14
Welche Flüssigkeit hat eine höhere Dichte, Glycerin oder Alkohol? erklären
Ssss
TK-April auf der Website in ganz Russland. Konzentration, Dichte und Brechungsindex von Glycerinlösungen 15 С. … 1,0594. 1.3633. 25.1.0620.
Berechnen Sie die Molmasse beider Stoffe. Bei Alkohol ist sie geringer (92 g/mol gegenüber 46 g/mol bei Alkohol) und die Dichte entsprechend geringer. Wenn es um Ethylalkohol geht.
Was ist der Sinn solcher Fragen? Informationen werden in Suchmaschinen gefunden
Das arithmetische Mittel der Dichten der Komponenten der Mischung.
Bestimmen Sie, welche Masse an Glycerin mit einer Dichte von 1,26 g ml verwendet werden sollte, um eine wässrige Lösung herzustellen c.42. ... 111 g Phthalsäureanhydrid und 46 g Glycerin mit einer Dichte von 28 V werden in einem Becherglas mit einem Fassungsvermögen von 0,25 l vorgelegt.
Wie berechnet man die Dichte und Viskosität einer Flüssigkeit, die Wasser, Alkohol und Glycerin enthält?
Dafür werden Rheometer verkauft. du musst nichts zählen. einfach einfrieren.
Triethylenglykol. Propylenglykol. Glycerin. … Propylenglykol 40 %. -25 C. ... Die Dichte von wässrigen Lösungen von Ethylenglykol bei verschiedenen Temperaturen.
Sie müssen den Prozentsatz aller Komponenten der Mischung kennen (mindestens!)
Auf keinen Fall. Suchen Sie nach Daten, die von jemandem empfangen wurden.
Bitte helfen Sie, schwimmt ein Stück Eis in Benzin, Kerosin, Glyzerin? Warum?
Es wird in Glycerin sein, es schwimmt nicht in Whisky - die Dichte ist ungefähr die gleiche wie bei Benzin
Es erhöht auch die Dichte der fertigen Lösung und verbessert die Qualität der Blasen. ... Glycerinlösung 25g FlascheTula Pharmaceutical Factory LLC. … Natriumtetraborat-Lösung in Glycerin-Fläschchen 20% 30g, Samara FF, Samara Russland.
Eis ist weniger dicht als Öl, also wird es sein.
Vergleichen Sie die Dichte von Eis mit der Dichte dieser Flüssigkeiten. Wenn die Dichte des Eises geringer ist, schwimmt es, wenn es größer ist, sinkt es.
Weiß nicht. kommt drauf an welches stück. Wenn genügend Luft im Eis ist, um es an der Oberfläche zu halten, schwimmt es, und wenn nicht, dann nicht. Versuch es selber. Kerosin ist billig.
Je nachdem auf welche Temperatur dieses Eis gekühlt wird
Der Siedepunkt wässriger Glycerinlösungen nimmt mit abnehmender Glycerinkonzentration mit einem Wassergehalt von 5% ab, der Siedepunkt beträgt 160-161, seine Dichte beträgt 1,26362 g cm3. … 25 25 C . ZnCl2.
Ich habe noch nie Eis im Benzintank und Kanister schwimmen sehen. Und er ist es sicherlich))). Also ist er wahrscheinlich ganz unten. Ich habe Glycerin nur in einem Fläschchen und in Hitze gesehen))).
Ojoy!
X Menge an verdünntem Glycerin, g A Dichte an destilliertem Glycerin, g ml ... Glycerinlösungen mit einer Konzentration von 25% und mehr unterliegen keiner mikrobiellen Kontamination, stärker verdünnte Lösungen sind ...
Schwimmt ein Stück Eis in Benzin, Kerosin, Glyzerin?
Finden Sie die Dichte heraus und das war's!
Dichte wässriger Lösungen von Alkoholen. Für folgende Substanzen sind Dichten wässriger Lösungen g cm3 bei 20 C angegeben: Ethanol, 1-Propanol, 2-Propanol, Ethylenglykol, Glycerin, D-Mannitol.
Ja)))
Wenn die Dichte des Eises geringer ist als die Dichte der Flüssigkeit, schwimmt das Eis
Wie hoch ist die Dichte von Glycerin bei einer Temperatur von 24 g? MIT?
Glycerin Grad Celsius020406080100120140169180Dichte g/cm3126712591250123812241208118811631126
Bei einer Temperatur von 24 Grad = durch Interpolation zwischen 20 und 40 Grad ermitteln
Berechnen Sie den Siedepunkt einer 8%igen Lösung von Glycerin C3H6O3 in Aceton. Die Antwort lautet 57,7 °C. 4.Eine Lösung, von der 100 ml 2,3 g enthalten ... Nehmen Sie die Dichte der Lösung gleich eins. Antwort 608 Pa. Ticket 14 25 1. Wie viel Gramm BaCl2 · 2H2O ...
Fragen zu Chemie))) Und Physik. Welche Flüssigkeit ist dichter als Wasser und leitet auch Strom, aber kein Metall?
Glycerin, Ethylenglykole, Formamide, Butyrolacton, fast alle Säuren, Amine. und vieles mehr.
Schwefelsäurekonzentration, Masse-%. Dichte bei 25 C, g cm ... 25,60-0,1950 0,000 8 - relative Feuchtigkeit,% - Brechungsindex einer wässrigen Lösung von Glycerin bei 25 C für Linie D Natrium - Lösungstemperatur, C ...