Punto de congelación del agua
El proceso de congelación se lleva a cabo cuando se enfría a cero grados en la escala Celsius. Esto no se aplica a todas las aguas. Las moléculas se adhieren a las impurezas, que son partículas de polvo, sal, etc. Por lo tanto, el agua pura o destilada, sin la presencia de estas mismas impurezas, bajo la influencia de las bajas temperaturas en la columna Celsius, puede permanecer en estado líquido más tiempo que el agua ordinaria.
También es interesante que mientras otras sustancias disminuyen de volumen al congelarse, el agua, por el contrario, aumenta. Esto se debe a que la distancia entre las moléculas se expande durante la transición al estado sólido. A pesar de que el volumen aumenta, la masa no aumenta al congelarse y pesa tanto como el agua caliente.
Muchas personas se preguntan por qué el agua no se congela bajo una gruesa capa de hielo. Cualquier físico responderá que bajo una capa de hielo, el agua no se congela, ya que la superficie del hielo sirve como aislante térmico.

¿Por qué el agua caliente se congela más rápido que el agua fría?
Se sabe que el agua caliente o tibia se congela más rápido que el agua fría. Increíble pero cierto. Este descubrimiento fue realizado por Erasto Mpemba. Realizó experimentos con la masa congelada y descubrió que si la masa está caliente, se congelará más rápido. La razón de esto, como han demostrado los estudios, es la alta transferencia de calor del agua caliente y tibia.

¿Están relacionados el punto de congelación del agua y la altitud?
Como sabes, la presión cambia en altura, por lo que la temperatura de transición al estado sólido de todas las soluciones acuosas en altura difiere de la temperatura en una superficie normal.
Ejemplos de cambios de temperatura en altitud:
- altitud 500 m - el punto de congelación del agua no es cero ° C, como en condiciones normales, sino en presencia de ya un ° C;
- altura 1500 m - la cristalización se produce en presencia de unos tres ° C, etc.

Cómo afecta la presión al proceso de cristalización del agua
Si comprende la relación entre la presión y la cristalización del agua, entonces todo es bastante simple.
¡Interesante! ¡Cuanto mayor sea la presión, menor será la velocidad de transformación del agua en cristales de hielo y mayor será el punto de ebullición!
Ese es todo el secreto, y si piensas lógicamente, con una disminución de la presión, todos los indicadores van en la dirección opuesta. Por eso, es difícil cocinar algo en la montaña, ya que la temperatura a la que hierve el agua no llega a los cien grados centígrados. Por el contrario, el hielo se derrite incluso a bajas temperaturas.
Temperatura de cristalización de soluciones acuosas.
El agua es un buen disolvente y por lo tanto se combina fácilmente con otras sustancias. Las soluciones resultantes, por supuesto, se congelarán en diferentes condiciones. Considere un par de opciones para los criterios de temperatura para congelar diferentes soluciones basadas en agua.
Agua y alcohol. Con una gran cantidad de alcohol en el agua, el proceso de congelación comenzará en presencia de temperaturas muy bajas. Por ejemplo, en una proporción de 60 % de agua por 40 % de alcohol, la cristalización comenzará en presencia de menos 22,5 °C.
Agua y sal. La temperatura a la que se produce la congelación está directamente relacionada con el grado de salinidad del agua. El principio es que cuanta más sal haya en el agua, menor será la temperatura de cristalización. La forma en que se congela el agua de mar está directamente relacionada con el contenido de sal.
Agua y refrescos. La temperatura de cristalización de la solución es del 44 por ciento, más 7°C.
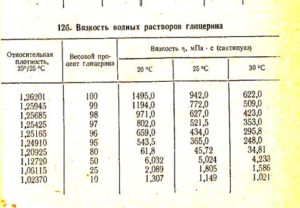
Agua y glicerina, en una proporción de 80% a 20%, donde 80 es glicerina, y 20 es agua, se requiere la presencia de -20°C para congelar la solución.
Todos los valores de temperatura fluctúan según el grado de concentración de soluciones extrañas u otras sustancias en el agua.
Medición de la viscosidad de líquidos con un viscosímetro Ostwald
Para determinar el coeficiente de viscosidad ηhis del líquido investigado usando un viscosímetro capilar Ostwald (Fig. 6), es necesario saber:
- η0 es la viscosidad del agua,
- t0 es el tiempo de flujo de agua entre las marcas a y b,
- tx es el tiempo de flujo del líquido investigado entre las marcas a y b,
- ρ0 es la densidad del agua,
- ρx es la densidad del líquido investigado.
Arroz. 6. Viscosímetro capilar Ostwald (a, b, d - marcas que limitan el nivel de líquido, c - capilar).
La viscosidad del líquido investigado está determinada por la fórmula (9).
Orden de trabajo
Tarea 1. Determinar la viscosidad de soluciones con diferentes concentraciones.
-
Vierta agua en la pata del viscosímetro que no tiene capilar (Fig. 6) hasta la marca d.
-
Con una pera, succione el líquido a través del capilar para marcar a. Después de quitar la pera, cierre el orificio de la rodilla izquierda del viscosímetro (con una mano, un corcho, un hisopo, etc.) (ver Fig. 6). Prepare y encienda el cronómetro, abriendo el orificio de la rodilla izquierda, y apáguelo cuando fluya la marca b, determinando así t0 - el tiempo de flujo de agua entre las marcas a y b.
-
Repita las mediciones 4-5 veces, encuentre el tiempo promedio.
-
Realice los pasos 1-3 para todos los líquidos de prueba.
-
Calcular los coeficientes de viscosidad de los líquidos estudiados utilizando la fórmula (9).
-
Ingrese los datos en la tabla 1.
tabla 1
| № | Concentración, % | t1 | t2 | t3 | t4 | t5 | | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 | ||||||||
| 5 | ||||||||
| 6 |
Tarea 2. Determinar la concentración de una solución desconocida.
-
Trazar la relación de viscosidad frente a la concentración de la solución
-
Conociendo la viscosidad de la solución desconocida, determine su concentración a partir del gráfico.
Tabla 2
Densidad del agua a diferentes temperaturas.
| r, kg/m3 | t, 0C | r, kg/m3 | t, 0C |
| 999,13 | 15 | 998,02 | 21 |
| 998,97 | 16 | 997,80 | 22 |
| 998,80 | 17 | 997,57 | 23 |
| 998,43 | 19 | 997,32 | 24 |
| 998,23 | 20 | 997,07 | 25 |
Tabla 3
Viscosidad del agua a diferentes temperaturas.
| η, Pa.s | t, 0C | η, Pa.s | t, 0C |
| 0,00114 | 15 | 0,00098 | 21 |
| 0,00111 | 16 | 0,00096 | 22 |
| 0,00108 | 17 | 0,00093 | 23 |
| 0,00103 | 19 | 0,00091 | 24 |
| 0,00100 | 20 | 0,00089 | 25 |
Tabla 4
Densidad de soluciones de glicerina de varias concentraciones.
| CON, % | r, kg/m3 | CON, % | r, kg/m3 |
| 5 | 1012,5 | 45 | 1112,5 |
| 10 | 1025,0 | 50 | 1125,0 |
| 15 | 1037,5 | 55 | 1137,5 |
| 20 | 1042,5 | 60 | 1150,0 |
| 25 | 1052,5 | 65 | 1162,5 |
| 30 | 1075,0 | 70 | 1175,0 |
| 35 | 1087,5 | 75 | 1187,5 |
| 40 | 1100,0 | 80 | 1200,0 |
Trabajo independiente sobre el tema:
– solución de problemas situacionales;
- escuchar resúmenes
Control final del conocimiento:
– resolución de problemas de tickets;
– respuestas a los tiquetes de control final;
- resumiendo.
Tarea para entender el tema de la lección.
Preguntas de control sobre el tema de la lección:
1. ¿Cómo se llama la viscosidad de un líquido?
2. ¿Qué tipo de flujo de fluido se llama laminar?¿Turbulento?
3. ¿Qué caracteriza a la fórmula de Reynolds?
4. Escribe la fórmula de Newton y explica el significado físico de las cantidades incluidas en ella.
5. ¿Cuál es el coeficiente de viscosidad dinámica? ¿En qué unidades se mide?
6. ¿Qué fluidos se llaman newtonianos? ¿Qué determina su coeficiente de viscosidad?
7. ¿Qué líquidos se denominan no newtonianos?¿Qué determina su coeficiente de viscosidad?
8. Escribe la fórmula de Poiseuille, explica el significado físico de las cantidades incluidas en ella.
9. ¿Qué métodos se utilizan para determinar la viscosidad de un líquido?
10. Informar sobre las propiedades reológicas de la sangre y otros fluidos biológicos, sobre el uso de análisis reológicos en medicina.
11. ¿Qué muestra el gradiente de velocidad? Mostrar gráficamente.
12. ¿Qué fenómeno se llama fricción interna?
Tareas de prueba sobre el tema:
¿ESTÁ JUSTIFICADA LA APLICACIÓN DE GLICERINA EN CALEFACCIÓN?
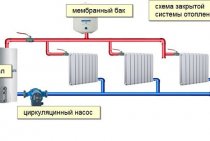
Se imponen requisitos bastante altos al refrigerante para los sistemas de calefacción. Debe ser a prueba de fuego y explosión, proporcionar un buen desempeño térmico y además no contener aditivos de uso prohibido. El glicol de etileno o el glicol de propileno se utiliza como base para la producción de fluido de transferencia de calor de alta calidad, que también garantiza el respeto por el medio ambiente.
Recientemente, han aparecido en el mercado refrigerantes anticongelantes a base de glicerina. Este producto es promocionado principalmente por pequeñas empresas poco conocidas en el mercado de anticongelantes. Surge la pregunta: glicerina y refrigerante: ¿es apropiada su unión?
Y, efectivamente, los primeros anticongelantes que aparecieron en nuestro país en los años veinte del siglo pasado se elaboraban a base de glicerina. Sus debilidades eran la fluidez insuficiente y la viscosidad extremadamente alta, que las bombas no podían manejar. Intentaron resolver el problema con la ayuda de alcohol, incluido el alcohol metílico. Sin embargo, junto con la mejora en la fluidez, aparecieron muchos problemas. El hecho es que el metanol es un fuerte veneno psicotrópico.Como resultado, el comportamiento de los conductores que involuntariamente olfatearon ese anticongelante a veces desafiaba cualquier lógica y representaba un peligro para la salud y la vida de los demás. Además, el alcohol metílico tiene un punto de ebullición bajo y cuando se evapora, la viscosidad del producto aumenta inmediatamente. El problema se resolvió solo cuando el etilenglicol se convirtió en la base del refrigerante. Y a fines de los años treinta, principios de los cuarenta, los anticongelantes de etilenglicol reemplazaron casi por completo a los de glicerina y metanol.
Además, la glicerina es térmicamente inestable, se descompone durante el calentamiento prolongado, con la formación de una sustancia volátil venenosa: la acroleína, que tiene un olor fuerte y desagradable que provoca lagrimeo. Los productos de descomposición son tóxicos y la precipitación aumenta la actividad corrosiva del refrigerante. Como resultado, los requisitos para juntas y piezas fabricadas con cauchos y plásticos no polares están aumentando. Además de la alta viscosidad, la glicerina también genera mucha espuma, lo que conduce a la ventilación del sistema y a una mala disipación del calor.
Los fabricantes de refrigerantes de glicerina están tratando de compensar todas las desventajas anteriores agregando varios aditivos, incluidos alcoholes alifáticos: metanol, etanol, propanol. Estos alcoholes pueden reducir significativamente la viscosidad o la densidad del refrigerante anticongelante. Pero ya hierven a temperaturas superiores a 65 grados, lo que conduce a un deterioro en el rendimiento térmico del refrigerante. Estos alcoholes son capaces de disolver el caucho y los polímeros, y también son propensos a la cavitación y a una fuerte evaporación. Además, el metanol es un veneno fuerte y su uso está prohibido en la producción de líquidos anticongelantes.
Asegurar la calidad de los refrigerantes de glicerina, especialmente con metanol, requiere la adición de costosos paquetes de aditivos a la mezcla. Y aunque el costo de la glicerina ahora es más bajo que el costo de los glicoles, el paquete de aditivos para fabricar fluidos de transferencia de calor de glicerina de calidad es más costoso que el paquete de aditivos para anticongelante a base de etilenglicol y propilenglicol. ¡Y si el costo del anticongelante de glicerina en el mercado es más bajo que el del glicol, significa que el fabricante simplemente ahorró en calidad y no agregó los costosos aditivos necesarios al producto!
Por lo tanto, la elección depende del comprador: o un refrigerante confiable y probado basado en glicoles, o un "pig in a poke" de glicerina.
La elección de nuestra empresa, como la mayoría de los principales fabricantes de anticongelantes, es fundamentalmente inequívoca: la glicerina no se puede usar en su forma pura, ¡pero mezclada con metanol es peligrosa y criminal!
El principal argumento que confirma nuestra posición sobre este tema es que, en cualquier instalación importante y grande, ¡los estándares existentes NO ESTÁN PERMITIDOS en el uso de glicerina en los sistemas de calefacción y refrigeración!
MEG
El etilenglicol es un producto de la hidratación del óxido de etileno en presencia de ácido sulfúrico o fosfórico. Se refiere a alcoholes polihídricos. No se congela a bajas temperaturas y baja el punto de congelación del agua. Capaz de absorber agua del aire.
Se comercializa en bidones metálicos y plásticos, hasta 227 litros. Así como cubos de plástico de 1000l.
Es necesario almacenar la sustancia en un recipiente sellado de aluminio o acero con protección anticorrosión en un almacén cerrado sin calefacción. La vida útil para el grado más alto es de 12 meses, para el primer grado: 3 años a partir de la fecha de producción.
Nombre del indicador Norma
Aspecto, olor Líquido transparente e incoloro de textura aceitosa. Sin olor.
Soluble en agua, alcoholes, tolueno, benceno
Densidad 1.112 g/cm?.
Punto de fusión 12,9 grados centígrados
Punto de ebullición 197,3 grados centígrados
Solicitud
Debido a su capacidad para bajar el punto de congelación, el monoetilenglicol se utiliza en la producción de anticongelantes y líquido de frenos para automóviles, así como en la fabricación de celofán y poliuretano. En menor medida, se utiliza en la producción de tintas y tintas de impresión.
Nivel de riesgo
Se refiere a sustancias combustibles. La autoignición ocurre a una temperatura de 380 grados, un destello de vapor cuando se calienta a 120 grados. Tóxico. No se permite la ingestión. Los vapores son menos dañinos.
Glicerol
Fórmula química: HOCH2CH(OH)CH2OH
Nombre internacional: Glicerina
NO CAS: 56-81-5
Calificación: Diablillo. "h", GOST 6259-75
Apariencia: líquido transparente e inodoro
Embalaje: Latas de 25 kg, bidones de 250 kg, cubos de 1500
Condiciones de almacenaje: en una habitación seca ventilada a baja temperatura
Sinónimos: 1,2,3-trioxipropano
Ofrecemos Glicerina en latas, barriles, cubos a precios competitivos.
| Especificación | |
| Peso molecular | 92.10 |
| Sustancia básica, no menos de | 99,5% (real 99,8%) |
| Contenido de cenizas, no más | 0,01 % (en realidad menos del 0,1 %) |
| Contenido de agua, no más | 0,5% (de hecho 0,1%) |
| Contenido de cloruros, no más | 0,001 % |
| Contenido de sulfato, no más | 0,002 % |
| Metales pesados, no más | 0.0005% (en realidad menos de 0.00005%) |
| Compuestos de cloro (como CL), no más | 0,003 % |
| Arsénico, no más | 0.00015% (real menos de 0.00001%) |
| Color (APHA), no más | 20 (en realidad menos de 10) |
La glicerina es un líquido incoloro, higroscópico, viscoso, inodoro y de sabor dulce. Miscible en cualquier proporción con agua, etanol, metanol, acetona, insoluble en cloroformo y éter. Cuando el glicerol se mezcla con agua, se libera calor y se produce la contracción (reducción de volumen). Cuando el glicerol interactúa con ácidos hidrohálicos o haluros de fósforo, se forman mono o dihalohidrinas; con ácidos inorgánicos y carboxílicos - ésteres completos e incompletos, con deshidratación - acroleína. El glicerol se puede oxidar y, dependiendo de las condiciones y la naturaleza del agente oxidante, se puede obtener gliceraldehído, ácido glicérico, ácido tartrónico, dihidroxiacetona, ácido mesoxalico. La glicerina se encuentra en grasas y aceites naturales como triglicéridos mixtos de ácidos carboxílicos.
Solicitud La glicerina se usa ampliamente • en la industria farmacéutica, por ejemplo para la producción de nitroglicerina, ungüentos medicinales; • en la industria alimentaria, por ejemplo en la producción de licores, confitería; • en la industria cosmética, en la fabricación de perfumes y cosméticos, • en la producción de resinas de gliptal; • como suavizante para telas, cuero, papel; • como componente de emulsionantes, anticongelantes, lubricantes, betunes para zapatos, jabones y adhesivos, • como materia prima en la producción de polialcoholes, que se utilizan en diversas espumas. • como plastificante para celofán, etc.
¿A qué temperatura se congela el agua en las tuberías de calefacción de un edificio residencial?
Si la temperatura en la casa permanece -10 durante varios días y hay agua en las tuberías, entonces se puede congelar, lo que provocará la ruptura de las tuberías. Muchos probablemente han visto baterías de calefacción modernas con función de drenaje de agua. Casi todas las baterías modernas están equipadas con la capacidad de drenar el agua. Esto se hace para que, en caso de emergencia, cuando la temperatura en la casa sea de -10, el agua no se congele y no rompa las tuberías. Si la situación ha llegado a esto, nos solidarizamos mucho con usted, lo más probable es que tenga que cambiar las baterías, ya que durante la congelación del agua, probablemente se hayan producido microgrietas que hagan que el funcionamiento de estas baterías sea peligroso.
¿Por qué el agua puede congelarse en las tuberías? Si durante la temporada de calefacción, justo cuando las baterías se están llenando de agua, se produce una avería y el agua se enfría, y la temperatura exterior desciende rápidamente, esto puede provocar la congelación de las tuberías.
Ya respondimos la pregunta a qué temperatura se congela el agua, como experimento, tome un vaso pequeño, llénelo hasta la mitad con agua y póngalo en el congelador durante varias horas, dos horas son suficientes para que el agua se convierta parcialmente en hielo.
El agua es una de las sustancias más esenciales en nuestro planeta. Tiene un montón de propiedades que lo hacen, hasta cierto punto, único. Una de las propiedades más famosas que incluso un niño pequeño conoce es la congelación del agua.Se sabe que 0 grados centígrados es la temperatura de cristalización del agua. Pero no todo es tan simple. Consideraremos algunas de las sutilezas de este proceso más adelante.

Densidad de la solución de glicerina a 25
La media aritmética de las densidades de alcohol y glicerol.
209.4. 1.047. 25.265.0. 1.060. ... Ver cuál es la Densidad de las soluciones acuosas de glicerina en otros diccionarios Archivo E236 Ácido fórmico.svg Fórmula estructural del ácido fórmico Ácido fórmico El ácido metanoico es el primero ...
¿Cuál es la densidad de la glicerina a 17 grados centígrados?
8
Densidad a 25 C, g cm. ... Una solución de glicerina a una concentración del 25% o más no expone la contaminación microbiana, en soluciones más diluidas, los microorganismos se multiplican bien en ella.
3,14
¿Qué líquido tiene mayor densidad, la glicerina o el alcohol? explique
Ssss
TK-abril en el sitio en toda Rusia. Concentración, densidad e índice de refracción de soluciones de glicerol 15 С. … 1.0594. 1.3633. 25.1.0620.
Calcular la masa molar de ambas sustancias. Para el alcohol, es menor (92 g/mol frente a 46 g/mol para el alcohol), y la densidad es correspondientemente menor. Cuando se trata de alcohol etílico.
¿Cuál es el punto de tales preguntas? La información se encuentra en los motores de búsqueda.
La media aritmética de las densidades de los componentes de la mezcla.
Determinar qué masa de glicerol con una densidad de 1.26 g ml se debe tomar para preparar una solución acuosa c.42. ... 111 g de anhídrido ftálico y 46 g de glicerina con una densidad de 28 V se colocan en un vaso de precipitados de vidrio con una capacidad de 0,25 l.
¿Cómo calcular la densidad y la viscosidad de un líquido que contiene agua, alcohol y glicerina?
Para esto, se venden reómetros. no tienes que contar nada. solo congela
trietilenglicol. propilenglicol. Glicerol. … propilenglicol 40%. -25 C. ... La densidad de soluciones acuosas de etilenglicol a varias temperaturas.
Necesita saber el porcentaje de todos los componentes de la mezcla (¡al menos!)
De ninguna manera. Es, buscar datos recibidos por alguien.
Por favor ayuda, ¿flotará un trozo de hielo en gasolina, queroseno, glicerina? ¿Por qué?
Estará en glicerina, no flota en el whisky, la densidad es casi la misma que la gasolina.
También aumenta la densidad de la solución final y mejora la calidad de las burbujas. ... Solución de glicerina botella de 25gTula Pharmaceutical Factory LLC. … Solución de tetraborato de sodio en vial de glicerina 20 % 30 g, Samara FF, Samara Rusia.
El hielo es menos denso que el aceite, así será.
Compara la densidad del hielo con la densidad de estos líquidos. si la densidad del hielo es menor, entonces flotará; si es mayor, se hundirá.
No lo sé. depende de que pieza. si hay suficiente aire en el hielo para mantenerlo en la superficie, flotará, y si no, no lo hará. Inténtalo tú mismo. el queroseno es barato.
Dependiendo de a qué temperatura se enfría este hielo
El punto de ebullición de las soluciones acuosas de glicerina disminuye con la disminución de la concentración de glicerol con un contenido de agua del 5%, el punto de ebullición es 160-161, su densidad es 1,26362 g cm3. … 25 25 C . ZnCl2.
Nunca he visto hielo flotando en el tanque de gasolina y el bote. Y ciertamente lo es))). Así que probablemente esté en el fondo. Vi glicerina solo en un vial y en calor))).
¡Oye!
X cantidad de glicerol diluido, g A densidad de glicerol destilado, g ml ... Las soluciones de glicerol a una concentración del 25% y superior no están sujetas a contaminación microbiana, las soluciones más diluidas son ...
¿Flotará un trozo de hielo en gasolina, queroseno, glicerina?
¡Averigua la densidad y listo!
Densidad de soluciones acuosas de alcoholes. Se dan densidades de soluciones acuosas g cm3 a 20 C para las siguientes sustancias: etanol, 1-propanol, 2-propanol, etilenglicol, glicerol, D-manitol.
Sí)))
Si la densidad del hielo es menor que la densidad del líquido, entonces el hielo flotará
¿Cuál es la densidad de la glicerina a una temperatura de 24 gr. ¿CON?
Glicerina Grados Celsius020406080100120140169180Densidad g/cm3126712591250123812241208118811631126
Para una temperatura de 24 grados = determinar por interpolación entre 20 y 40 grados
Calcule el punto de ebullición de una solución al 8% de glicerol C3H6O3 en acetona. La respuesta es 57.7oC. 4.Una solución, 100 ml de los cuales contienen 2,3 g ... Tome la densidad de la solución igual a uno. Respuesta 608 Pa. Boleto 14 25 1. ¿Cuántos gramos de BaCl2 · 2H2O...
Preguntas sobre Química))) Y Física. ¿Qué líquido es más denso que el agua y también conduce la electricidad pero no el metal?
Glicerina, glicoles de etileno, formamidas, butirolactona, casi todos los ácidos, aminas. y mucho más.
Concentración de ácido sulfúrico, % en masa. Densidad a 25 C, g cm.... 25,60-0,1950 0,000 8 - humedad relativa,% - índice de refracción de una solución acuosa de glicerol a 25 C para línea D sodio - temperatura de la solución, C ...