Trebam li uzemljiti grijanu šipku za ručnike
Prvo morate znati da uzemljenje (izgradnja uzemljenja vlastitim rukama) nije potrebno ako:
- 1. Koristite električnu grijaću ručnika (takve grijane držače za ručnike obično su opremljene posebnim utikačima u kojima se nalazi žica za uzemljenje, sve je to spojeno na utičnicu, a same utičnice moraju već biti spojene na petlju za uzemljenje) .
- 2. Živite u privatnoj kući ili stanu i imate zaseban sustav grijanja.
Uzemljenje grijane šipke za ručnike je obavezno u sljedećim slučajevima:
- 1. Ako je vaša sušilica spojena na sustav grijanja plastičnom cijevi. Unutar metalno-plastične cijevi nalazi se aluminij, koji provodi električnu struju: na spojevima gdje se nalaze armature, električni krug je prekinut. U skladu s tim, takav grijani držač za ručnike mora biti spojen na petlju za uzemljenje ili na uspon tople vode.
- 2. Ako je vaš sustav tople vode izrađen od plastičnih cijevi.
Kako uzemljiti grijanu šipku za ručnike
Sve električne grijače za ručnike, kao što je gore spomenuto, spojene su na uzemljenu utičnicu, dok takve sušilice imaju žicu za uzemljenje s posebnim kontaktom na utikaču. Budući da se grijane držače za ručnike obično ugrađuju u kupaonicu, trebali biste pregledati utičnicu na koju će se spojiti. Takav izlaz mora biti u posebnoj zaštitnoj kutiji koja sprječava ulazak vlage u sam izlaz.
Postoje 2 glavna načina za uzemljenje grijane šipke za ručnike:
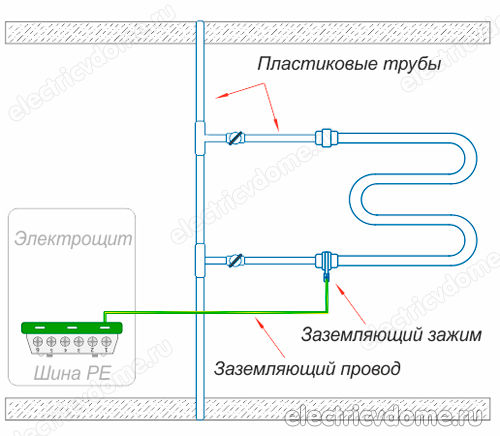
- 1. Pomoću sustava za izjednačavanje potencijala, koji se mora instalirati ručno, uzemljite ovaj sustav na zajedničku masu električne ploče. To treba učiniti ako se umjesto metalnih komunikacija u kući ili stanu koriste komunikacije izrađene od polimera (metalno-plastične cijevi).
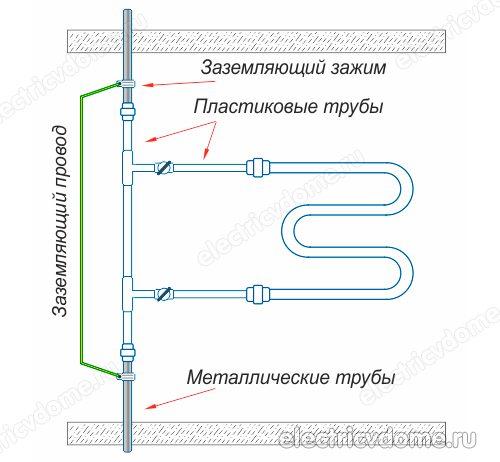
- 2. Izravno uzemljenje cijevi tijela grijane tračnice za ručnike s konvencionalnom žicom na čelični uspon.
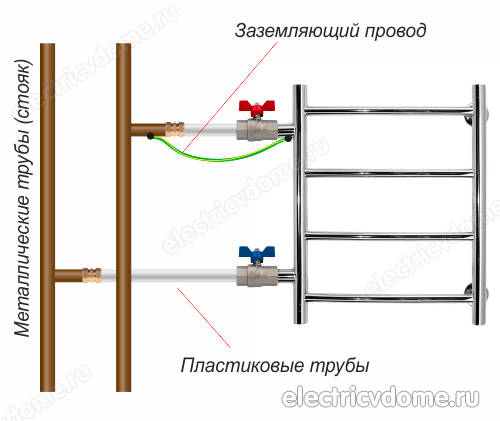
Da biste izvršili uzemljenje grijane tračnice za ručnike na drugi način, prvo morate nabaviti stezaljku, nakon što s nje uklonite sve izolacijske materijale. Ova stezaljka mora imati terminal za spajanje žice. Zatim je stezaljka pričvršćena na cijev grijanog tijela nosača ručnika.
Uzima se obična bakrena žica, koja bi trebala imati presjek od 4 mm2. Ova žica je s jedne strane spojena na stezaljku, njen drugi kraj mora biti spojen ili na masu električne ploče ili na čelični uspon. Osim toga, ne zaboravite spojiti druge uređaje u vašoj kupaonici na petlju za uzemljenje.
| Takve metode ne zahtijevaju puno vremena za njihovu provedbu, ali zauzvrat dobivaju dug i neprekidan rad grijane držače za ručnike, a u budućnosti pitanje "kako uzemljiti grijanu šipku za ručnike" neće uzrokovati poteškoće. |
Prijatelji također gledaju video o tome što vam je potrebno za uzemljenje grijane šipke za ručnike.
Povezani sadržaji na stranici:
- O uzemljivanju jednostavnim riječima
- Zašto je kupka uzemljena?
- Dizajn uređaja za uzemljenje
Uzroci elektrokorozije
Pojava Foucaultovih vrtložnih struja prilično je složen i nepredvidiv fenomen. U sustavima opskrbe toplom vodom, a ponekad i u sustavu grijanja, takve se struje pojavljuju zbog mnogih razloga koji se čine nepovezanim.
Općenito, vrtložne struje nastaju s razlikom potencijala. Prilikom gradnje kuće sve metalne konstrukcije spojene su na zajedničku petlju uzemljenja, a ranije su u izgradnji koristili uzemljenje duž petlje, ali sada su zadovoljni metodom izjednačavanja potencijala.
Kada se plastični sustavi ugrađuju u stan umjesto postojećeg metalnog sustava, razlika potencijala nastaje zbog puknuća uzemljenja (npr. na grijanoj vodilici za ručnike postoji jedan potencijal, a na usponu potpuno drugi). Otuda i razlika potencijala, dakle zalutale struje. Mogu se pojaviti i kao posljedica kratkog spoja, nedostatka uzemljenja obližnjih električnih kućanskih aparata, bilo da se radi o perilici rublja i tako dalje.
Čak i prisutnost/odsutnost tramvajskih pruga u neposrednoj blizini igra ulogu. Zalutale struje također se javljaju kada je došlo do kršenja izolacije električnog ožičenja, prekida mreže ili uzemljenja u sustavu grijanja.
Sve to dovodi do električne korozije vodovoda, također je uzrokovana blizinom dva različita materijala, posebice nehrđajućeg i crnog čelika. Mjesto kroz koje naboj prolazi u grijanu šipku za ručnike, kao rezultat toga, prolazi kroz elektrokemijsku reakciju, pa se tamo događa oštećenje. Takvi se problemi obično rješavaju izravnim uzemljenjem same grijane držače ručnika.
Prilikom kupnje vodene grijane vodilice za ručnike potrebno je upoznati se s pravilima njezina rada, posebno obratiti pozornost na to je li potrebno uzemljiti grijaću držač za ručnike ili ne, kako biste tu točku uzeli u obzir tijekom popravak, a ne nakon dovršetka popravka
Zašto mljeti vodilicu za ručnike
Nakon što su plastične cijevi počele zamjenjivati obične metalne, počeli su ignorirati njihovo uzemljenje, pogrešno vjerujući da metalna cijev i metalno-plastična cijev imaju istu električnu vodljivost. Ovo nije istina. Nema kontakta između metalno-plastične cijevi i aluminija: nisu spojeni.
Praksa pokazuje da 90 posto grijanih držača za ručnike počinje propuštati upravo u slučaju zamjene metalnih sustava tople vode s njihovim plastičnim kolegama (na primjer, polipropilenom). Stare metalne cijevi zamjenjuju se modernim plastičnim kako bi se smanjile vrtložne struje. Međutim, korozija se i dalje pokazuje.
Prvi simptomi električne korozije su pojava mrlja hrđe na grijanoj vodilici za ručnike, a hrđa se pojavljuje čak i na uređajima od nehrđajućeg čelika. Općenito, svi metalni električni proizvodi u dodiru s vodom podložni su i elektrokemijskoj i galvanskoj koroziji. Elektrokorozija nastaje u prisutnosti lutajućih struja. Kao rezultat toga, metal je istovremeno izložen električnoj struji i vodi, nakon čega se pojavljuju kvarovi metala, a odatle se počinje širiti korozija.
Kada dva različita metala dođu u dodir, od kojih je jedan reaktivniji od drugog, oba metala ulaze u kemijsku reakciju. Čista voda je vrlo loš vodič električne struje (dielektrik), ali zbog velike koncentracije raznih nečistoća voda se pretvara u svojevrsni elektrolit.
Ne zaboravite da temperatura ima veliki utjecaj na električnu vodljivost: što je temperatura vode viša, to bolje provodi struju. Ovaj fenomen je poznat kao "galvanska korozija", ona je ta koja metodično čini grijanu držaču za ručnike neupotrebljivom.
Potreba za antikorozivnom zaštitom
Zaštita metala od utjecaja koji destruktivno djeluju na njegovu površinu jedan je od glavnih zadataka ljudi koji rade s mehanizmima, jedinicama i strojevima, brodovima i građevinskim procesima.

Što se uređaj ili dio aktivnije koristi, veća je vjerojatnost da će biti izložen destruktivnim učincima atmosferskih uvjeta, tekućina s kojima se susrećemo tijekom rada.Mnoge grane znanosti i industrijske proizvodnje rade na zaštiti metala od korozije, ali glavne metode ostaju nepromijenjene i sastoje se u stvaranju zaštitnih premaza:
- metal;
- nemetalni;
- kemijski.
Nemetalni premazi su stvoreni pomoću organskih i anorganskih spojeva, njihov princip rada je prilično učinkovit i razlikuje se od drugih vrsta zaštite. Za stvaranje nemetalne zaštite u industrijskoj i građevinskoj proizvodnji koriste se boje i lakovi, beton i bitumen te visokomolekularni spojevi, koji se posebno aktivno usvajaju posljednjih godina, kada je kemija polimera dosegla velike visine.

Kemija je pridonijela stvaranju zaštitnih premaza metodama:
- oksidacija (stvaranje zaštitnog filma na metalu pomoću oksidnih filmova);
- fosfatiranje (fosfatni filmovi);
- nitriranje (zasićenje površine čelika dušikom);
- cementiranje (spojevi s ugljikom);
- plaviti (spojevi s organskim tvarima);
- promjena sastava metala uvođenjem antikorozivnih aditiva u njega);
- modifikacija okolnog korozivnog okoliša uvođenjem inhibitora koji na njega utječu.
Elektrokemijska zaštita od korozije je proces obrnut od elektrokemijske korozije. Ovisno o pomaku potencijala metala na pozitivnu ili negativnu stranu, razlikuju se anodna i katodna zaštita. Spajanjem protektora ili izvora istosmjerne struje na metalni proizvod stvara se katodna polarizacija na metalnoj površini koja sprječava uništavanje metala kroz anodu.
Metode elektrokemijske zaštite sastoje se od dvije mogućnosti:
- metalna prevlaka je zaštićena drugim metalom, koji ima negativniji potencijal (odnosno zaštitni metal je manje stabilan od onog koji se štiti), a to se naziva eloksiranjem;
- premaz se nanosi od manje aktivnog metala, a tada je i naziva se katodnim.

Anodna zaštita od korozije je, na primjer, pocinčano željezo. Dok se sav cink iz zaštitnog sloja ne potroši, željezo će biti relativno sigurno.
Katodna zaštita je nikliranje ili bakreno prevlačenje. U tom slučaju uništavanje zaštitnog sloja dovodi do uništenja sloja koji štiti. Postavljanje zaštitnika za zaštitu metalnog proizvoda ne razlikuje se od reakcije u drugim slučajevima. Zaštitnik djeluje kao anoda, a ono što je pod njegovim protektoratom ostaje netaknuto, koristeći za to stvorene uvjete.
Što je korozija
Proces razaranja gornjeg sloja metalnog materijala pod utjecajem vanjskih utjecaja naziva se korozijom u širem smislu.

Pojam korozija u ovom slučaju je samo karakteristika činjenice da metalna površina ulazi u kemijsku reakciju i pod njezinim utjecajem gubi svoja izvorna svojstva.
4 glavna znaka po kojima možete utvrditi da ovaj proces postoji:
- proces koji se razvija na površini i na kraju prodire u metalni proizvod;
- reakcija nastaje spontano iz činjenice da je poremećena stabilnost termodinamičke ravnoteže između okoline i sustava atoma u slitini ili monolitu;
- kemija ovaj proces ne doživljava samo kao reakciju uništenja, već kao reakciju redukcije i oksidacije: pri ulasku u reakciju neki atomi zamjenjuju druge;
- svojstva i karakteristike metala tijekom takve reakcije podliježu značajnim promjenama, ili se gube tamo gdje se dogodi.
Metode zaštite metala
Elektrokemijska korozija jedna je od glavnih prepreka na putu ljudskog djelovanja. Zaštita od utjecaja destruktivnih procesa i njihova strujanja na površini konstrukcija i konstrukcija jedan je od trajnih i hitnih zadataka svake industrijske proizvodnje i bilo koje kućne aktivnosti osobe.

Razvijeno je nekoliko metoda takve zaštite, a sve se aktivno koriste u svakodnevnom životnom ciklusu:
- Elektrokemijska zaštita - elektrolitička prema principu rada, korištenjem kemijskih zakona, štiti metal pomoću anode, katode i gaznoga sloja.
- Obrada elektroiskrim primjenom raznih instalacija - beskontaktnih, kontaktnih, anodno-mehaničkih.
- Prskanje električnim lukom glavna je prednost u debljini nanesenog sloja i relativnoj jeftinosti postupka.
- Učinkovita antikorozivna obrada je uklanjanje onečišćenja i čišćenje tretirane površine, nakon čega slijedi nanošenje antikorozivnog i zatim dodatnog zaštitnog sloja na površinu.
Sve ove metode razvijene su u procesu ljudskog djelovanja u svrhu zaštite alata, vozila i transporta na spoju nekoliko industrijskih sektora, a korištenjem znanstvenih dostignuća.
Elektrokemijska korozija, koja je prirodni proces uništavanja metalne površine pod utjecajem neutralnih ili agresivnih čimbenika okoliša, složen je problem. Gubitke od toga trpe strojogradnja, transport i industrijska poduzeća, vozila. A to je problem koji zahtijeva svakodnevno rješavanje.
Vrste korozije
Ovisno o vrsti metala i redoks reakciji koja se s njim događa, korozija može biti:
- ujednačen ili neujednačen;
- lokalno i točka (neke su sekcije iz nekog razloga reagirale, dok druge nisu);
- ulcerozni, također poznat kao pitting;
- podzemni;
- pucanje;
- interkristalni, koji nastaju duž granica metalnog kristala.
Također, ovisno o tome kakvi vanjski čimbenici utječu na površinu, korozija može biti kemijska i elektrokemijska. Kemijska korozija nastaje kao rezultat nekih reakcija pod utjecajem kemijskih interakcija, ali bez sudjelovanja električne struje, a može biti čak i svojstvena nafti i plinu. Elektrokemijski se razlikuje po određenim procesima, složeniji je od kemijskog.

Na videu: korozija metala.
Uzroci i znakovi elektrokemijske korozije
Elektrokemijska korozija se razlikuje od kemijske korozije po tome što se proces uništavanja odvija u elektrolitskom sustavu, što uzrokuje nastanak električne struje unutar ovog sustava. Dva konjugirana procesa, anodni i katodni, dovode do uklanjanja nestabilnih atoma iz kristalne rešetke metala. Tijekom anodnog procesa ioni prelaze u otopinu, a elektroni iz anodnog procesa padaju u zamku oksidirajuće tvari i vežu ih depolarizator.
Dakle, depolarizacija je uklanjanje slobodnih elektrona s katodnih mjesta, a depolarizator je tvar koja je odgovorna za ovaj proces. Glavne reakcije odvijaju se uz sudjelovanje vodika i kisika kao depolarizatora.
Brojni su primjeri elektrokemijske korozije raznih vrsta, koja u prirodi i pod utjecajem različitih uvjeta utječe na metalne površine. Vodik djeluje u kiseloj sredini, dok kisik djeluje u neutralnoj.
Gotovo svi metali podliježu elektrokemijskoj koroziji, a na temelju toga su podijeljeni u 4 skupine, određuje se vrijednost njihovog elektrodnog potencijala:
- aktivni korodiraju čak iu okruženju u kojem nema oksidacijskih sredstava;
- srednje aktivni ulaze u reakciju oksidacije u kiseloj sredini;
- neaktivni ne reagiraju u odsutnosti oksidacijskih sredstava u neutralnom i kiselom okruženju;
- ne reagiraju - visoka stabilnost (plemeniti metali, paladij, zlato, platina, iridij).
Ali ista reakcija može se odvijati i u vodi, u otopinama baza, soli i kiselina. U visokospecijaliziranoj razlici atmosferske korozije, tla i prozračivanja razlikuju se morska i biološka (nastaje pod utjecajem bakterija).
Postoji čak i električna korozija, koja nastaje pod utjecajem električne struje, a rezultat je lutajućih struja koje nastaju tamo gdje električnu struju koristi osoba za obavljanje određenih aktivnosti.
U tom slučaju dolazi do uništenja homogene metalne površine zbog termodinamičke nestabilnosti u okolišu. I heterogena - zbog sastava kristalne rešetke, u kojoj se atomi jednog metala drže čvršće od atoma stranih inkluzija.Te se reakcije razlikuju po brzini ionizacije iona i redukciji oksidativnih komponenti okoliša.
Uništavanje metalnih površina tijekom elektrokemijske korozije sastoji se u istovremenoj pojavi dvaju procesa: anodnog i katodnog, a razlike između procesa su u tome što se otapanje događa na anodama koje su u dodiru s okolinom kroz mnoge mikroelektrode koje su dio površine bilo kojeg metala i zatvorena sam za sebe.