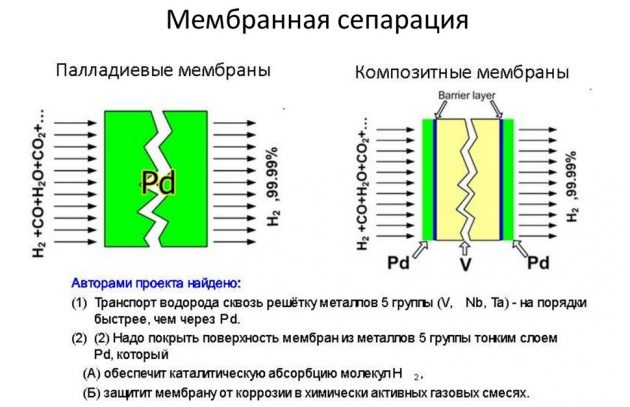
Módszerek hidrogén előállítására ipari körülmények között
Kivonás metán-átalakítással
. Az 1000 Celsius fokra előmelegített elpárologtatott vizet nyomás alatt és katalizátor jelenlétében metánnal keverik össze. Ez a módszer érdekes és bevált, azt is meg kell jegyezni, hogy folyamatosan fejlesztik: új, olcsóbb és hatékonyabb katalizátorok keresése folyik.
Fontolja meg a hidrogén előállításának legősibb módszerét - szénelgázosítás
. Levegő hozzáférés és 1300 Celsius fokos hőmérséklet hiányában a szén és a vízgőz felmelegszik. Így a hidrogén kiszorul a vízből, és szén-dioxid keletkezik (a hidrogén felül lesz, a szintén a reakció eredményeként kapott szén-dioxid pedig alul). Ez lesz a gázelegy szétválasztása, minden nagyon egyszerű.
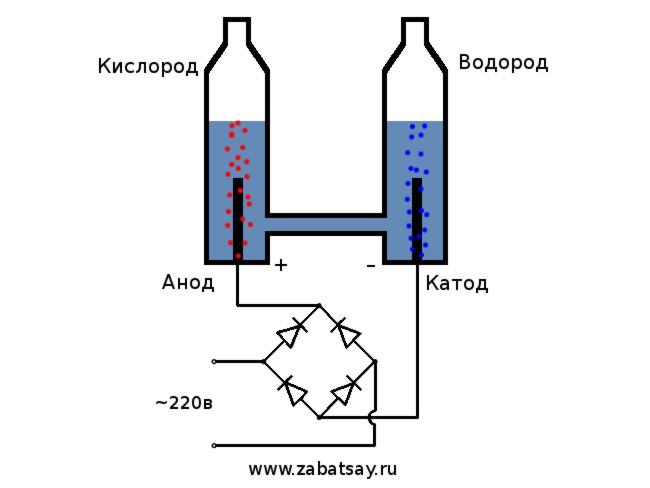
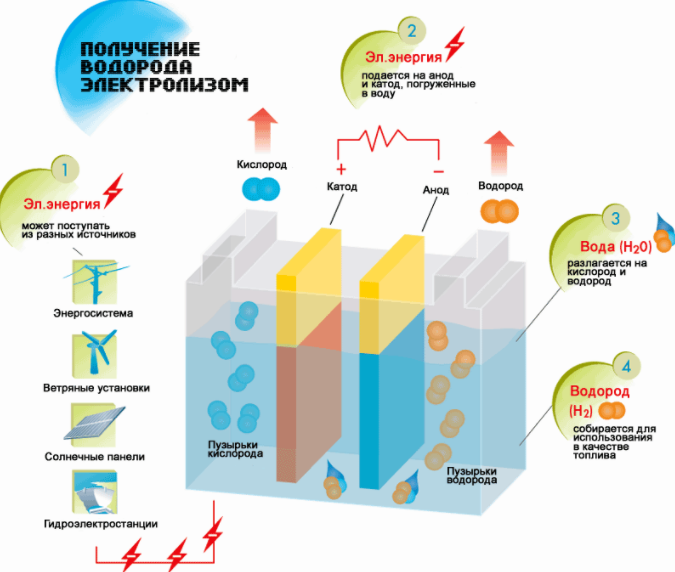
Hidrogén kinyerése azáltal víz elektrolízis
legegyszerűbb lehetőségnek tartották. A megvalósításhoz szódaoldatot kell önteni a tartályba, és két elektromos elemet kell elhelyezni. Az egyik pozitív töltésű (anód), a másik negatívan (katód). Áram esetén a hidrogén a katódra, az oxigén pedig az anódra kerül.
Hidrogén kinyerése a módszer szerint részleges oxidáció
. Ehhez alumínium és gallium ötvözetet használnak. Vízbe kerül, ami a reakció során hidrogén és alumínium-oxid képződéséhez vezet. A gallium szükséges a reakció teljes lejátszódásához (ez az elem nem teszi lehetővé az alumínium idő előtti oxidációját).
A közelmúltban vált jelentőségre biotechnológiák felhasználási módja
: oxigén- és kénhiány esetén a chlamydomonas intenzív hidrogént kezd kibocsátani. Nagyon érdekes hatás, amelyet jelenleg aktívan tanulmányoznak.
Ne feledkezzünk meg egy másik régi, bevált hidrogén-előállítási módszerről sem, ami a másfajta felhasználás lúgos elemek
és vizet. Ez a technika elvileg a szükséges biztonsági intézkedések mellett laboratóriumi körülmények között is megvalósítható. Így a reakció során (hevítéskor és katalizátorokkal megy végbe) fém-oxid és hidrogén képződik. Már csak össze kell gyűjteni.
Szerezzen be hidrogént a víz és a szén-monoxid kölcsönhatásai
csak ipari környezetben lehetséges. Szén-dioxid és hidrogén képződik, elválasztásuk elvét fentebb ismertettük.
A TALÁLMÁNYNAK A KÖVETKEZŐ ELŐNYÖK RENDELKEZIK
A gázok oxidációjából nyert hő közvetlenül a helyszínen hasznosítható, a hidrogént és oxigént pedig a kipufogó gőz és az ipari víz ártalmatlanításából nyerik.
Alacsony vízfogyasztás áram- és hőtermelés során.
A módszer egyszerűsége.
Jelentős energiamegtakarítás, mint csak arra költik, hogy az önindítót állandó hőmérsékletűre melegítsék.
Magas folyamattermelékenység, mert a vízmolekulák disszociációja tizedmásodpercekig tart.
A módszer robbanás- és tűzbiztonsága, mert megvalósítása során nincs szükség tartályokra a hidrogén és az oxigén összegyűjtésére.
A berendezés működése során a víz többször megtisztul, desztillált vízzé alakul. Ezzel kiküszöbölhető a csapadék és a vízkő, ami növeli a berendezés élettartamát.
A telepítés közönséges acélból készül; a hőálló acélból készült kazánok kivételével béléssel és falak árnyékolásával. Vagyis nincs szükség speciális drága anyagokra.
A találmány alkalmazható lehet
Az ipart az erőművek szénhidrogén- és nukleáris üzemanyagának olcsó, széles körben elterjedt és környezetbarát vízzel való helyettesítésével, ezen erőművek teljesítményének megőrzése mellett.
KÖVETELÉS
Módszer hidrogén és oxigén előállítására vízgőzből
, amely magában foglalja ennek a gőznek az elektromos mezőn való átvezetését, azzal jellemezve, hogy túlhevített vízgőzt használnak 500-550 o C
nagyfeszültségű egyenáramú elektromos mezőn áthaladva a gőz disszociációja és hidrogén- és oxigénatomokra való szétválasztása.
Régóta szerettem volna valami ilyesmit csinálni. De az akkumulátorral és egy pár elektródával végzett további kísérletek nem értek el. Egy teljes értékű berendezést szerettem volna készíteni hidrogén előállítására, mennyiségben a léggömb felfújása érdekében. Mielőtt egy teljes értékű készüléket készítene a víz elektrolíziséhez otthon, úgy döntöttem, hogy mindent megnézek a modellen.
Az elektrolizátor általános sémája így néz ki.
Ez a modell nem alkalmas teljes napi használatra. De az ötletet tesztelték.
Ezért az elektródákhoz úgy döntöttem, hogy grafitot használok. Az elektródák számára kiváló grafitforrás a trolibusz áramgyűjtő. Rengetegen hevernek belőlük a végállomásokon. Emlékeztetni kell arra, hogy az egyik elektróda megsemmisül.
Fűrészelés és kikészítés reszelővel. Az elektrolízis intenzitása az áram erősségétől és az elektródák területétől függ.
Az elektródákhoz vezetékek vannak rögzítve. A vezetékeket gondosan szigetelni kell.
A műanyag palackok nagyon alkalmasak az elektrolizáló modell testére. A fedélben lyukak vannak kialakítva a csövek és vezetékek számára.
Minden gondosan be van vonva tömítőanyaggal.
A levágott palacknyak két tartály összekapcsolására alkalmas.
Össze kell kötni őket, és meg kell olvasztani a varratot.
A dió palackkupakból készül.
Két palack alján lyukak vannak kialakítva. Minden össze van kötve és gondosan megtöltve tömítőanyaggal.
Feszültségforrásként 220V-os háztartási hálózatot fogunk használni. Szeretném figyelmeztetni, hogy ez egy meglehetősen veszélyes játék. Tehát, ha nincs elegendő készség, vagy kétségek merülnek fel, akkor jobb, ha nem ismételjük meg. A háztartási hálózatban váltóáram van, elektrolízishez ki kell egyenesíteni. A diódahíd tökéletes erre. A képen látható nem volt elég erős, és gyorsan kiégett. A legjobb megoldás a kínai MB156 diódahíd volt alumínium tokban.
A diódahíd nagyon felforrósodik. Aktív hűtést igényel. A számítógép processzorának hűtője tökéletesen illeszkedik. Az esethez megfelelő méretű forrasztódobozt használhat. Elektromos árukban értékesítik.
A diódahíd alá több réteg kartont kell helyezni.
A szükséges lyukakat a forrasztódoboz fedelében készítik el.
Így néz ki az összeszerelt egység. Az elektrolizátort a hálózatról, a ventilátort egy univerzális áramforrásról táplálják. A szódabikarbóna oldatát elektrolitként használják. Itt emlékezni kell arra, hogy minél nagyobb az oldat koncentrációja, annál nagyobb a reakciósebesség. De ugyanakkor a fűtés magasabb. Ezenkívül a katódon a nátrium bomlásának reakciója hozzájárul a melegítéshez. Ez a reakció exoterm. Ennek eredményeként hidrogén és nátrium-hidroxid képződik.
A fenti képen látható készülék nagyon forró volt. Időnként ki kellett kapcsolni, és meg kellett várni, amíg kihűl. A fűtés problémáját részben az elektrolit hűtése oldotta meg. Ehhez egy asztali szökőkút pumpát használtam. Egy hosszú cső fut egyik palackból a másikba egy szivattyún és egy vödör hideg vízen keresztül.
Ennek a kérdésnek a relevanciája ma meglehetősen nagy, mivel a hidrogén felhasználási köre rendkívül kiterjedt, és tiszta formájában gyakorlatilag nem található meg a természetben. Éppen ezért számos módszert dolgoztak ki ennek a gáznak más vegyületekből kémiai és fizikai reakciókkal történő kinyerésére. Ez az, amit ebben a cikkben tárgyalunk.
Hidrogéntermelés a háztartásban
Elektrolitikus cella választása
A ház elemének megszerzéséhez speciális készülékre van szükség - elektrolizátorra.Az ilyen berendezésekre számos lehetőség kínálkozik a piacon, a készülékeket ismert technológiai cégek és kis gyártók egyaránt kínálják. A márkás egységek drágábbak, de a felépítésük minősége magasabb.
A háztartási készülék kis méretű és könnyen használható. Főbb részletei a következők:
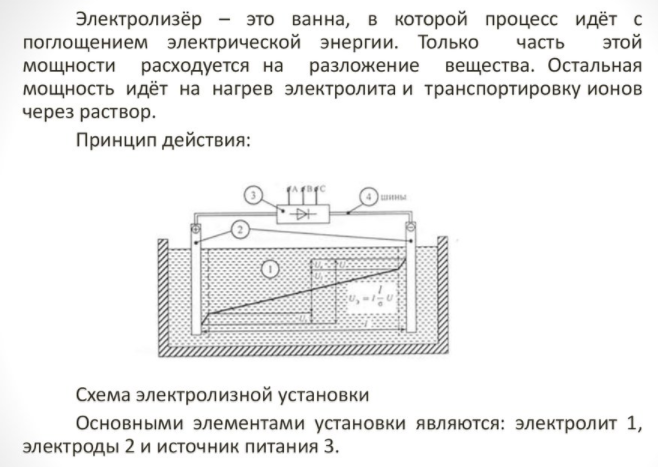
- reformátor;
- tisztító rendszer;
- üzemanyagcellák;
- kompresszor berendezések;
- hidrogén tároló tartály.
Nyersanyagként egyszerű csapvizet vesznek, az elektromos áram pedig egy közönséges konnektorból származik. A napelemes egységek villamos energiát takarítanak meg.
Az "otthoni" hidrogént fűtési vagy főzési rendszerekben használják. Dúsítják a levegő-üzemanyag keveréket is, hogy növeljék az autómotorok teljesítményét.
A készülék készítése saját kezűleg
Még olcsóbb, ha saját kezűleg otthon készíti el a készüléket. A száraz cella úgy néz ki, mint egy lezárt tartály, amely két elektródalapból áll egy tartályban elektrolitoldattal. A World Wide Web számos sémát kínál a különböző modellek összeszerelésére:
- két szűrővel;
- a tartály felső vagy alsó elrendezésével;
- két vagy három szeleppel;
- horganyzott táblával;
- az elektródákon.
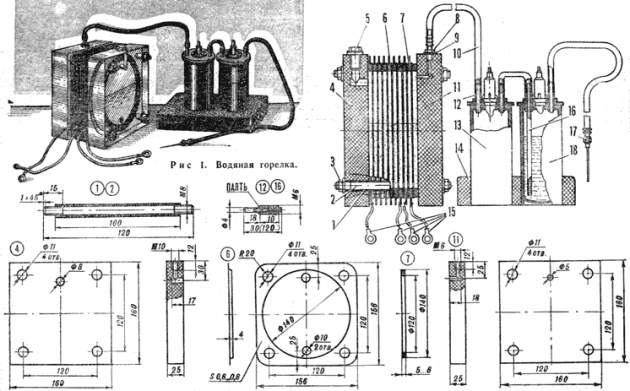
Egy egyszerű berendezés hidrogén előállítására könnyen létrehozható. Szükség lesz hozzá:
- rozsdamentes acéllemez;
- átlátszó cső;
- szerelvények;
- műanyag tartály (1,5 l);
- vízszűrő és visszacsapó szelep.
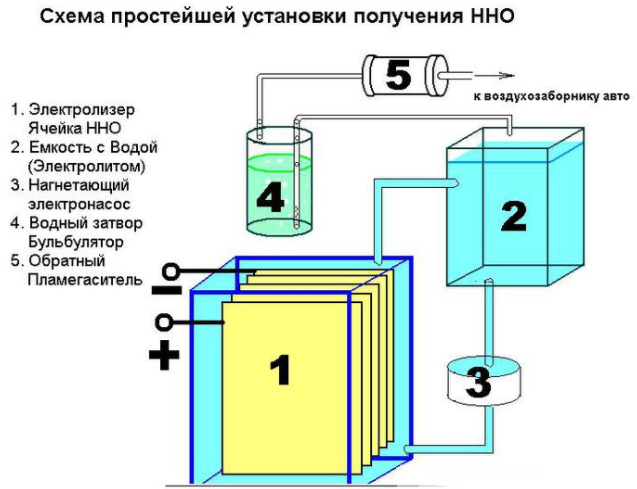
Ezenkívül különféle hardverekre lesz szükség: anyák, alátétek, csavarok. Mindenekelőtt 16 négyzet alakú rekeszre kell vágnia a lapot, és mindegyikből vágnia kell egy sarkot. A vele szemben lévő sarokban lyukat kell fúrni a lemezek csavarozásához. Az állandó áram biztosítása érdekében a lemezeket a következő séma szerint kell csatlakoztatni: plusz-mínusz-plusz-mínusz. Ezeket az alkatrészeket egymástól csővel, a csatlakozásnál csavarral és alátétekkel (a lemezek között három darab) választják el. 8 tányér kerül a pluszra és a mínuszra.
Megfelelő összeszerelés esetén a lemezek szélei nem érintik az elektródákat. Az összegyűjtött részeket egy műanyag edénybe engedik le. A falak érintkezési helyén két rögzítőlyuk van csavarokkal. Szereljen be biztonsági szelepet a felesleges gáz eltávolításához. A szerelvények a tartály fedelébe vannak szerelve, és a varratok szilikonnal vannak lezárva.
Eszköz tesztelése
Az eszköz teszteléséhez hajtson végre több műveletet:
- Töltse fel folyadékkal.
- Fedővel letakarva csatlakoztassa a cső egyik végét a szerelvényhez.
- A másodikat leengedik a vízbe.
- Csatlakoztassa az áramforráshoz.
Miután csatlakoztatta a készüléket a konnektorhoz, néhány másodperc múlva észrevehető lesz az elektrolízis folyamata és a csapadék.
A tiszta víznek nincs jó elektromos vezetőképessége. A mutató javítása érdekében alkáli-nátrium-hidroxid hozzáadásával elektrolitikus oldatot kell készíteni. Olyan kompozíciókban található, amelyek olyan csövek tisztítására szolgálnak, mint a "Mole".
A hidrogén előállításának módszerei
A hidrogén színtelen és szagtalan gáznemű elem, amelynek sűrűsége a levegőhöz viszonyítva 1/14. Ritkán található szabad állapotban. Általában a hidrogént más kémiai elemekkel kombinálják: oxigénnel, szénnel.
Az ipari szükségletek és energia hidrogéntermelését többféle módszerrel végzik. A legnépszerűbbek a következők:
- víz elektrolízis;
- koncentrációs módszer;
- alacsony hőmérsékletű kondenzáció;
- adszorpció.
A hidrogén nem csak gáz- vagy vízvegyületekből izolálható. A hidrogént fa és szén magas hőmérsékletnek kitéve, valamint biohulladék feldolgozásával állítják elő.
Az energetikai célú atomi hidrogént egy molekuláris anyag termikus disszociációjának módszerével állítják elő platinából, volfrámból vagy palládiumból készült huzalon. Hidrogén környezetben, 1,33 Pa-nál kisebb nyomáson melegítik.A radioaktív elemeket hidrogén előállítására is használják.
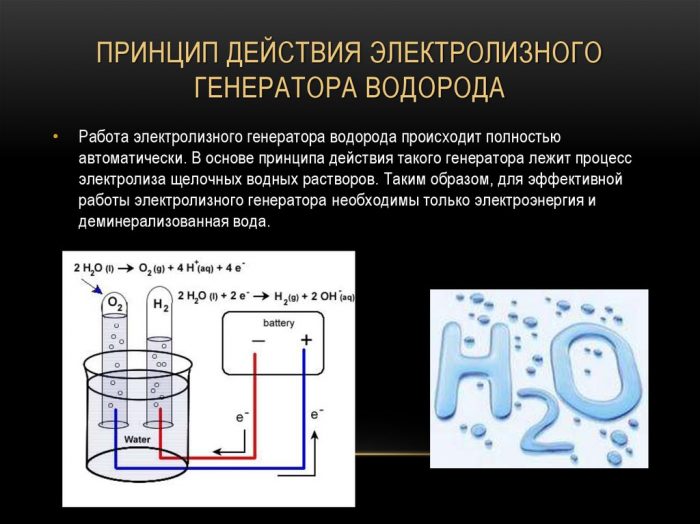
elektrolízis módszer
A hidrogénkivonás legegyszerűbb és legnépszerűbb módszere a vízelektrolízis. Lehetővé teszi gyakorlatilag tiszta hidrogén előállítását. A módszer további előnyei a következők:
- nyersanyagok elérhetősége;
- nyomás alatt lévő elem beszerzése;
- a folyamat automatizálásának lehetősége a mozgó alkatrészek hiánya miatt.
A folyadék elektrolízissel történő felosztása a hidrogén égésének fordítottja. Lényege, hogy egyenáram hatására a vizes elektrolit oldatba mártott elektródákon oxigén és hidrogén szabadul fel.
További előnyt jelent az ipari értékű melléktermékek előállítása. Így az oxigén nagy mennyiségben szükséges az energiaszektor technológiai folyamatainak katalizálásához, a talaj és víztestek tisztításához, valamint a háztartási hulladékok ártalmatlanításához. Az elektrolízissel előállított nehézvizet az energiaipar atomreaktorokban használják fel.
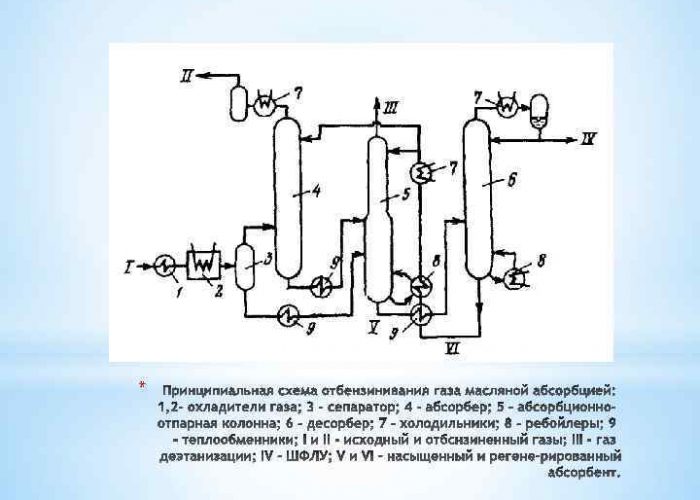
Hidrogén előállítása koncentrálással
Ez a módszer egy elem elválasztásán alapul az azt tartalmazó gázkeverékektől. Így az ipari mennyiségben előállított anyag legnagyobb részét metán gőzreformálásával nyerik ki. Az így előállított hidrogént az energetikában, az olajfinomításban, a rakétaiparban, valamint a nitrogénműtrágyák előállítására használják fel. A H2 megszerzésének folyamata különböző módon történik:
- rövid ciklus;
- kriogén;
- membrán.
Ez utóbbi módszer a leghatékonyabb és olcsóbb.
Kondenzáció alacsony hőmérsékleten
A H2 előállításának ez a technikája a gázvegyületek nyomás alatti erős hűtése. Ennek eredményeként kétfázisú rendszerré alakulnak, amelyet ezt követően egy szeparátor választ el folyékony komponensre és gázra. A hűtéshez folyékony közeget használnak:
- víz;
- cseppfolyósított etán vagy propán;
- folyékony ammónia.
Ez az eljárás nem olyan egyszerű, mint amilyennek látszik. A szénhidrogéngázokat egyszerre nem lehet majd tisztán elkülöníteni. Az alkatrészek egy része az elválasztó kamrából vett gázzal távozik, ami nem gazdaságos. A probléma megoldható az alapanyag mélyhűtésével az elválasztás előtt. De ehhez sok energia kell.
Az alacsony hőmérsékletű kondenzátorok modern rendszereiben metánmentesítő vagy etánmentesítő oszlopok is rendelkezésre állnak. Az utolsó elválasztási szakaszból a gázfázis eltávolításra kerül, és a folyadék a hőcsere után a nyersgázárammal a desztillációs oszlopba kerül.
Adszorpciós módszer
Az adszorpció során adszorbenseket használnak a hidrogén felszabadítására - szilárd anyagok, amelyek felszívják a gázkeverék szükséges összetevőit. Adszorbensként aktív szenet, szilikátgélt, zeolitokat használnak. Ennek a folyamatnak a végrehajtásához speciális eszközöket használnak - ciklikus adszorbereket vagy molekulaszitákat. Nyomás alatt alkalmazva ezzel a módszerrel a hidrogén 85 százaléka visszanyerhető.
Ha összehasonlítjuk az adszorpciót az alacsony hőmérsékletű kondenzációval, akkor az eljárás - átlagosan 30 százalékkal - alacsonyabb anyag- és üzemeltetési költséget láthatjuk. Az adszorpciós módszerrel hidrogént állítanak elő energia és oldószerek felhasználásával. Ez a módszer lehetővé teszi a H2 90 százalékának kinyerését a gázelegyből és a végtermék előállítását 99,9%-os hidrogénkoncentrációig.