Kas lemia jūros vandens druskingumą
Matyti šiek tiek aukštesnę figūrą 3,5 ppm
, galite pamanyti, kad tai yra bet kurio jūros vandens mūsų planetoje konstanta. Tačiau viskas nėra taip paprasta, druskingumas priklauso nuo regiono. Taip atsitiko, kad kuo toliau į šiaurę regionas yra, tuo ši vertė didesnė.
Priešingai, pietuose gali pasigirti ne tokia sūri jūra ir vandenynai. Žinoma, visos taisyklės turi savo išimčių. Druskos kiekis jūrose paprastai yra šiek tiek mažesnis nei vandenynuose.
Koks apskritai yra geografinis padalijimas? Nežinoma, tyrinėtojai tai laiko savaime suprantamu dalyku, yra visko. Galbūt atsakymo reikėtų ieškoti ankstesniuose mūsų planetos vystymosi laikotarpiuose. Ne tuo metu, kai gimė gyvybė – daug anksčiau.
Jau žinome, kad vandens druskingumas priklauso nuo:
- magnio chloridas.
- natrio chloridas.
- kitos druskos.
Galbūt kai kuriose žemės plutos vietose šių medžiagų telkiniai buvo kiek didesni nei gretimuose regionuose. Kita vertus, jūros srovių niekas neatšaukė, anksčiau ar vėliau bendras lygis turėjo susilyginti.
Taigi, greičiausiai, nedidelis skirtumas yra susijęs su mūsų planetos klimato ypatumais. Ne pati nepagrįstiausia nuomonė, jei prisimenate šalčius ir svarstote, ką būtent vanduo su dideliu druskos kiekiu užšąla lėčiau.
Užšalimo etapai
Labai įdomu stebėti, kaip užšąla jūros vanduo. Jis nėra iš karto padengtas vienoda ledo pluta, kaip gėlas vanduo. Daliai pavirtus ledu (o jis šviežias), likusi dalis dar labiau sūroka, o užšalimui reikalingas dar stipresnis šerkšnas.
Ledo rūšys
Jūrai vėsstant susidaro įvairių tipų ledas:
- sniego audra;
- dumblas;
- adatos;
- Salo;
- nilas.
Jei jūra dar neužšalusi, bet yra labai arti jos ir tuo metu iškrenta sniegas, liesdamasis su paviršiumi jis netirpsta, o prisisotina vandens ir sudaro klampią purią masę, vadinamą sniegu. Sušalusi ši košė virsta dumblu, kuris labai pavojingas į audrą patekusiems laivams. Dėl to denis akimirksniu pasidengia ledo pluta.
Kai termometras pasiekia užšalimui būtiną žymę, jūroje pradeda formuotis ledo adatos – kristalai labai plonų šešiakampių prizmių pavidalu. Surinkę juos tinkleliu, nuplovę druską ir išlydę, pamatysite, kad jie neriebūs.
Kai dar labiau atšąla, riebalai pradeda stingti ir suformuoja ledo plutą, skaidrią ir trapią kaip stiklas. Toks ledas vadinamas nilas, arba buteliukas. Jis sūrus, nors susidaro iš neraugintų spyglių. Faktas yra tas, kad užšalimo metu adatos užfiksuoja mažiausius aplinkinio sūraus vandens lašus.
Tik jūrose yra toks reiškinys kaip plaukiojantis ledas. Jis atsiranda todėl, kad vanduo čia greičiau atšąla prie kranto. Ten susidaręs ledas užšąla iki pakrantės krašto, todėl buvo vadinamas greituoju ledu. Ramiu oru stiprėjant šalčiui, jis greitai užfiksuoja naujas teritorijas, kartais siekia keliasdešimt kilometrų. Tačiau vos tik pakyla stiprus vėjas, greitas ledas pradeda skilti į įvairaus dydžio gabalus. Šios ledo sangrūdos, dažnai didžiulės (ledo laukai), vėjo ir srovės neša per visą jūrą, todėl laivams kyla problemų.
Jūros vandens gėlinimas.
Kalbant apie gėlinimą, visi bent šiek tiek girdėjo, kai kurie dabar net prisimena filmą „Vandens pasaulis“. Kiek realu kiekviename name pastatyti vieną tokį nešiojamąjį distiliatorių ir visiems laikams pamiršti žmonijos geriamojo vandens problemą? Vis dar fikcija, o ne tikrovė.
Viskas dėl sunaudojamos energijos, nes efektyviam darbui reikia didžiulių pajėgumų, ne mažesnių nei branduolinis reaktorius. Šiuo principu veikia gėlinimo gamykla Kazachstane.Idėja buvo pateikta ir Kryme, tačiau Sevastopolio reaktoriaus galios tokiems tūriams nepakako.
Prieš pusę amžiaus, prieš daugybę branduolinių nelaimių, dar buvo galima manyti, kad taikus atomas pateks į visus namus. Buvo net šūkis. Tačiau jau aišku, kad branduoliniai mikroreaktoriai nenaudojami:
- Buitiniuose prietaisuose.
- Pramonės įmonėse.
- Automobilių ir lėktuvų konstrukcijoje.
- Ir taip, miesto ribose.
Kitame amžiuje nesitikima. Mokslas gali imtis dar vieno šuolio ir mus nustebinti, tačiau kol kas tai tik nerūpestingų romantikų fantazijos ir viltys.
Distiliuoto vandens užšalimo temperatūra
Ar distiliuotas vanduo užšąla? Prisiminkite, kad vanduo užšaltų, jame turi būti tam tikri kristalizacijos centrai, kurie gali būti oro burbuliukai, suspenduotos dalelės, taip pat pažeisti indo, kuriame jis yra, sieneles.
Distiliuotas vanduo, visiškai neturintis jokių priemaišų, neturi kristalizacijos branduolių, todėl jo užšalimas prasideda labai žemoje temperatūroje. Pradinė distiliuoto vandens užšalimo temperatūra yra -42 laipsniai. Mokslininkams pavyko pasiekti distiliuoto vandens peršalimą iki -70 laipsnių.
Vanduo, kuris buvo veikiamas labai žemoje temperatūroje, bet nesikristalizavo, vadinamas „peršaldymu“. Galite įdėti distiliuoto vandens butelį į šaldiklį, pasiekti hipotermiją ir tada pademonstruoti labai veiksmingą triuką - žiūrėkite vaizdo įrašą:
Švelniai bakstelėję į išimtą iš šaldytuvo butelį arba įmetę į jį nedidelį ledo gabalėlį, galite parodyti, kaip akimirksniu jis virsta ledu, kuris atrodo kaip pailgi kristalai.
Distiliuotas vanduo: ar ši išgryninta medžiaga užšąla, ar ne veikiama slėgio? Toks procesas įmanomas tik specialiai sukurtomis laboratorinėmis sąlygomis.
ÑаÑÑолÑемпеÑаÑÑÑа
- ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Δ¶¶Ð ð ð ð Ð Ð ΔÐ Ð ð ð ð Ð ΔÐ Ð ð ð Ð Ð Ð ΔÐ Ð Ð Ð Ð Ð ð Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δ ° сср²ð¾ñð ° ñвÐμÐ »Ð¸ ÑиÑÑÑ. РРРРРРРРв Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ° Ð ° ° ° ° ñññ Ð ÐμÐ ð ð ð ð ð Ðμ ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð ñ »Ð ²Ðððð ооо²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² ²Ð Ð DND »D ÑоÐ'ÐμÑжР° ниÐμ Ñол D в ND ° ÑÑоР»Ðμ мÐμнÑÑÐμ, ÑÐμм ÑÑÐμÐ ± ÑÐμмоÐμ Ð'л N ÑвÑÐμкÑиÑÐμÑкого ND ° ÑÑвоÑÐ °, воÐ'Ð ° ÑÑкоÑÐ¸Ñ Ð¾Ð * ¸ оÑлажденÑÑаиоиии Veikia ñðμμððμð½ððμðμð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð 𠸸ив ° ° ÐµÑ ÐºÐ¾Ð½ÑенÑÑаÑÐ¸Ñ Ñоии оÑалÑном ѾаÑ. Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð -
Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð - O Ð Ð Ð Ð Ð Ð μñ DD ° мÐμÑÐ · Ð ° РниÐμ ÑвÑÐμкÑиÑÐμÑкого ND ° ÑÑвоÑÐ ° ā ÑÑо пÑоÑÐμÑÑ Ñ NND ° ÑÑиÐμм ÑкÑÑÑой ÑÐμпР»Ð¾ÑÑ, поÑÑÐ¾Ð¼Ñ ÑÐμмпÐμÑÐ ° ÑÑÑÐ ° оÑÑÐ ° ÐμÑÑÑ Ð½ÐμиР· менной. РРРРРРРРРРРРРРРРРРРРв ¿Ñипонижении - - O Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ¸ поÑÑоÑннойDD ° ннÑй пÑоÑÐμÑÑ Ð¿ÑимÐμнÑÐμÑÑÑ Ð² пР»Ð ° Ð ÑÑинÑÐ ° nnn иÑпР° ÑиÑÐμл NN пÑи NND ° нÑпоÑÑиÑовкÐμ пÑоÐ'ÑкÑов .
- ¸Ñ и ÑлоÑида наÑÑиÑ. Ð Ð Ð сср²ð²Ð¾¾ ñÐ »Ð¾¾Ð¸Ð'Ð ° кР° ð» ññ𸸠п¿Ðμгð¾ и¸Ð¿Ð³ð¾ и¸Ð¿Ð¾Ð »ñÐ · срμсссс в п¿Ð¾Ð¼ññл Ðμннññ п¿Ð½¾¾ÐμññÐ ° п¿Ð½Ðμñ ° ¸ замоÑаживании пÑодÑкÑов.. 17.8 °С. ... Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 °C Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð Ð Ð Ð Ð Ð Ð Ð ² · A Ð ð ð ð ð ð ð Ð Ð ¿ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðððððððððððððððððð tion вР° ñ ссср¾ссрºÐ¸Ð¹ п¿Ð¾Ð'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ ¼ Ðð ð ð ð ð ð ð ð ð ð ð ð ð Ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð сссряр½ср °ÐºÑ ÑаÑÑооа ÑоÑлаждаемÑм пÑодÑкÑом.
Ð Ð ° сср²ð²Ð¾ ñÐ »Ð¾¾Ð¸Ð'Ð ° Ð½ð ° ñ ооой ñол н) нÐμ по¾¾¾¸ пи¸ÐμÐ LTL²ñÐμ п¿Ð¾Ð'ñкñññ.. о¾ÐÐÐ Ð ° Ð ð ð ð Ðñððð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð РоÐμ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° - Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð в 1 °С. Ð Ð Ð Ð Ð Ð Ð Ð Ð 2 Ð Ð ·
VANDENS CIKLAS PASAULIO VANDENYNE
Poliariniuose regionuose vanduo, atvėsęs, tampa tankesnis ir grimzta į dugną. Iš ten jis lėtai slenka link pusiaujo. Todėl visose platumose gilūs vandenys yra šalti. Netgi ties pusiauju dugno vandenyse temperatūra siekia tik 1–2 laipsnius virš nulio.
Kadangi srovės neša šiltą vandenį iš pusiaujo į vidutinio klimato platumas, šaltas vanduo iš gelmių kyla labai lėtai, kad užimtų savo vietą. Paviršiuje jis vėl sušyla, eina į subpolines zonas, kur atvėsta, nugrimzta į dugną ir vėl juda dugnu iki pusiaujo.
Taigi, vandenynuose vyksta savotiškas vandens ciklas: paviršiuje vanduo juda iš pusiaujo į subpolines zonas ir vandenynų dugnu – iš subpoliarinių zonų į pusiaują. Šis vandens maišymosi procesas kartu su kitais aukščiau minėtais reiškiniais sukuria vandenynų vienybę.
Jei radote klaidą, pažymėkite teksto dalį ir spustelėkite Ctrl + Enter
.
Skiltyje apie tai, kokią žemiausią įprastos (valgomosios, NaCl) druskos vandens-druskos tirpalo temperatūrą galima pasiekti, pateikia autorius Europos
geriausias atsakymas yra Į vandenį įpylus druskos, ledo tirpimo greitis didėja, o ledo lydymosi temperatūra nukrenta žemiau. Taip yra todėl, kad pridėjus druskos susilpnėja molekulinė sanglauda ir sunaikinamos ledo kristalinės gardelės. Ledo-druskos mišinio tirpimas vyksta pašalinant šilumą iš aplinkos, dėl to aplinkinis oras atvėsta ir jo temperatūra mažėja. Didėjant druskos kiekiui ledo ir druskos mišinyje, jo lydymosi temperatūra mažėja. Druskos tirpalas, kurio lydymosi temperatūra yra žemiausia, vadinamas eutektiku, o jo lydymosi temperatūra – kriohidrato tašku. Ledo ir druskos mišinio su valgomąja druska kriohidrato temperatūra yra -21,2°C, o druskos koncentracija tirpale yra 23,1% visos mišinio masės, o tai yra maždaug 30 kg druskos 100 kg druskos. ledas.Toliau didėjant druskos koncentracijai, tai ne ledo ir druskos mišinio lydymosi temperatūros mažėjimas, o lydymosi temperatūros padidėjimas (esant 25% druskos koncentracijai tirpale nuo bendros masės, lydymosi temperatūra pakyla iki -8 °C).Šaldant kriohidrato tašką atitinkančios koncentracijos valgomosios druskos vandeninį tirpalą, gaunamas homogeninis ledo ir druskos kristalų mišinys, vadinamas eutektiniu kietu tirpalu.Eutektinės kietos medžiagos tirpalo lydymosi temperatūra. natrio chlorido yra -21,2 ° C, o lydymosi šiluma yra 236 kJ / kg. Eutektinis tirpalas naudojamas aušinimui be sukimo momento. Norėdami tai padaryti, eutektinis valgomosios druskos tirpalas supilamas į nulius - sandariai uždarytas formas - ir jos užšaldomos. Sušalusiais nuliais šaldomi prekystaliai, spintelės, šaldomi nešiojamieji šaltkrepšiai ir pan.(atidarei buitinio šaldytuvo šaldiklį – tokį konteinerį rasite) Prekyboje aušinimas ledu-drusku buvo plačiai naudojamas iki masinės įrangos gamybos. su mašinos aušinimu.
Atsakymas iš išdžiūti
žemiausia temperatūra iš bet kurios temperatūros yra absoliutus nulis, apie -273 laipsniai Celsijaus
Atsakymas iš Olya
temperatūra priklauso nuo druskos koncentracijos tirpale, kuo didesnė koncentracija, tuo žemesnė užšalimo temperatūra. žinynas kurį laiką iš manęs buvo atimtas)), bet jei remsimės tuo, kad jūros vanduo yra druskos tirpalas, galime daryti išvadą, kad užšalimo temperatūra yra daug žemesnė nei nulis .... laipsnių -15-20
Atsakymas iš galintis
22,4 % NaCl vandeninis tirpalas užšąla 21,2 °C temperatūroje
į klausimą Vandeninis NaCl tirpalas "kristalizacijos temperatūra"
Atsakymas iš Jergėjus Neznamovas
10.8 lentelė. NaCl tirpalo užšalimo temperatūraNaCl kiekis, g 100 g vandens 5 - -4,4 9,0 - -5,4 10,6 - -6,4 12,3 - -7,5 14,0 - -8,6 15,7 - -9,8 17,5 - -11,0 19,2 - 1,6 .3 - - 15,1 25,0 - - 16,0 26,9 - -18,2 29,0 - -20,0 30,1 - -21,2
Sūrus vandens užšalimo temperatūra
Eksperimentai su ledu vaikams visada įdomūs. Atlikdamas eksperimentus su Vladu, aš padariau net keletą atradimų sau.
Šiandien rasime atsakymus į šiuos klausimus:
- Kaip vanduo elgiasi užšalęs?
- Kas atsitiks, jei užšaldysite sūrų vandenį?
- kailis sušildys ledą?
- ir kai kurie kiti…
užšalęs vanduo

Ar sūrus vanduo užšąla?
Kuo sūresnis vanduo, tuo žemesnė užšalimo temperatūra. Eksperimentui paėmėme dvi stiklines – vienoje gėlo vandens (pažymėta raide B), kitoje labai sūraus vandens (pažymėto raidėmis B + C).
Visą naktį išstovėjus šaldiklyje sūrus vanduo nesušalo, o stiklinėje susidarė ledo kristalai. Gėlas vanduo virto ledu. Kol aš manipuliavau puodeliais ir druskos tirpalais, Vladikas sukūrė savo neplanuotą eksperimentą.
Į puodelį įpylė vandens, augalinio aliejaus ir atsargiai įdėjo į šaldiklį. 
Sūrus vanduo šaldiklyje neužšalo, bet kas atsitiks, jei ant ledo pabarstysite druskos? Patikrinkime.
Patirtis su ledu ir druska
Paimkite du ledo kubelius. Vieną iš jų pabarstykite druska, o antrą palikite palyginimui. 
Užšaldome didelį varveklą ir apibarstom druska, paėmėme šepetėlius ir 
Mūsų patyręs kūrybiškumas vienija visą šeimą, todėl Makaruškino rašiklis pateko į fotoaparato objektyvą!
Makaras ir Vladas yra labai visi mėgsta sušalti
. Kartais šaldiklyje atsiduria visiškai netikėti daiktai.
Nuo vaikystės svajojau padaryti šią patirtį, tačiau mama neturėjo kailinių, o daugelis

Kaip puiku būti suaugusiam, turėti kailinį ir daryti visokius vaikiškus eksperimentus!
Jūsų Galina Kuzmina
Lentelėje pateiktos kalcio chlorido CaCl 2 tirpalo termofizinės savybės, priklausomai nuo temperatūros ir druskos koncentracijos: tirpalo savitoji šiluma, šilumos laidumas, vandeninių tirpalų klampumas, jų šiluminis difuziškumas ir Prandtl skaičius. Druskos CaCl 2 koncentracija tirpale yra nuo 9,4 iki 29,9%. Temperatūra, kuriai esant suteikiamos savybės, nustatoma pagal druskos kiekį tirpale ir svyruoja nuo -55 iki 20°C.
kalcio chloridas CaCl 2 negali užšalti iki minus 55°С
. Šiam efektui pasiekti druskos koncentracija tirpale turi būti 29,9%, o jos tankis – 1286 kg/m 3 .
Didėjant druskos koncentracijai tirpale, didėja ne tik jo tankis, bet ir tokios termofizinės savybės kaip vandeninių tirpalų dinaminė ir kinematinė klampumas, taip pat Prandtl skaičius. Pavyzdžiui, dinaminis CaCl 2 tirpalo klampumas
esant 9,4% druskos koncentracijai 20°C temperatūroje yra 0,001236 Pa s, o kalcio chlorido koncentracijai tirpale padidėjus iki 30%, jo dinaminis klampumas padidėja iki 0,003511 Pa s.
Reikia pažymėti, kad temperatūra turi didžiausią įtaką šios druskos vandeninių tirpalų klampumui. Kai kalcio chlorido tirpalas atšaldomas nuo 20 iki -55°C, jo dinaminis klampumas gali padidėti 18 kartų, o kinematinis – 25 kartus.
Atsižvelgiant į tai CaCl 2 tirpalo termofizinės savybės
:
- , kg / m 3;
- užšalimo temperatūra °С;
- dinaminis vandeninių tirpalų klampumas, Pa s;
- Prandtl numeris.
ÑаÑÑолÑемпеÑаÑÑÑа
- ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Δ¶¶Ð ð ð ð Ð Ð ΔÐ Ð ð ð ð Ð ΔÐ Ð ð ð Ð Ð Ð ΔÐ Ð Ð Ð Ð Ð ð Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δ ° сср²ð¾ñð ° ñвÐμÐ »Ð¸ ÑиÑÑÑ. РРРРРРРРв Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ° Ð ° ° ° ° ñññ Ð ÐμÐ ð ð ð ð ð Ðμ ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð ñ »Ð ²Ðððð ооо²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² ²Ð Ð DND »D ÑоÐ'ÐμÑжР° ниÐμ Ñол D в ND ° ÑÑоР»Ðμ мÐμнÑÑÐμ, ÑÐμм ÑÑÐμÐ ± ÑÐμмоÐμ Ð'л N ÑвÑÐμкÑиÑÐμÑкого ND ° ÑÑвоÑÐ °, воÐ'Ð ° ÑÑкоÑÐ¸Ñ Ð¾Ð * ¸ оÑлажденÑÑаиоиии Veikia ñðμμððμð½ððμðμð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð 𠸸ив ° ° ÐµÑ ÐºÐ¾Ð½ÑенÑÑаÑÐ¸Ñ Ñоии оÑалÑном ѾаÑ.Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð -
Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð - O Ð Ð Ð Ð Ð Ð μñ DD ° мÐμÑÐ · Ð ° РниÐμ ÑвÑÐμкÑиÑÐμÑкого ND ° ÑÑвоÑÐ ° ā ÑÑо пÑоÑÐμÑÑ Ñ NND ° ÑÑиÐμм ÑкÑÑÑой ÑÐμпР»Ð¾ÑÑ, поÑÑÐ¾Ð¼Ñ ÑÐμмпÐμÑÐ ° ÑÑÑÐ ° оÑÑÐ ° ÐμÑÑÑ Ð½ÐμиР· менной. РРРРРРРРРРРРРРРРРРРРв ¿Ñипонижении - - O Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ¸ поÑÑоÑнной DD ° ннÑй пÑоÑÐμÑÑ Ð¿ÑимÐμнÑÐμÑÑÑ Ð² пР»Ð ° Ð ÑÑинÑÐ ° nnn иÑпР° ÑиÑÐμл NN пÑи NND ° нÑпоÑÑиÑовкÐμ пÑоÐ'ÑкÑов .
- ¸Ñ и ÑлоÑида наÑÑиÑ. Ð Ð Ð сср²ð²Ð¾¾ ñÐ »Ð¾¾Ð¸Ð'Ð ° кР° ð» ññ𸸠п¿Ðμгð¾ и¸Ð¿Ð³ð¾ и¸Ð¿Ð¾Ð »ñÐ · срμсссс в п¿Ð¾Ð¼ññл Ðμннññ п¿Ð½¾¾ÐμññÐ ° п¿Ð½Ðμñ ° ¸ замоÑаживании пÑодÑкÑов.. 17.8 °С. ... Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 °C Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð Ð Ð Ð Ð Ð Ð Ð ² · A Ð ð ð ð ð ð ð Ð Ð ¿ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðððððððððððððððððð tion вР° ñ ссср¾ссрºÐ¸Ð¹ п¿Ð¾Ð'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ'ñÐ ¼ Ðð ð ð ð ð ð ð ð ð ð ð ð ð Ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð сссряр½ср °ÐºÑ ÑаÑÑооа ÑоÑлаждаемÑм пÑодÑкÑом.
Ð Ð ° сср²ð²Ð¾ ñÐ »Ð¾¾Ð¸Ð'Ð ° Ð½ð ° ñ ооой ñол н) нÐμ по¾¾¾¸ пи¸ÐμÐ LTL²ñÐμ п¿Ð¾Ð'ñкñññ.. о¾ÐÐÐ Ð ° Ð ð ð ð Ðñððð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð РоÐμ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° - Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð в 1 °С. Ð Ð Ð Ð Ð Ð Ð Ð Ð 2 Ð Ð ·
Kokioje temperatūroje gali užšalti jūros vanduo?
Tačiau pagrindinis klausimas dar neatsakytas. Jau sužinojome, kad druska lėtina vandens užšalimą, jūrą ledo pluta pasidengs ne esant nuliui, o minusinei temperatūrai. Tačiau kiek termometro rodmenys turėtų nueiti iki minuso, kad pajūrio regionų gyventojai išeidami iš namų negirdėtų įprasto banglenčių garso?
Norint nustatyti šią vertę, yra speciali formulė, sudėtinga ir suprantama tik specialistams. Tai priklauso nuo pagrindinio rodiklio - druskingumo lygis
. Bet kadangi turime vidutinę šio rodiklio reikšmę, ar galime rasti ir vidutinį užšalimo tašką? Žinoma.
Jei jums nereikia visko skaičiuoti iki šimtosios dalies, tam tikram regionui, prisiminti –1,91 laipsnio temperatūrą
.
Gali atrodyti, kad skirtumas nėra toks didelis, tik du laipsniai. Bet per sezoninius temperatūrų svyravimus tai gali suvaidinti didžiulį vaidmenį ten, kur termometro stulpelis nukrenta bent 0. Būtų tik 2 laipsniais vėsiau, tos pačios Afrikos ar Pietų Amerikos gyventojai galėtų matyti ledą prie kranto, bet deja. Tačiau nemanome, kad tokia netektis juos labai nuliūdino.
NaCl tirpalo termofizinės savybės
Lentelėje parodytos natrio chlorido NaCl tirpalo termofizinės savybės, priklausomai nuo temperatūros ir druskos koncentracijos. Natrio chlorido NaCl koncentracija tirpale yra nuo 7 iki 23,1%. Pažymėtina, kad aušinant vandeninį natrio chlorido tirpalą, jo savitoji šiluminė talpa šiek tiek pakinta, sumažėja šilumos laidumas, didėja tirpalo klampumas.
Atsižvelgiant į tai NaCl tirpalo termofizinės savybės
:
- tirpalo tankis, kg/m 3;
- užšalimo temperatūra °С;
- savitoji (masės) šiluminė talpa, kJ/(kg deg.);
- šilumos laidumo koeficientas, W/(m deg);
- dinaminis tirpalo klampumas, Pa s;
- kinematinė tirpalo klampa, m 2 /s;
- šiluminis difuziškumas, m 2 /s;
- Prandtl numeris.
Iš ko pagamintas jūros vanduo?
Kuo jūros turinys skiriasi nuo gėlo vandens? Skirtumas nėra toks didelis, bet vis tiek:
- Daug daugiau druskos.
- Vyrauja magnio ir natrio druskos.
- Tankis skiriasi nežymiai, per kelis procentus.
- Vandenilio sulfidas gali susidaryti gylyje.
Pagrindinis jūros vandens komponentas, kad ir kaip nuspėjamai tai skambėtų, yra vanduo. Tačiau skirtingai nei upių ir ežerų vanduo, tai yra daug natrio ir magnio chloridų
.
Apskaičiuota, kad druskingumas yra 3,5 ppm, bet, kad būtų aiškiau, - 3,5 tūkstantosios procento visos sudėties.
Ir net ši, ne pati įspūdingiausia figūra, vandeniui suteikia ne tik specifinio skonio, bet ir padaro jį negeriamu. Absoliučių kontraindikacijų nėra, jūros vanduo nėra nuodas ar toksiška medžiaga, ir iš poros gurkšnių nieko blogo nenutiks. Apie pasekmes bus galima kalbėti, jei žmogus bus bent visą dieną.Taip pat į jūros vandens sudėtį įeina:
- Fluoras.
- Bromas.
- Kalcis.
- Kalis.
- Chloras.
- sulfatai.
- Auksas.
Tiesa, procentais visų šių elementų yra daug mažiau nei druskų.
Vandens būsenos ir rūšys
Vanduo planetoje Žemėje gali turėti tris pagrindines agregacijos būsenas: skystą, kietą ir dujinę, kurios gali virsti įvairiomis formomis, kurios vienu metu egzistuoja viena su kita (ledkalniai jūros vandenyje, vandens garai ir ledo kristalai debesyse danguje, ledynai ir laisvieji). - tekančios upės).
Priklausomai nuo kilmės, paskirties ir sudėties savybių, vanduo gali būti:
- šviežias;
- mineralinis;
- jūrinis;
- gėrimas (čia įtraukiame vandenį iš čiaupo);
- lietus;
- atšildytas;
- sūrus;
- struktūrizuotas;
- distiliuotas;
- dejonizuotas.
Vandenilio izotopų buvimas daro vandenį:
- šviesa;
- sunkus (deuteris);
- supersunkus (tritis).
Visi žinome, kad vanduo gali būti minkštas ir kietas: šį rodiklį lemia magnio ir kalcio katijonų kiekis.
Kiekvienas iš mūsų išvardytų vandens tipų ir agreguotų būsenų turi savo užšalimo ir lydymosi temperatūrą.
Užšaldančio sūraus vandens vaizdo įrašas

 Ką žinote apie vandens virimo temperatūrą?
Ką žinote apie vandens virimo temperatūrą?

Temperatūros režimas visų pirma lemia užšalimo proceso greitį.
Temperatūra teigiamų ir neigiamų verčių diapazone turi įtakos reakcijų greičiui, junginių tirpumui, tirpimo greičiui, krešėjimui, taip pat nedisocijuotų jonų porų koncentracijai. Tirpaluose yra keletas temperatūros tipų: struktūrinė, užšalimo temperatūra. Kristalizacijos pradžios temperatūra (užšalimo taškas) - temperatūra, kurioje dėl tirpalo aušinimo prasideda kristalų susidarymas. Užšalimo temperatūros sumažėjimas ΔТз yra skirtumas tarp gryno tirpiklio ir tirpalo užšalimo temperatūros. Sūrymo užšalimo temperatūra visada yra žemesnė už gryno vandens užšalimo temperatūrą ir priklauso nuo ištirpusių druskų koncentracijos. Šią sūrymų priklausomybę galima išreikšti lygtimi:
kur KAM
- proporcingumo koeficientas; SU
yra tirpios medžiagos koncentracija tirpale.
Mažiau praskiestuose tirpaluose kristalizacijos pradžios temperatūra nustatoma pagal atitinkamos sistemos būsenos diagramą. Kadangi jūros vandens ir labai mineralizuotų natūralių sūrymų užšalimo temperatūra skirsis, manome, kad ši temperatūra turėtų būti skaičiuojama naudojant skirtingas formules.
Atlikome darbe naudojamų valgomosios druskos, jūros vandens ir natūralių sūrymų tirpalų užšalimo temperatūros eksperimentinių duomenų aproksimaciją. Užšalimo temperatūros pokyčių priklausomybės grafine ir analitine forma pateiktos 41-43 paveiksluose.
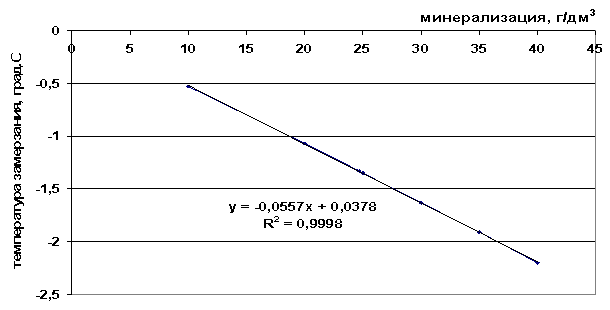
Ryžiai. 41. Užšalimo temperatūros priklausomybė nuo druskos tirpalo druskingumo
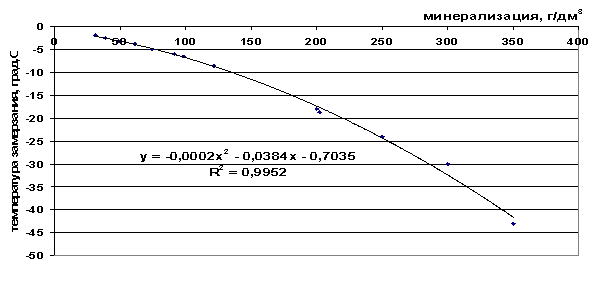
Ryžiai. 42. Jūros vandens užšalimo temperatūros priklausomybė nuo druskingumo
Ryžiai. 43. Sūrymo užšalimo temperatūros priklausomybė nuo druskingumo
Iš pateiktų užšalimo taško verčių (9 lentelė) matyti, kad užšalimo temperatūra mažėja didėjant bendram tirpalo druskingumui ir didėjant į užšalusią sistemą įtrauktų komponentų skaičiui - ΔТз(NaCl)
9 lentelė. Sudarytų grafinių priklausomybių analizė
|
Ctot, g/dm 3 |
Užšalimo temperatūra, °С |
||
|
NaCl tirpalas |
jūros vandens |
||
|
t = 8∙10 -5 M 2 -0,0945 M + 1,0595, |
0,0557 mln. + 0,0378, |
t = -2∙10 -4 M 2 -0,0384M-0,7035, |
|
*
R 2 – aproksimacijos patikimumas
Yra žinoma, kad atskirų druskų užšalimas iš gėlinto vandens įvyksta esant skirtingoms temperatūroms, pavyzdžiui, esant -2°C temperatūrai, nusėda kalcio karbonatas. Esant -3,5 ° C natrio sulfatas. Temperatūrai nukritus iki –20 °C, nusėda valgomoji druska, iki –25,5–26 °C – magnio chloridai, o esant labai žemai – 40–55 °C temperatūrai – kalio ir kalcio chloridai. Esant neigiamoms temperatūroms, kristalinių hidratų, kurie yra nestabilūs žemesnėje nei 0°C temperatūroje, susidarymo procesas yra specifinis. Pavyzdžiui, hidrohalitas NaCl * 2H 2 O susidaro -0,15 ° C temperatūroje, MgCl 2 * 12H 2 O yra stabilus -15 ° C temperatūroje, o MgCl 2 * 8H 2 O yra žemesnėje nei 0 ° C temperatūroje, Na 2 CO 3 * 7H 2 O susidaro tik -10°C temperatūroje. KCl kristalizuojasi 0°С temperatūroje KCl pavidalu, prie -6,6°С jau egzistuoja dvi fazės - KCl ir KCl*H 2 O, esant -10,6°С nusėda tik KCl*H 2 O. Esant neigiamai temperatūrai, atskiri kristaliniai hidratai su maksimaliu įmanomu kristalizacijos vandens molekulių skaičiumi, pagal koordinacinius skaičius tam tikroje reikšme, ir jų mišinius (bet ne mišrius kristalus). Reikia pastebėti nenormalų koncentruotų tirpalų užšalimo temperatūros sumažėjimą.
Atkreipiame jūsų dėmesį į leidyklos „Gamtos istorijos akademija“ leidžiamus žurnalus
Kokioje temperatūroje vanduo užšąla? Atrodytų – paprasčiausias klausimas, į kurį gali atsakyti net vaikas: vandens užšalimo temperatūra esant normaliam 760 mmHg atmosferos slėgiui yra nulis laipsnių Celsijaus.
Tačiau vanduo (nepaisant itin plataus paplitimo mūsų planetoje) yra pati paslaptingiausia ir iki galo nesuvokta substancija, todėl atsakymas į šį klausimą reikalauja išsamios ir pagrįstos diskusijos.
- Rusijoje ir Europoje temperatūra matuojama pagal Celsijaus skalę, kurios didžiausia vertė – 100 laipsnių.
- Amerikiečių mokslininkas Farenheitas sukūrė savo skalę su 180 padalų.
- Yra dar vienas temperatūros matavimo vienetas – kelvinas, pavadintas anglų fiziko Tomsono, gavusio lordo Kelvino titulą, vardu.
Kodėl neturėtumėte gerti jūros vandens
Šią temą jau trumpai palietėme, pažvelkime į ją šiek tiek plačiau. Kartu su jūros vandeniu į organizmą patenka du jonai – magnio ir natrio.
|
Natrio |
Magnis |
|
Dalyvauja palaikant vandens ir druskos pusiausvyrą, vienas iš pagrindinių jonų kartu su kaliu. |
Pagrindinis poveikis yra centrinei nervų sistemai. |
|
Padidėjus skaičiui Na |
Labai lėtai išsiskiria iš organizmo. |
|
Sutrinka visi biologiniai ir biocheminiai procesai. |
Perteklius organizme sukelia viduriavimą, o tai apsunkina dehidrataciją. |
|
Žmogaus inkstai negali susidoroti su tiek daug druskos organizme. |
Galbūt nervų sutrikimų vystymasis, netinkama būklė. |
Negalima sakyti, kad žmogui visų šių medžiagų nereikia, tačiau poreikiai visada telpa tam tikrose ribose. Išgėrę kelis litrus tokio vandens, per toli peržengsite jų ribas.
Tačiau šiandien skubus jūros vandens naudojimo poreikis gali iškilti tik tarp laivų avarijų aukų.