Methoden voor het produceren van waterstof onder industriële omstandigheden
Extractie door methaanconversie
. Verdampt water, voorverwarmd tot 1000 graden Celsius, wordt onder druk en in aanwezigheid van een katalysator gemengd met methaan. Deze methode is interessant en bewezen, waarbij ook moet worden opgemerkt dat deze voortdurend wordt verbeterd: er wordt gezocht naar nieuwe katalysatoren die goedkoper en efficiënter zijn.
Overweeg de oudste methode om waterstof te verkrijgen - kolenvergassing
. Bij afwezigheid van luchttoegang en een temperatuur van 1300 graden Celsius worden kolen en waterdamp verwarmd. Zo wordt waterstof uit water verdrongen en wordt koolstofdioxide verkregen (waterstof zal bovenaan zijn, koolstofdioxide, ook verkregen als resultaat van de reactie, zal onderaan zijn). Dit zal de scheiding van het gasmengsel zijn, alles is heel eenvoudig.
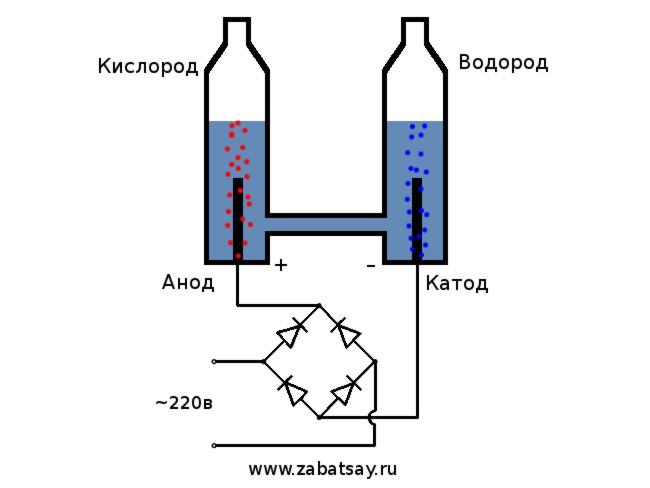
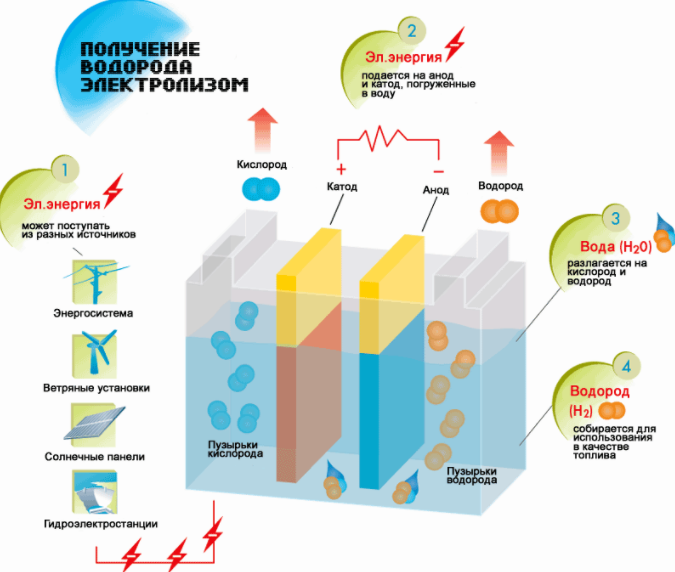
Waterstof verkrijgen door: waterelektrolyse
beschouwd als de gemakkelijkste optie. Voor de implementatie ervan is het noodzakelijk om een oplossing van soda in de container te gieten en daar ook twee elektrische elementen te plaatsen. De ene zal positief geladen zijn (anode) en de andere negatief (kathode). Als er stroom wordt aangelegd, gaat waterstof naar de kathode en zuurstof naar de anode.
Waterstof verkrijgen volgens de methode gedeeltelijke oxidatie
. Hiervoor wordt een legering van aluminium en gallium gebruikt. Het wordt in water geplaatst, wat leidt tot de vorming van waterstof en aluminiumoxide tijdens de reactie. Gallium is nodig om de reactie volledig te laten verlopen (dit element zorgt ervoor dat aluminium niet voortijdig oxideert).
Recent aan relevantie gewonnen methode voor het gebruik van biotechnologie
: bij gebrek aan zuurstof en zwavel begint chlamydomonas intensief waterstof af te geven. Een zeer interessant effect, dat nu actief wordt bestudeerd.
Vergeet niet een andere oude, beproefde methode om waterstof te produceren, namelijk om anders te gebruiken alkalische elementen
en water. In principe is deze techniek haalbaar in laboratoriumomstandigheden met de nodige veiligheidsmaatregelen. Zo worden tijdens de reactie (deze verloopt bij verhitting en met katalysatoren) metaaloxide en waterstof gevormd. Het blijft alleen om het te verzamelen.
Krijg waterstof door interacties van water en koolmonoxide
alleen mogelijk in een industriële omgeving. Kooldioxide en waterstof worden gevormd, het principe van hun scheiding is hierboven beschreven.
DE UITVINDING HEEFT DE VOLGENDE VOORDELEN:
De warmte die wordt verkregen door de oxidatie van gassen kan direct ter plaatse worden gebruikt, en waterstof en zuurstof worden verkregen door de afvoer van uitlaatstoom en industrieel water.
Laag waterverbruik bij het opwekken van elektriciteit en warmte.
De eenvoud van de methode.
Aanzienlijke energiebesparingen, zoals het wordt alleen besteed aan het opwarmen van de starter tot een stabiel thermisch regime.
Hoge procesproductiviteit, omdat dissociatie van watermoleculen duurt tienden van een seconde.
Explosie- en brandveiligheid van de methode, omdat bij de uitvoering zijn er geen tanks nodig om waterstof en zuurstof op te vangen.
Tijdens de werking van de installatie wordt het water herhaaldelijk gezuiverd en omgezet in gedestilleerd water. Dit elimineert neerslag en kalkaanslag, wat de levensduur van de installatie verlengt.
De installatie is gemaakt van gewoon staal; met uitzondering van ketels van hittebestendig staal met bekleding en afscherming van hun wanden. Dat wil zeggen dat er geen speciale dure materialen nodig zijn.
De uitvinding kan toepassing vinden in
industrie door koolwaterstof en splijtstof in elektriciteitscentrales te vervangen door goedkoop, wijdverbreid en milieuvriendelijk water, terwijl de kracht van deze centrales behouden blijft.
CLAIM
Methode voor het produceren van waterstof en zuurstof uit waterdamp
, wat inhoudt dat deze stoom door een elektrisch veld wordt geleid, met het kenmerk dat oververhitte waterdamp wordt gebruikt met een temperatuur 500 - 550 o C
, door een elektrisch veld met gelijkstroom met hoge spanning geleid om de damp te dissociëren en te scheiden in waterstof- en zuurstofatomen.
Ik wilde al heel lang zoiets doen. Maar verdere experimenten met een batterij en een paar elektroden kwamen niet uit. Ik wilde een volwaardig apparaat maken voor de productie van waterstof, in hoeveelheden om de ballon op te blazen. Alvorens een volwaardig apparaat voor waterelektrolyse te maken thuis, besloot ik alles op het model te controleren.
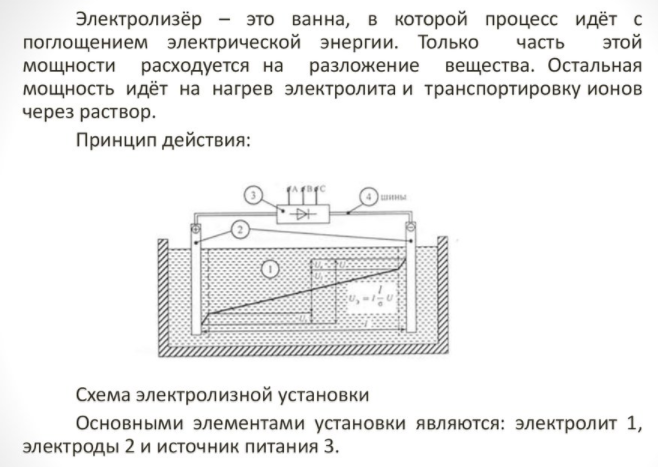
Het algemene schema van de elektrolyseur ziet er als volgt uit.
Dit model is niet geschikt voor volledig dagelijks gebruik. Maar het idee werd getest.
Dus voor de elektroden besloot ik grafiet te gebruiken. Een uitstekende bron van grafiet voor elektroden is de stroomafnemer van de trolleybus. Er zijn er genoeg die rondslingeren bij de laatste haltes. Er moet aan worden herinnerd dat een van de elektroden zal worden vernietigd.
Zagen en afwerken met een vijl. De intensiteit van elektrolyse hangt af van de sterkte van de stroom en het oppervlak van de elektroden.
Aan de elektroden zijn draden bevestigd. Draden moeten zorgvuldig worden geïsoleerd.
Plastic flessen zijn redelijk geschikt voor het lichaam van het elektrolysemodel. In het deksel zijn gaten gemaakt voor buizen en draden.
Alles wordt zorgvuldig ingesmeerd met kit.
Afgesneden flessenhalzen zijn geschikt om twee containers aan te sluiten.
Ze moeten met elkaar worden verbonden en de naad smelten.
Noten worden gemaakt van kroonkurken.
In de bodem van twee flessen worden gaten gemaakt. Alles is aangesloten en zorgvuldig gevuld met kit.
Als spanningsbron gebruiken we een huishoudnet van 220V. Ik wil je waarschuwen dat dit nogal gevaarlijk speelgoed is. Dus als er niet voldoende vaardigheden zijn of als er twijfels zijn, is het beter om niet te herhalen. In het huishoudelijke netwerk hebben we wisselstroom, voor elektrolyse moet deze worden rechtgetrokken. Een diodebrug is hier perfect voor. Die op de foto was niet krachtig genoeg en brandde snel op. De beste optie was de Chinese MB156 diodebrug in een aluminium behuizing.
De diodebrug wordt erg heet. Vereist actieve koeling. Een koeler voor een computerprocessor past er perfect in. Voor het geval kunt u een soldeerdoos van geschikt formaat gebruiken. Verkocht in elektrische goederen.
Onder de diodebrug is het noodzakelijk om meerdere lagen karton te plaatsen.
De nodige gaten worden gemaakt in het deksel van de soldeerdoos.
Zo ziet de gemonteerde unit eruit. De elektrolyser wordt gevoed vanuit het lichtnet, de ventilator van een universele stroombron. Als elektrolyt wordt een oplossing van zuiveringszout gebruikt. Hierbij moet worden bedacht dat hoe hoger de concentratie van de oplossing, hoe hoger de reactiesnelheid. Maar tegelijkertijd is de verwarming hoger. Bovendien zal de reactie van natriumontleding aan de kathode zijn bijdrage leveren aan de verwarming. Deze reactie is exotherm. Als gevolg hiervan zullen waterstof en natriumhydroxide worden gevormd.
Het apparaat op de foto hierboven was erg heet. Het moest periodiek worden uitgeschakeld en wachten tot het afkoelt. Het probleem met verwarming werd gedeeltelijk opgelost door de elektrolyt af te koelen. Hiervoor heb ik een tafelfonteinpomp gebruikt. Een lange buis loopt van de ene fles naar de andere door een pomp en een emmer koud water.
De relevantie van dit probleem is tegenwoordig vrij hoog vanwege het feit dat de reikwijdte van het gebruik van waterstof extreem uitgebreid is en dat het in zijn pure vorm praktisch nergens in de natuur wordt gevonden. Daarom zijn er verschillende methoden ontwikkeld om dit gas via chemische en fysische reacties uit andere verbindingen te halen. Dit is wat in dit artikel wordt besproken.
Waterstofproductie in het huishouden
Keuze van een elektrolysecel
Om een element van het huis te verkrijgen, is een speciaal apparaat nodig - een elektrolyse.Er zijn veel opties voor dergelijke apparatuur op de markt, de apparaten worden aangeboden door zowel bekende technologiebedrijven als kleine fabrikanten. Merkeenheden zijn duurder, maar hun bouwkwaliteit is hoger.
Het huishoudapparaat is klein van formaat en gemakkelijk te gebruiken. De belangrijkste details zijn:
- hervormer;
- reinigingssysteem;
- brandstofcellen;
- compressor apparatuur;
- waterstof opslagtank.
Gewoon kraanwater wordt als grondstof genomen en elektriciteit komt uit een gewoon stopcontact. Units op zonne-energie besparen op elektriciteit.
"Home" waterstof wordt gebruikt in verwarmings- of kooksystemen. Ze verrijken ook het lucht-brandstofmengsel om het vermogen van automotoren te vergroten.
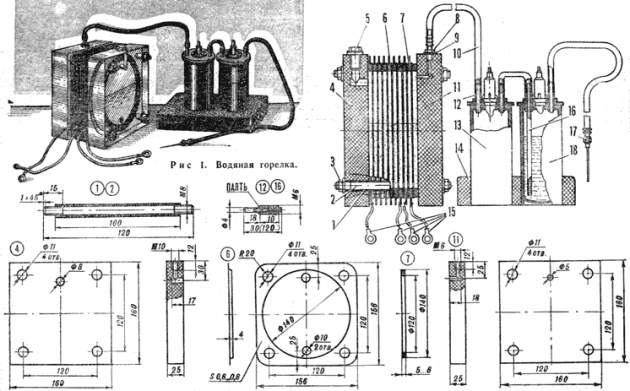
Het apparaat met je eigen handen maken
Het is zelfs goedkoper om het apparaat thuis zelf te maken. Een droge cel ziet eruit als een afgesloten container, die bestaat uit twee elektrodeplaten in een container met een elektrolytische oplossing. Het World Wide Web biedt een verscheidenheid aan schema's voor het samenstellen van apparaten van verschillende modellen:
- met twee filters;
- met de boven- of onderkant van de container;
- met twee of drie kleppen;
- met gegalvaniseerde plaat;
- op de elektroden.
Een eenvoudig apparaat om waterstof te produceren is eenvoudig te maken. Het vereist:
- plaat roestvrij staal;
- transparante buis;
- uitrusting;
- plastic container (1,5 l);
- waterfilter en terugslagklep.
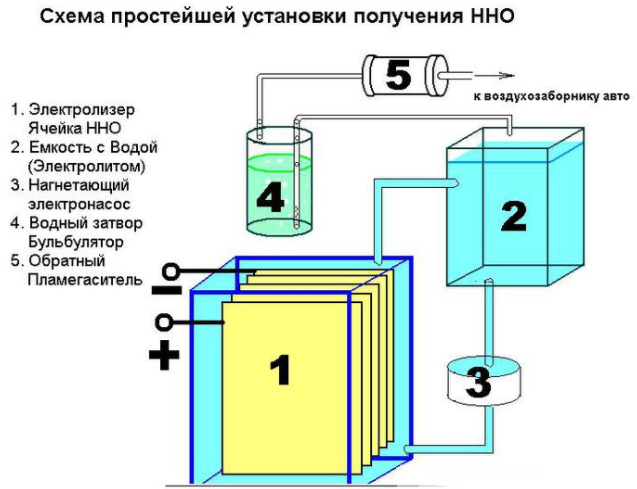
Daarnaast is er verschillende hardware nodig: moeren, ringen, bouten. Allereerst moet je het vel in 16 vierkante compartimenten snijden, van elk een hoek afsnijden. In de tegenoverliggende hoek moet een gat worden geboord voor het vastschroeven van de platen. Om een constante stroom te garanderen, moeten de platen worden aangesloten volgens het schema: plus-min-plus-min. Deze delen zijn van elkaar geïsoleerd met een buis, en bij de verbinding met een bout en ringen (drie stuks tussen de platen). Op de plus en min worden 8 borden geplaatst.
Bij juiste montage raken de randen van de platen de elektroden niet. De verzamelde delen worden neergelaten in een plastic container. Op de plaats waar de wanden elkaar raken, zijn met bouten twee montagegaten gemaakt. Installeer een veiligheidsklep om overtollig gas te verwijderen. Fittingen zijn gemonteerd in het deksel van de container en de naden zijn afgedicht met siliconen.
Apparaat testen
Voer verschillende acties uit om het apparaat te testen:
- Vul met vloeistof.
- Sluit het ene uiteinde van de buis aan op de fitting en sluit af met een deksel.
- De tweede wordt in het water neergelaten.
- Sluit aan op een stroombron.
Nadat het apparaat in het stopcontact is gestoken, zal na enkele seconden het elektrolyseproces en de neerslag merkbaar zijn.
Zuiver water heeft geen goede elektrische geleidbaarheid. Om deze indicator te verbeteren, moet u een elektrolytische oplossing maken door alkali - natriumhydroxide toe te voegen. Het zit in composities voor het reinigen van pijpen zoals "Mole".
Methoden voor het produceren van waterstof
Waterstof is een kleurloos en geurloos gasvormig element met een dichtheid van 1/14 ten opzichte van lucht. Het wordt zelden gevonden in de vrije staat. Gewoonlijk wordt waterstof gecombineerd met andere chemische elementen: zuurstof, koolstof.
Waterstofproductie voor industriële behoeften en energie wordt op verschillende manieren uitgevoerd. De meest populaire zijn:
- water elektrolyse;
- concentratie methode;
- condensatie bij lage temperatuur;
- adsorptie.
Waterstof kan niet alleen worden geïsoleerd uit gas- of waterverbindingen. Waterstof wordt geproduceerd door hout en steenkool bloot te stellen aan hoge temperaturen en door bioafval te verwerken.
Atoomwaterstof voor energietechniek wordt verkregen met behulp van de methode van thermische dissociatie van een moleculaire stof op een draad gemaakt van platina, wolfraam of palladium. Het wordt verwarmd in een waterstofomgeving bij een druk van minder dan 1,33 Pa.Radioactieve elementen worden ook gebruikt om waterstof te produceren.
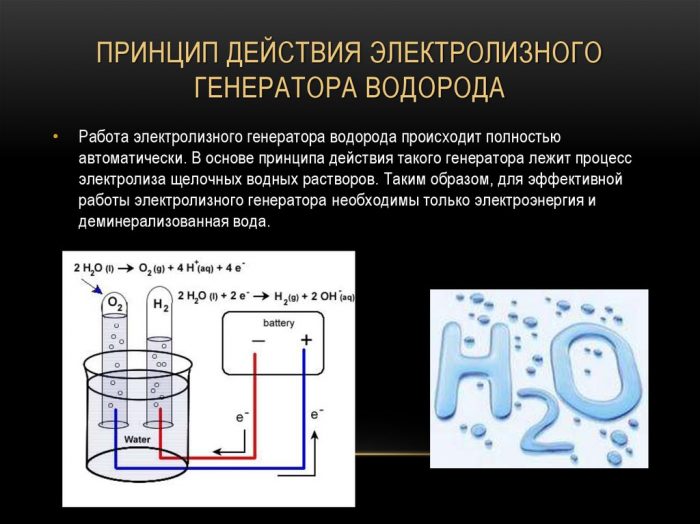
elektrolyse methode:
De eenvoudigste en meest populaire methode voor waterstofextractie is waterelektrolyse. Het maakt het mogelijk om praktisch zuivere waterstof te verkrijgen. Andere voordelen van deze methode zijn:
- beschikbaarheid van grondstoffen;
- het verkrijgen van een element onder druk;
- de mogelijkheid om het proces te automatiseren door het ontbreken van bewegende delen.
De procedure voor het splitsen van een vloeistof door elektrolyse is het omgekeerde van de verbranding van waterstof. De essentie is dat onder invloed van gelijkstroom zuurstof en waterstof vrijkomen op elektroden die zijn gedompeld in een waterige elektrolytoplossing.
Een bijkomend voordeel is de productie van bijproducten met industriële waarde. Zo is zuurstof in een groot volume nodig voor het katalyseren van technologische processen in de energiesector, het reinigen van bodem en waterlichamen en het afvoeren van huishoudelijk afval. Zwaar water geproduceerd door elektrolyse wordt gebruikt in de energie-industrie in kernreactoren.
Productie van waterstof door concentratie
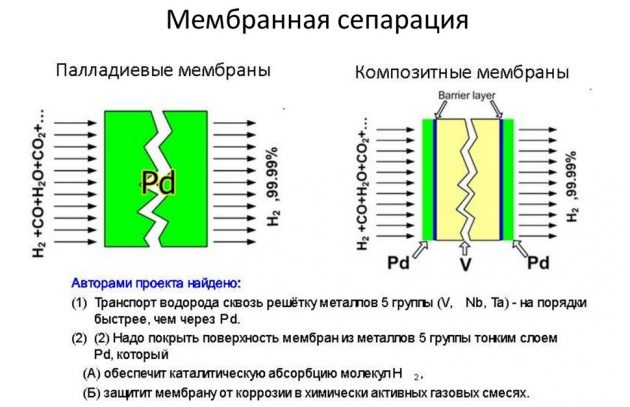
Deze methode is gebaseerd op de scheiding van een element uit gasmengsels die het bevatten. Zo wordt het grootste deel van de in industriële volumes geproduceerde stof gewonnen met stoomreforming van methaan. Waterstof die in dit proces wordt geproduceerd, wordt gebruikt in energie, olieraffinage, raketindustrie en voor de productie van stikstofmeststoffen. Het proces om H2 te verkrijgen wordt op verschillende manieren uitgevoerd:
- korte cyclus;
- cryogeen;
- membraan.
De laatste methode wordt als de meest effectieve en goedkopere beschouwd.
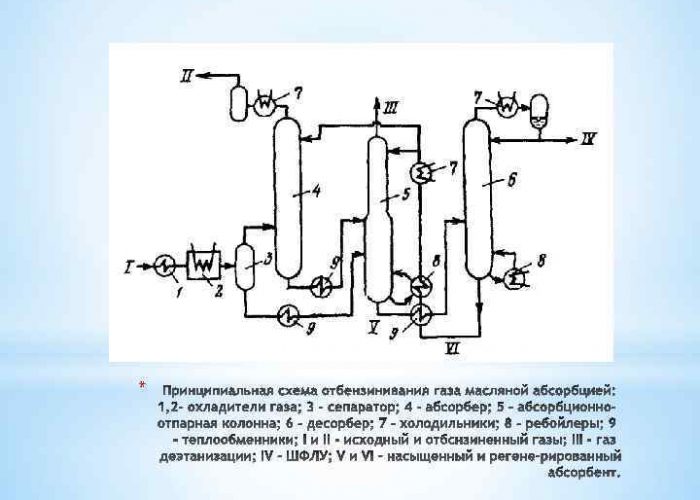
Condensatie bij lage temperaturen
Deze techniek voor het verkrijgen van H2 bestaat uit het sterk afkoelen van gasverbindingen onder druk. Hierdoor worden ze omgezet in een tweefasensysteem, dat vervolgens door een separator wordt gescheiden in een vloeibare component en een gas. Vloeibare media worden gebruikt voor koeling:
- water;
- vloeibaar gemaakt ethaan of propaan;
- vloeibare ammoniak.
Deze procedure is niet zo eenvoudig als het lijkt. Het is niet mogelijk om koolwaterstofgassen tegelijk schoon te scheiden. Een deel van de componenten gaat weg met het gas uit het scheidingscompartiment, wat niet economisch is. Het probleem kan worden opgelost door de grondstof vóór scheiding diep te koelen. Maar dit kost veel energie.
In moderne systemen van lagetemperatuurcondensors zijn bovendien demethanisatie- of deethanisatiekolommen aanwezig. De gasfase wordt verwijderd uit de laatste scheidingstrap en de vloeistof wordt na warmtewisseling met de ruwe gasstroom naar de destillatiekolom gestuurd.
Adsorptie methode:
Tijdens adsorptie worden adsorptiemiddelen gebruikt om waterstof vrij te maken - vaste stoffen die de noodzakelijke componenten van het gasmengsel absorberen. Als adsorbentia worden actieve kool, silicaatgel en zeolieten gebruikt. Om dit proces uit te voeren, worden speciale apparaten gebruikt - cyclische adsorbers of moleculaire zeven. Bij toepassing onder druk kan deze methode 85 procent waterstof terugwinnen.
Als we adsorptie vergelijken met condensatie bij lage temperatuur, kunnen we de lagere materiaal- en operationele kosten van het proces vaststellen - gemiddeld met 30 procent. De adsorptiemethode produceert waterstof voor energie en met gebruik van oplosmiddelen. Deze methode maakt de extractie van 90 procent H2 uit het gasmengsel en de productie van het eindproduct met een waterstofconcentratie tot 99,9% mogelijk.