CLAIM
1. De methode van directe vloeibaarmaking van steenkool, die de volgende fasen omvat:
(1) het bereiden van een steenkoolsuspensie uit ruwe steenkool en een katalysator;
(2) het mengen van de koolsuspensie met waterstof en voorbehandeling van het mengsel, gevolgd door de toevoer naar het reactiesysteem voor het uitvoeren van de vloeibaarmakingsreactie;
(3) het scheiden van de reactieproducten die aan de reactor zijn onttrokken in een separator (9, 10) om een vloeibare fase en een gasfase te vormen, waarbij de vloeibare fase wordt onderworpen aan fractionering in een destillatiekolom (11) bij atmosferische druk om een product in de vorm van een dieselbrandstoffractie en een restproduct;
(4) het toevoeren van het in de atmosferische drukkolom verkregen restproduct aan een vacuümdestillatiekolom (12) voor scheiding in destillaat en residu;
(5) het mengen van de dieselbrandstoffractie en het destillaat om een mengsel te vormen en vervolgens het mengsel toe te voeren aan de hydroprocessingreactor (13) met geforceerde circulatie met gefluïdiseerd bed om het hydrogeneringsproces uit te voeren;
(6) fractionering van de hydrogeneringsproducten tot olieproducten en waterstofdonoroplosmiddel dat wordt gerecirculeerd naar stap (1).
2. Werkwijze volgens conclusie 1, waarbij stap (1) de volgende bewerkingen omvat:
(a) het omzetten van de ruwe steenkool in steenkoolpoeder met een bepaalde deeltjesgrootte na het drogen en malen van de ruwe steenkool in een voorbehandelingsapparaat; (b) het behandelen van de katalysatorvoeding (3) en het steenkoolpoeder in de katalysatorbereidingsinrichting (4) om een ultrafijn poeder voor het vloeibaar maken van steenkool te verkrijgen; (c) het mengen in de inrichting (5) voor het bereiden van een suspensie van de koolvloeibaarmakingskatalysator en koolpoeder met een waterstofdonoroplosmiddel (16) om een koolsuspensie te vormen.
3. Werkwijze volgens conclusie 1, waarbij de reactiestap voor het vloeibaar maken van kolen de volgende stappen omvat:
(a) het voeden van de kolenslurry na het mengen met waterstof (6) en het voorverwarmen ervan in de eerste wervelbedreactor (7) met geforceerde circulatie om de vloeibaarmakingsreactie uit te voeren om reactieproducten te verkrijgen die de reactor verlaten; (b) het toevoeren van de reactieproducten die de eerste wervelbedreactor (7) verlaten, na ze te hebben gemengd met waterstof, naar de tweede wervelbedreactor (8) met geforceerde circulatie om de vloeibaarmakingsreactie voort te zetten, waarbij genoemde wervelbedreactoren werken bij de volgende reactie omstandigheden: reactietemperatuur 430-465°C; reactiedruk 15-19 MPa; de verhouding van de hoeveelheden gas en vloeistof 600-1000 nl/kg; volumetrische snelheid van kolensuspensie 0,7-1,0 t/m3 h; de mate van toevoeging van de katalysator Fe/droge kool = 0,5-1,0 gew.%.
4. Werkwijze volgens conclusie 1, waarbij stap (3) de volgende bewerkingen omvat:
(a) het toevoeren van de stroom reactieproducten aan een hogetemperatuurscheider (9) voor scheiding in een gasfase en een vloeibare fase, terwijl de temperatuur in de hogetemperatuurscheider op 420°C wordt gehouden;
(b) het toevoeren van de gasfase van de hogetemperatuurscheider (9) naar de lagetemperatuurscheider (10) voor verdere scheiding in gas en vloeistof, terwijl de temperatuur in de lagetemperatuurscheider op kamertemperatuur wordt gehouden.
5. Werkwijze volgens conclusie 2, waarbij -FeOOH als vloeibaarmakingskatalysator wordt gebruikt, waarvan de deeltjes een diameter hebben van 20-30 nm en een lengte van 100-180 nm, en de katalysator zwavel bevat in een molaire verhouding van S/Fe=2.
6. Werkwijze volgens conclusie 1, waarbij de hydrogenering in stap (5) wordt uitgevoerd onder de volgende omstandigheden: reactietemperatuur 330-390°C; reactiedruk 10-15 MPa; de verhouding van de hoeveelheden gas en vloeistof 600-1000 nl/kg; ruimtesnelheid 0,8-2,5 h-1.
7. Werkwijze volgens conclusie 1, waarbij het teruggevoerde waterstofdonoroplosmiddel een gehydrogeneerd vloeibaar gemaakt aardolieproduct is met een kookpunt in het traject van 220-450°C.
8. Werkwijze volgens conclusie 1, waarbij het residu in de vacuümdestillatiekolom (12) een gehalte aan vaste stof van 50-55 gew.% heeft.
9. Werkwijze volgens conclusie 1, waarbij het mengsel van de dieselbrandstoffractie die de atmosferische drukkolom verlaat en het destillaat uit de vacuümkolom een kookpunt heeft van C 5 in het bereik van 530 ° .
10.2. Werkwijze volgens conclusie 1, waarbij de hydroprocessingreactor met gefluïdiseerd bed (13) met geforceerde circulatie een interne reactor is, waarbij een circulatiepomp nabij de bodem van de reactor is geïnstalleerd en de katalysator in de reactor tijdens bedrijf kan worden vervangen.
CLAIM
1. Werkwijze voor het verbranden van steenkool, daaronder begrepen drogen, vermalen tot fijn gedispergeerde toestand, mengen van gemalen steenkool met een gerichte zuurstofhoudende gasstroom en verbranden, met het kenmerk, dat de gemalen steenkool wordt verhit tot een semi-verkooksingstemperatuur van ca. Minstens 500 °C komen daaruit vluchtige gasvormige koolwaterstoffen vrij, die door condensatie verder worden verdeeld in vloeibare en gasvormige fracties, en de door verhitting van de gemalen steenkool verkregen halfcokes wordt gemengd met de gerichte zuurstofhoudende gasstroom en verbrand.
2. Werkwijze volgens conclusie 1, met het kenmerk, dat het drogen van de gemalen steenkool gelijktijdig met het malen van de steenkool wordt uitgevoerd.
3. Werkwijze volgens conclusie 1, met het kenmerk, dat de gemalen kool door vermenging met een gasvormige warmtedrager tot een semi-verkooksingstemperatuur wordt verwarmd.
4. Werkwijze volgens conclusie 1, met het kenmerk, dat de gemalen steenkool wordt verwarmd tot de temperatuur van semi-cokesvorming door deze te mengen met een vaste warmtedrager met een temperatuur van 800-1300°C.
5. Werkwijze volgens conclusie 3, met het kenmerk, dat de gasvormige warmtedrager gassen zijn die ontstaan bij de verbranding van ten minste een deel van vluchtige gasvormige koolwaterstoffen.
6. Werkwijze volgens conclusie 3, met het kenmerk, dat het gasvormige koelmiddel de gassen zijn die worden gevormd tijdens de verbranding van ten minste een deel van de resulterende semi-cokes.
7. Werkwijze volgens conclusie 4, met het kenmerk, dat de vaste warmtedrager de resulterende halfcokes is.
8. Werkwijze volgens conclusie 4, met het kenmerk, dat de vaste warmtedrager kwartszand is.
9. Werkwijze volgens conclusie 4, met het kenmerk, dat de vaste warmtedrager een keramisch gedispergeerd materiaal is.
10. Werkwijze volgens conclusie 4, met het kenmerk, dat de vaste warmtedrager steenkool is.
11. Werkwijze volgens conclusie 4, met het kenmerk, dat de vaste warmtedrager een oxide van een anorganische stof is met een fractiegrootte van 0,5-5 mm.
12. Werkwijze volgens conclusie 9, of 10, of 12, met het kenmerk, dat het koelmiddel na gebruik door zeven van de halfcokes wordt gescheiden.
13. Werkwijze volgens conclusie 1, met het kenmerk, dat de gasvormige fractie van vluchtige koolwaterstoffen geheel of gedeeltelijk wordt verbrand.
14. Werkwijze volgens conclusie 13, met het kenmerk, dat de gasvormige fractie van vluchtige koolwaterstoffen vóór verbranding wordt gezuiverd van zwavelhoudende stoffen.
15. Werkwijze volgens conclusie 1, met het kenmerk, dat de verhitting van de gemalen steenkool tot de temperatuur van semi-verkooksing wordt uitgevoerd in een wervelkamer door deze te mengen met heet gas.
Antwoorden op paragraaf 19
1. Wat zijn de belangrijkste natuurlijke bronnen van koolwaterstoffen die u kent: olie, aardgas, schalie, steenkool.
2. Wat is de samenstelling van aardgas? Toon op de geografische kaart de belangrijkste afzettingen: a) aardgas; B' olie; c) kolen.
3. Welke voordelen heeft aardgas ten opzichte van andere brandstoffen? Waarvoor wordt aardgas in de chemische industrie gebruikt Aardgas is in vergelijking met andere bronnen van koolwaterstoffen het gemakkelijkst te winnen, te transporteren en te verwerken. In de chemische industrie wordt aardgas gebruikt als bron van koolwaterstoffen met een laag molecuulgewicht.
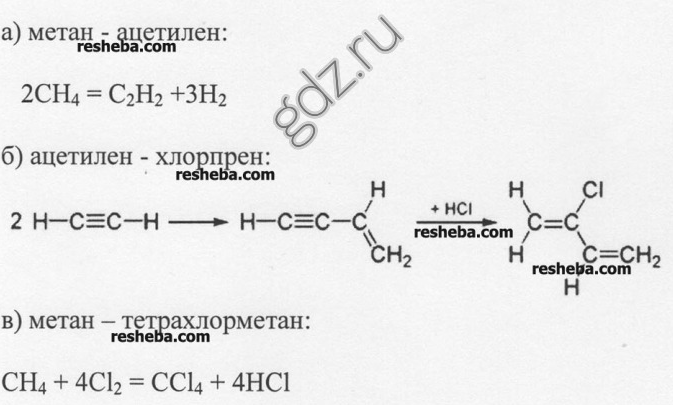
4. Schrijf de reactievergelijkingen voor het verkrijgen van: a) acetyleen uit methaan; b) chloropreenrubber uit acetyleen; c) tetrachloorkoolstof uit methaan.
5. Wat is het verschil tussen geassocieerde petroleumgassen en aardgas Geassocieerde gassen zijn vluchtige koolwaterstoffen opgelost in olie. Hun isolatie vindt plaats door destillatie. In tegenstelling tot aardgas kan het in elk stadium van de ontwikkeling van een olieveld vrijkomen.
6.Beschrijf de belangrijkste producten die worden verkregen uit geassocieerde petroleumgassen Belangrijkste producten: methaan, ethaan, propaan, n-butaan, pentaan, isobutaan, isopentaan, n-hexaan, n-heptaan, hexaan en heptaan-isomeren.
7. Noem de belangrijkste olieproducten, geef hun samenstelling en toepassingsgebieden aan.
8. Welke smeeroliën worden bij de productie gebruikt Tandwieloliën, industriële oliën, snijoliën voor werktuigmachines, enz.
9. Hoe wordt de oliedestillatie uitgevoerd?
10. Wat is oliekraken? Maak een vergelijking voor de reacties van koolwaterstofsplitsing en in dit proces.
11. Waarom is het mogelijk om bij directe destillatie van olie niet meer dan 20% benzine te verkrijgen, omdat het gehalte van de benzinefractie in olie beperkt is.
12. Wat is het verschil tussen thermisch kraken en katalytisch kraken? Geef een beschrijving van de benzines voor thermisch en katalytisch kraken Bij thermisch kraken is het noodzakelijk om de reactanten tot hoge temperaturen te verhitten, bij katalytisch kraken vermindert de introductie van een katalysator de activeringsenergie van de reactie, wat de reactie aanzienlijk kan verminderen temperatuur.
13. Hoe kan men gekraakte benzine praktisch onderscheiden van gewone benzine?Gekraakte benzine heeft een hoger octaangetal dan gewone benzine, d.w.z. beter bestand tegen detonatie en aanbevolen voor gebruik in verbrandingsmotoren.
14. Wat is aromatisering van olie? Schrijf reactievergelijkingen die dit proces verklaren.
15. Wat zijn de belangrijkste producten die worden verkregen door cokeskolen: naftaleen, antraceen, fenantreen, fenolen en koololiën.
16. Hoe wordt cokes geproduceerd en waar wordt het gebruikt Cokes is een grijs poreus vast product dat wordt verkregen door het cocokoken van kolen bij temperaturen van 950-1100 zonder zuurstof. Het wordt gebruikt voor het smelten van ijzer, als een rookloze brandstof, een ijzerertsreductiemiddel en een bakpoeder voor ladingsmaterialen.
17. Wat zijn de belangrijkste producten die worden verkregen: a) uit koolteer; b) uit teerwater; c) uit cokesovengas? Waar worden ze toegepast? Welke organische stoffen kunnen uit cokesovengas worden gewonnen? a) benzeen, tolueen, naftaleen - chemische industrie b) ammoniak, fenolen, organische zuren - chemische industrie c) waterstof, methaan, ethyleen - brandstof.
18. Denk aan alle belangrijke manieren om aromatische koolwaterstoffen te verkrijgen. Wat is het verschil tussen de methoden om aromatische koolwaterstoffen te verkrijgen uit de cokesproducten van steenkool en olie? Schrijf de vergelijkingen van de overeenkomstige reacties op.Ze verschillen in de methoden om te verkrijgen: de raffinage van primaire olie is gebaseerd op het verschil in de fysische eigenschappen van verschillende fracties, en cokesvorming is puur gebaseerd op de chemische eigenschappen van steenkool.
19. Leg uit hoe, bij het oplossen van energieproblemen in het land, de manieren van verwerking en gebruik van natuurlijke koolwaterstofbronnen zullen worden verbeterd Zoeken naar nieuwe energiebronnen, optimalisatie van olieproductie- en raffinageprocessen, ontwikkeling van nieuwe katalysatoren om de kosten van alle productie, enz.
20. Wat zijn de vooruitzichten voor het winnen van vloeibare brandstof uit steenkool In de toekomst is het mogelijk om vloeibare brandstof uit steenkool te winnen, op voorwaarde dat de productiekosten ervan worden verlaagd.
Taak 1. Het is bekend dat het gas 0,9 methaan, 0,05 ethaan, 0,03 propaan, 0,02 stikstof in volumefracties bevat. Hoeveel lucht is er nodig om onder normale omstandigheden 1 m3 van dit gas te verbranden?

Opdracht 3. Bereken welk volume (in l) en welke massa (in kg) koolmonoxide (IV) wordt verkregen door 5 mol octaan (n.o.) te verbranden.
2 Hydrogenering
Bruinkoolhydrogenering is een proces van directe verwerking van steenkool tot synthetische brandstoffen met vloeibare en gasvormige aggregatietoestanden, die plaatsvindt bij hoge druk en relatief hoge temperatuur.
Deze richting van steenkoolverwerking wordt in verschillende landen van de wereld onderzocht.In het buitenland heeft deze technologie de grootste industriële introductie gekregen in Zuid-Afrika, waar vier fabrieken actief zijn, met een totale jaarlijkse capaciteit van ongeveer 8-10 miljoen ton vloeibare brandstof. Het werk wordt uitgevoerd met behulp van de gepatenteerde SASOL-technologie op basis van de verbeterde Fischer-Tropsch-methode. Aangezien SASOL een beleid heeft om hoge betalingen te handhaven voor het recht om de technologie te gebruiken, leidt dit tot hoge kosten van de industriële implementatie in andere landen.[]
Bereiding van bruinkool omvat breken, drogen, bereiding van steenkool-hydrogenaatpasta. Het malen wordt uitgevoerd tot een deeltjesgrootte van minder dan 0,1 mm - om de reactiviteit van het oppervlak te vergroten, wordt het geïmplementeerd in desintegrators. In dit geval neemt het externe specifieke oppervlak met 20-30 keer toe, het volume van de overgangsporiën - met 5-10 keer. De steenkool wordt vervolgens gedroogd. De poriën zijn gevuld met vocht, wat het binnendringen van reagentia in de steenkoolstof voorkomt, het komt vrij tijdens het proces in de reactiezone, waardoor de partiële druk van H2 wordt verlaagd en ook de hoeveelheid afvalwater toeneemt. Voor het drogen worden buisstoomdrogers, vortexkamers, droogleidingen gebruikt waarin steenkool wordt gedroogd tot een restvochtgehalte van 1,5%. De warmtedrager zijn hete rookgassen met een minimaal O2-gehalte (0,1-0,2%) zodat de kolen geen oxidatie ondergaan. Steenkool wordt niet verwarmd boven 150-200 ° C om een afname van de reactiviteit te voorkomen.
Vereisten voor bruinkool gevoed voor vloeibaarmaking
Op basis van een groot experimenteel materiaal is bewezen dat steenkool met een goede hydraulica 65 tot 85% C, meer dan 5% H bevat en meer dan 30% vluchtige (V) opbrengst heeft. Rationeel vochtgehalte van de initiële steenkool voor het hydrogeneringsproces - Wrt = 10-15%, asgehalte Ad = 10-12%, waarde d
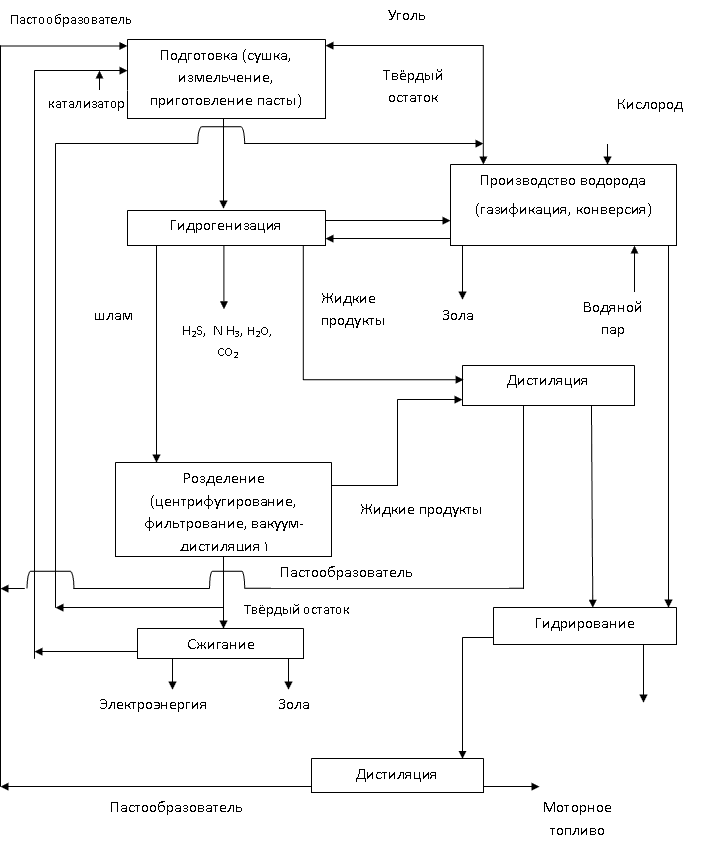
Het meest voorkomende hydrogeneringsschema is weergegeven in figuur 1.2 []
Rijst. 1.2 - Regeling voor het verkrijgen van synthetische vloeibare brandstof uit bruinkool
Dynamiek van gasverbruik uit steenkool in de wereld
| Beoogd gebruik | Gebruik in 2001, MW voor gas | Aandeel in 2001, % | In gebruik genomen voor eind 2004, MW voor gas | Jaarlijkse capaciteitsuitbreiding in 2002-2004, % |
| Chemische productie | 18 000 | 45 | 5 000 | 9,3 |
| Intracyclische vergassing (stroomopwekking) | 12 000 | 30 | 11 200 | 31 |
| Fischer-Tropsch-synthese | 10 000 | 25 | ||
| TOTAAL | 40 000 | 100 | 17 200 | 14,3 |
De gegeven gegevens tonen duidelijk de versnelling van de dynamiek van de betrokkenheid van kolenvergassing in de mondiale industrie. De toegenomen belangstelling voor intracyclische vergassing van steenkool in ontwikkelde landen is te wijten aan twee redenen.
Ten eerste zijn thermische centrales met intracyclische vergassing minder gevaarlijk voor het milieu. Dankzij gasvoorbehandeling wordt de uitstoot van zwaveloxiden, stikstofoxiden en fijnstof verminderd.
Ten tweede kan het gebruik van een binaire cyclus de efficiëntie van de centrale aanzienlijk verhogen en bijgevolg het specifieke brandstofverbruik verminderen.
In tafel. Tabel 2 toont de karakteristieke waarden van specifieke emissies en efficiëntie voor TPP's met intracyclische vergassing en voor TPP's met traditionele kolenverbranding.
tafel 2
Specifieke emissies en efficiëntie voor thermische centrales met intercyclische vergassing en conventionele verbranding van kolen
| Parameters: | Traditionele kolencentrale | TPP met intracyclusvergassing |
| De concentratie van schadelijke stoffen in rookgassen (voor een kolengestookte thermische centrale - volgens de Europese norm), mg / m3 - SOx - NEEx - Vaste deeltjes | 130 150 16 | 10 30 10 |
| Elektrisch rendement, % | 33-35 | 42-46 |
Opgemerkt moet worden dat de specifieke kapitaalkosten bij het gebruik van intracyclusvergassing ongeveer 1500 US dollar per 1 kW bedragen met het vooruitzicht te verminderen tot 1000-1200 US dollar, terwijl voor een traditionele kolengestookte thermische centrale de specifieke kapitaalkosten ongeveer 800-900 Amerikaanse dollars per 1 kW. Het is duidelijk dat een thermische centrale met intracyclische vergassing van vaste brandstof aantrekkelijker is in aanwezigheid van milieubeperkingen op de locatie en bij gebruik van vrij dure brandstof, aangezien het brandstofverbruik per 1 kW wordt verminderd.
Deze omstandigheden zijn typisch voor ontwikkelde landen.Momenteel wordt het gebruik van intracyclische vergassing van vaste brandstoffen beschouwd als de meest veelbelovende richting in de energiesector.
3.3 Technische ontwikkelingen in de afgelopen eeuw
Op dit moment zijn de volgende meest kosteneffectieve toepassingsgebieden van de vergassingsmethode geïdentificeerd:
— vergassing van zwavelhoudende en asrijke brandstoffen met daaropvolgende verbranding van de resulterende gassen in krachtige thermische centrales. De kolen die jaarlijks in Rusland worden gedolven bevatten ongeveer 10 miljoen ton zwavel, waarvan het meeste bij verbranding in de vorm van giftige zwaveloxiden en koolstofsulfide in de atmosfeer terechtkomt. Tijdens de vergassing van zwavelhoudende kolen wordt waterstofsulfide gevormd, dat relatief eenvoudig kan worden geëxtraheerd en vervolgens kan worden verwerkt tot commercieel zwavel of zwavelzuur.
— vergassing van vaste brandstoffen voor grootschalige productie van aardgasvervangers. Deze richting is van het grootste belang voor de lokale gasvoorziening naar gebieden die ver verwijderd zijn van aardgas- en olievelden of van hoofdleidingen.
— vergassing van vaste brandstoffen om synthesegas, reductiegassen en waterstof te verkrijgen voor de behoeften van de chemische, petrochemische en metallurgische industrie.
Het vergassingsproces is afhankelijk van vele factoren die de samenstelling van het resulterende gas en de calorische waarde ervan beïnvloeden. In dit opzicht is er nog steeds geen enkele algemeen aanvaarde classificatie van methoden voor de uitvoering van het beschouwde proces. Hieronder vindt u een van de mogelijke classificatiemogelijkheden.
Naar type ontploffing (vergasser): lucht, lucht-zuurstof, stoom-lucht, stoom-zuurstof.
Door druk: bij atmosferische druk, bij verhoogde druk.
· door de grootte van brandstofdeeltjes: vergassing van grofkorrelige (brok), fijnkorrelige en verpulverde brandstof.
· volgens de ontwerpkenmerken van de reactiezone: in een vaste dichte laag brandstof, in een gefluïdiseerde laag brandstof, in een verpulverde kolenvlam.
door de methode van asverwijdering: in vaste vorm, in de vorm van vloeibare slakken.
Door de methode van warmtetoevoer: met gedeeltelijke verbranding van brandstof in een gasgenerator, met het mengen van brandstof met een voorverwarmde vaste, vloeibare of gasvormige warmtedrager (regeneratieve verwarming), met warmtetoevoer door de wand van het apparaat (recuperatieve verwarming).
Koolmonoxide, metaalcarbonylen en de 18-elektronenregel
Talrijk
syntheses op basis van koolmonoxide en
waterstof vertegenwoordigen een enorme
zowel praktisch als theoretisch
rente, zoals toegestaan vanaf twee
de eenvoudigste stoffen om de meest waardevolle te ontvangen
organische bestanddelen. En hier
katalyse speelt een belangrijke rol
overgangsmetalen die in staat zijn tot:
inerte CO-moleculen activeren en
H2.
Activering van moleculen is hun vertaling in
meer reactieve toestand.
Er moet met name worden opgemerkt dat in de transformaties
synthesegas is op grote schaal ontwikkeld
een nieuw type katalyse - katalyse door complexen
overgangsmetalen of metaalcomplex
katalyse (zie het artikel van O.N. Temkin
).
Dus
Is het CO-molecuul inert? Vertegenwoordiging
over de inertie van koolmonoxide
voorwaardelijk karakter. Terug in 1890 Mond
verkregen uit metallisch nikkel en
koolmonoxide eerste carbonyl
metaalverbinding, vluchtige vloeistof
met een kookpunt van 43°C - Ni (CO)4 .
De geschiedenis van deze ontdekking is interessant.
die als willekeurig kunnen worden geclassificeerd. maandag,
onderzoek naar de oorzaken van snelle corrosie
nikkelreactoren in productie
soda uit NaCl, ammoniak en CO2,
gevonden dat de oorzaak van corrosie is:
aanwezigheid in CO2 onzuiverheden
koolmonoxide, dat reageerde
met nikkel om tetracarbonyl te vormen
Ni (CO)4 .
Door deze ontdekking kon Mond verder
methoden ontwikkelen voor het zuiveren van nikkel
door de productie van een vluchtige carbonyl
nikkel en de daaropvolgende thermische
ontleding weer tot nikkel en CO. Aan de overkant
25 jaar ontdekte ook per ongeluk carbonyl
ijzer - Fe(CO)5.
Toen BASF een lang vergeten
stalen cilinder met CO, onderaan te vinden
gele vloeistof - ijzerpentacarbonyl,
die geleidelijk uitgroeide tot
het resultaat van een metaalreactie
ijzer met CO onder hoge druk.
Omdat metaalcarbonylen
zeer giftige verbindingen, aanvankelijk
de houding van scheikundigen tegenover hen was erg
cool, maar in de toekomst waren
geweldige eigenschappen ontdekt, waaronder
inclusief katalysator, die bepaalde
hun brede toepassing, vooral in de chemie
koolmonoxide. Merk op dat veel
metalen in fijn gedispergeerde staat
kan direct reageren
met koolmonoxide, maar op deze manier
alleen nikkelcarbonylen ontvangen en
klier. Carbonylen van andere metalen
verkregen door hun verbindingen te herstellen
in aanwezigheid van CO bij hoge
druk.
Verbinding
overgangscarbonylcomplexen
metalen kunnen worden voorspeld op basis van:
18 elektronenregel, volgens welke
het complex zal stabiel zijn als de som
valentie-elektronen van metaal en elektronen,
geleverd door het ligand, in ons geval
CO, zal gelijk zijn aan 18, aangezien in dit geval
elektronische configuratie komt overeen
stabiele configuratie van atomen
edelgassen (krypton).
Molecuul
koolmonoxide is eenzaam
elektronenparen, terwijl een elektronenpaar
op koolstof kan worden verstrekt
om een band met het metaal te vormen
donor-acceptor type. Als
Beschouw bijvoorbeeld de structuur van carbonylen
ijzer en nikkel Fe(CO)5 en
Ni (CO)4.
De ijzer- en nikkelatomen hebben respectievelijk
8 en 10 valentie-elektronen, en om te vullen
elektronenschil van een atoom vóór configuratie
edelgas atoom krypton
10 en 8 elektronen ontbreken, en daarom
bij de vorming van carbonylen tot het ijzeratoom
moet elektronenparen leveren
vijf CO-moleculen en een nikkelatoom
vier.
overgangsperiode
metalen met een oneven aantal valenties
elektronen, vormen binucleaire
carbonyl complexen. Dus, voor kobalt,
met negen valentie-elektronen
naar stabiele elektronische configuratie
negen elektronen missen. enkele kern
complexen door vier paren te nemen
van CO-moleculen zal ongepaard zijn
elektronen, en dergelijke deeltjes van de radicaal
personages met elkaar omgaan.
om een metaal-metaal binding te vormen, en
resulterend in de vorming van een dimeer
Co-complex2(CO)8.
Interactie
of coördinatie van koolmonoxide met
metaal leidt tot een herverdeling
elektronendichtheid niet alleen op CO,
maar ook op metaal, wat een aanzienlijke invloed heeft op
op de reactiviteit van de carbonyl
complex. De meest voorkomende is
lineaire type coördinatie genoemd
CO:
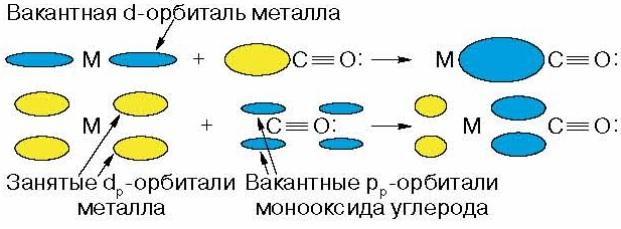
Bij
dit is niet alleen de s-interactie
door een vrij elektronenpaar
koolstof, maar ook p-interactie als gevolg van
elektronenoverdracht van de d-orbitaal van het metaal
tot energetisch beschikbaar vacant
koolstof orbitalen:
Relevantie
Er is dus behoefte aan de ontwikkeling van een dergelijke technologie voor de primaire verwerking en agglomeratie van bruinkool, waarbij rekening wordt gehouden met de specifieke eigenschappen van de oorspronkelijke bruinkool, de omstandigheden van het proces van hydraulisch transport van kolen en de vereisten voor de kenmerken van steenkoolgrondstoffen bij verdere bewerkingen voor de verwerking ervan - pyrolyse, verbranding, vloeibaar maken, briketteren, uitdroging. De oplossing voor dit probleem kan de technologie zijn om steenkool te behandelen met oliereagentia - olie-aggregatie.
Selectieve olie-aggregatie van steenkool combineert een reeks processen voor het structureren van een dunne polydisperse steenkoolfase in een waterig medium met behulp van oliereagentia.De processen van selectieve olieaggregatie van steenkool zijn gebaseerd op het mechanisme van adhesieve interactie tussen een oleofiel steenkooloppervlak en oliën, wat resulteert in de selectieve bevochtiging en aggregatie ervan in een turbulente waterstroom. Hydrofiele deeltjes die niet door olie worden bevochtigd, worden niet opgenomen in de structuur van de aggregaten, waardoor ze kunnen worden geïsoleerd in de vorm van een rotssuspensie.
De behandeling van bruinkool door selectieve olie-aggregatie elimineert de desintegratie en het weken, "behoud" van organisch materiaal in hydrofobe aggregaten, die gemakkelijk worden gedehydrateerd door mechanische methoden en een goede grondstof zijn voor pyrolyse, briketteren en vergassing.
1 Briketteren
Briketteren van steenkool is een fysisch en chemisch proces om een mechanisch en thermisch sterk product van hoge kwaliteit te verkrijgen - een briket met een bepaalde geometrische vorm, grootte en gewicht.
Het technologische proces van het briketteren van bruinkool zonder bindmiddel bestaat uit de volgende bewerkingen: steenkool bereiden in termen van grootte en vochtigheid en persen.
Technologische indicatoren waaraan bruinkoolbriketten moeten voldoen: briketgewicht 100-500 g, mechanische slijtvastheid 75-80%, compressie en buiging respectievelijk 70-90 en 10-15 MPa, vochtopname 3-4%, calorische waarde 24000-30000 kJ/kg, asgehalte 10-25%.[]