Vannets frysepunkt
Fryseprosessen finner sted når den er avkjølt til null grader på Celsius-skalaen. Dette gjelder ikke alt vann. Molekyler fester seg til urenheter, som er partikler av støv, salt osv. Derfor kan rent eller destillert vann, uten nærvær av disse urenhetene, under påvirkning av lave temperaturer i Celsius-kolonnen, forbli i flytende tilstand lenger enn vanlig vann.
Det er også interessant at mens andre stoffer reduseres i volum ved frysing, øker vann tvert imot. Dette er fordi avstanden mellom molekylene utvides under overgangen til fast tilstand. Til tross for at volumet øker, øker ikke massen ved frysing, og veier like mye som varmt vann.
Mange lurer på hvorfor vann ikke fryser under et tykt lag med is. Enhver fysiker vil svare at under et islag fryser ikke vann, siden overflaten av isen fungerer som en varmeisolator.

Hvorfor fryser varmt vann raskere enn kaldt vann?
Det er kjent at varmt eller varmt vann fryser raskere enn kaldt vann. Utrolig men sant. Denne oppdagelsen ble gjort av Erasto Mpemba. Han utførte eksperimenter med å bruke den frosne massen, og fant ut at hvis massen er varm, vil den fryse raskere. Årsaken til dette, som studier har vist, er den høye varmeoverføringen av varmt og varmt vann.

Er frysepunktet til vann og høyde relatert?
Som du vet endrer trykket seg i høyden, så overgangstemperaturen til fast tilstand av alle vandige løsninger i høyden er forskjellig fra temperaturen på en normal overflate.
Eksempler på temperaturendringer i høyden:
- høyde 500 m - frysepunktet for vann er ikke null ° C, som under normale forhold, men i nærvær av allerede en ° C;
- høyde 1500 m - krystallisering skjer i nærvær av omtrent tre ° C, etc.

Hvordan trykk påvirker prosessen med vannkrystallisering
Hvis du forstår forholdet mellom trykk og krystallisering av vann, så er alt ganske enkelt.
Interessant! Jo høyere trykk, desto lavere er transformasjonshastigheten av vann til iskrystaller, og jo høyere kokepunkt!
Det er hele hemmeligheten, og hvis du tenker logisk, går alle indikatorer i motsatt retning med en reduksjon i trykket. Derfor er det vanskelig å lage mat i fjellet, siden temperaturen som vannet koker ikke når hundre grader Celsius. Motsatt smelter is selv ved lave temperaturer.
Krystallisasjonstemperatur av vandige løsninger
Vann er et godt løsemiddel og kombineres derfor lett med andre stoffer. De resulterende løsningene vil selvfølgelig fryse under forskjellige forhold. Vurder et par alternativer for temperaturkriterier for frysing av ulike løsninger basert på vann.
Vann og alkohol. Med en stor mengde alkohol i vannet vil fryseprosessen begynne i nærvær av svært lave temperaturer. For eksempel, ved et forhold på 60% vann til 40% alkohol, vil krystallisering begynne i nærvær av minus 22,5 ° C.
Vann og salt. Temperaturen der frysing oppstår er direkte relatert til saltholdighetsgraden i vannet. Prinsippet er at jo mer salt i vannet, desto lavere er krystalliseringstemperaturen. Hvordan sjøvann fryser er direkte relatert til saltinnholdet.
Vann og brus. Krystallisasjonstemperaturen til løsningen er 44 prosent pluss 7°C.
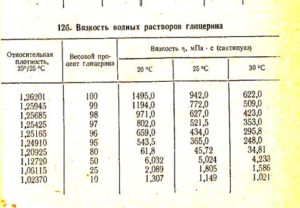
Vann og glyserin, i et forhold på 80% til 20%, hvor 80 er glyserin, og 20 er vann, er tilstedeværelse av -20 ° C nødvendig for å fryse løsningen.
Alle temperaturverdier svinger avhengig av graden av konsentrasjon av fremmede løsninger eller andre stoffer i vannet.
Måling av viskositeten til væsker med et Ostwald-viskosimeter
For å bestemme viskositetskoeffisienten ηhis til den undersøkte væsken ved bruk av et Ostwald kapillærviskosimeter (fig. 6), er det nødvendig å vite:
- η0 er viskositeten til vann,
- t0 er tiden for vannstrømmen mellom merkene a og b,
- tx er strømningstiden for den undersøkte væsken mellom merkene a og b,
- ρ0 er tettheten til vann,
- ρx er tettheten til den undersøkte væsken.
Ris. 6. Ostwald kapillær viskosimeter (a, b, d - merker som begrenser væskenivået, c - kapillær).
Viskositeten til den undersøkte væsken bestemmes av formelen (9).
Arbeidsordre
Oppgave 1. Bestem viskositeten til løsninger med forskjellige konsentrasjoner.
-
Hell vann i benet på viskosimeteret som ikke har kapillær (fig. 6) opp til merket d.
-
Med en pære, sug væsken gjennom kapillæren for å markere en. Etter å ha fjernet pæren, lukk hullet til venstre kne på viskosimeteret (med en hånd, en kork, en vattpinne, etc.) (se fig. 6). Forbered og slå på stoppeklokken, åpne hullet i venstre kne, og slå den av når merke b renner, og bestemmer dermed t0 - tiden for vannstrømmen mellom merkene a og b.
-
Gjenta målingene 4-5 ganger, finn gjennomsnittstiden.
-
Utfør trinn 1-3 for alle testvæsker.
-
Beregn viskositetskoeffisientene til de undersøkte væskene ved å bruke formel (9).
-
Skriv inn dataene i tabell 1.
Tabell 1
| № | Konsentrasjon, % | t1 | t2 | t3 | t4 | t5 | | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 | ||||||||
| 5 | ||||||||
| 6 |
Oppgave 2. Bestem konsentrasjonen av en ukjent løsning.
-
Plott viskositetsforhold vs løsningskonsentrasjon
-
Når du kjenner til viskositeten til den ukjente løsningen, bestemmer du dens konsentrasjon fra grafen.
Tabell 2
Tetthet av vann ved forskjellige temperaturer
| ρ, kg/m3 | t, 0C | ρ, kg/m3 | t, 0C |
| 999,13 | 15 | 998,02 | 21 |
| 998,97 | 16 | 997,80 | 22 |
| 998,80 | 17 | 997,57 | 23 |
| 998,43 | 19 | 997,32 | 24 |
| 998,23 | 20 | 997,07 | 25 |
Tabell 3
Viskositet av vann ved forskjellige temperaturer
| η, Pa.s | t, 0C | η, Pa.s | t, 0C |
| 0,00114 | 15 | 0,00098 | 21 |
| 0,00111 | 16 | 0,00096 | 22 |
| 0,00108 | 17 | 0,00093 | 23 |
| 0,00103 | 19 | 0,00091 | 24 |
| 0,00100 | 20 | 0,00089 | 25 |
Tabell 4
Tetthet av glyserinløsninger i forskjellige konsentrasjoner
| MED, % | ρ, kg/m3 | MED, % | ρ, kg/m3 |
| 5 | 1012,5 | 45 | 1112,5 |
| 10 | 1025,0 | 50 | 1125,0 |
| 15 | 1037,5 | 55 | 1137,5 |
| 20 | 1042,5 | 60 | 1150,0 |
| 25 | 1052,5 | 65 | 1162,5 |
| 30 | 1075,0 | 70 | 1175,0 |
| 35 | 1087,5 | 75 | 1187,5 |
| 40 | 1100,0 | 80 | 1200,0 |
Selvstendig arbeid med temaet:
– løsning av situasjonsproblemer;
- lytte til abstrakter
Endelig kontroll av kunnskap:
– løse problemer for billetter;
– svar på sluttkontrollbilletter;
- oppsummering.
Lekser for å forstå temaet for leksjonen
Kontrollspørsmål om emnet for leksjonen:
1. Hva kalles viskositeten til en væske?
2. Hva slags væskestrøm kalles laminær?Turbulent?
3. Hva kjennetegner Reynolds-formelen?
4. Skriv Newtons formel og forklar den fysiske betydningen av mengdene som inngår i den?
5. Hva er koeffisienten for dynamisk viskositet? I hvilke enheter måles det?
6. Hvilke væsker kalles newtonsk? Hva bestemmer deres viskositetskoeffisient?
7. Hvilke væsker kalles ikke-newtonske Hva bestemmer deres viskositetskoeffisient?
8. Skriv Poiseuille-formelen, forklar den fysiske betydningen av mengdene som inngår i den.
9. Hvilke metoder brukes for å bestemme viskositeten til en væske?
10. Fortell om de reologiske egenskapene til blod og andre biologiske væsker, om bruk av reologiske analyser i medisinen.
11. Hva viser hastighetsgradienten? Vis grafisk.
12. Hvilket fenomen kalles intern friksjon?
Testoppgaver om emnet:
ER PÅFØRINGEN AV GLYSERIN I OPPVARMING BEKREFTIG?
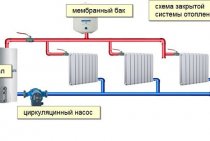
Det stilles ganske høye krav til kjølevæsken for varmesystemer. Den må være brann- og eksplosjonssikker, gi god termisk ytelse, og heller ikke inneholde tilsetningsstoffer som er forbudt for bruk. Etylenglykol eller propylenglykol brukes som grunnlag for produksjon av høykvalitets varmeoverføringsvæske, som også sikrer miljøvennlighet.
Nylig har glyserinbaserte frostvæsker dukket opp på markedet. Dette produktet markedsføres hovedsakelig av små, lite kjente firmaer på frostvæskemarkedet. Spørsmålet oppstår: glyserin og kjølevæske - er deres forening passende?
Og faktisk, de første frostvæskene som dukket opp i vårt land i tjueårene av forrige århundre ble laget på grunnlag av glyserin. Svakhetene deres var utilstrekkelig fluiditet og ekstremt høy viskositet, som pumpene ikke kunne håndtere. De prøvde å løse problemet ved hjelp av alkohol, inkludert metylalkohol. Men sammen med forbedringen i flyten dukket det opp mange problemer. Faktum er at metanol er en sterk psykotrop gift.Som et resultat trosset oppførselen til sjåfører som ufrivillig snuste slik frostvæske noen ganger enhver logikk og utgjorde en fare for andres helse og liv. I tillegg har metylalkohol et lavt kokepunkt og når det fordamper, øker viskositeten til produktet umiddelbart. Problemet ble løst først da etylenglykol ble grunnlaget for kjølevæsken. Og på slutten av trettitallet, begynnelsen av førtitallet, erstattet frostvæsker med etylenglykol nesten fullstendig glyserin-metanol.
I tillegg er glyserin termisk ustabil, brytes ned under langvarig oppvarming, med dannelse av et giftig flyktig stoff - akrolein, som har en skarp ubehagelig lukt som forårsaker riving. Nedbrytningsprodukter er giftige, og utfelling øker den korrosive aktiviteten til kjølevæsken. Som et resultat øker kravene til tetninger og deler laget av ikke-polar gummi og plast. I tillegg til høy viskositet skummer glyserin også sterkt, noe som fører til lufting av systemet og dårlig varmeavledning.
Produsenter av glyserinkjølevæsker prøver å kompensere for alle de ovennevnte ulempene ved å legge til forskjellige tilsetningsstoffer, inkludert alifatiske alkoholer - metanol, etanol, propanol. Disse alkoholene kan redusere viskositeten eller tettheten til frostvæsken betydelig. Men de koker allerede ved temperaturer over 65 grader, noe som fører til en forringelse av kjølevæskens termiske ytelse. Disse alkoholene er i stand til å løse opp gummi og polymerer, og er også utsatt for kavitasjon og sterk fordampning. I tillegg er metanol en sterk gift og er forbudt for bruk i produksjon av frostvæsker.
Å sikre kvaliteten på glyserinkjølevæsker, spesielt med metanol, krever tilsetning av dyre additivpakker til blandingen. Og selv om kostnadene for glyserin nå er lavere enn kostnadene for glykoler, er tilsetningspakken for å lage kvalitetsglyserin varmeoverføringsvæsker dyrere enn tilsetningspakken for frostvæske basert på etylenglykol og propylenglykol. Og hvis prisen på glyserin frostvæske på markedet er lavere enn for glykol, betyr det at produsenten ganske enkelt har spart på kvalitet og ikke lagt til de nødvendige dyre tilsetningsstoffene til produktet!
Så valget er opp til kjøperen: enten en pålitelig og velprøvd kjølevæske basert på glykoler, eller en glyserin "pig in a poke".
Valget av selskapet vårt, som de fleste av de ledende produsentene av frostvæsker, er grunnleggende entydig - glyserin kan ikke brukes i sin rene form, men blandet med metanol er farlig og kriminelt!
Hovedargumentet som bekrefter vår posisjon i dette spørsmålet er at i et hvilket som helst viktig og stort anlegg er bruk av glyserin i varme- og kjølesystemer IKKE TILLATT av eksisterende standarder!
MEG
Etylenglykol er et produkt av etylenoksidhydrering i nærvær av svovelsyre eller fosforsyre. Refererer til flerverdige alkoholer. Fryser ikke ved lave temperaturer og senker frysepunktet til vann. I stand til å absorbere vann fra luften.
Den selges i metall- og plastfat, opptil 227 liter. Samt plastkuber 1000l.
Det er nødvendig å lagre stoffet i en forseglet beholder laget av aluminium eller stål med anti-korrosjonsbeskyttelse i et lukket lager uten oppvarming. Holdbarheten for høyeste klasse er 12 måneder, for første klasse - 3 år fra produksjonsdatoen.
Navn på indikator Norm
Utseende, lukt Klar, fargeløs væske med en oljeaktig tekstur. Uten lukt.
Løselig i vann, alkoholer, toluen, benzen
Tetthet 1,112 g/cm?.
Smeltepunkt 12,9 grader Celsius
Kokepunkt 197,3 grader Celsius
applikasjon
På grunn av sin evne til å redusere frysepunktet, brukes monoetylenglykol i produksjon av frostvæske og bremsevæske for biler, samt i produksjon av cellofan og polyuretan. I mindre grad brukes det til produksjon av blekk og trykkfarger.
Fareklasse
Refererer til brennbare stoffer. Selvantenning skjer ved en temperatur på 380 grader, et dampglimt ved oppvarming til 120 grader. Giftig. Svelging er ikke tillatt. Damp er mindre skadelig.
Glyserol
Kjemisk formel: HOCH2CH(OH)CH2OH
Internasjonalt navn: Glyserin
CAS NR: 56-81-5
Kvalifikasjon: Imp. "h", GOST 6259-75
Utseende: klar, luktfri væske
Pakking: 25 kg bokser, 250 kg fat, 1500 kuber
Lagringsforhold: i et ventilert tørt rom ved lav temperatur
Synonymer: 1,2,3-trioksypropan
Vi tilbyr Glyserin i bokser, fat, terninger til konkurransedyktige priser.
| Spesifikasjon | |
| Molekylær vekt | 92.10 |
| Grunnstoff, ikke mindre enn | 99,5 % (faktisk 99,8 %) |
| Askeinnhold, ikke mer | 0,01 % (faktisk mindre enn 0,1 %) |
| Vanninnhold, ikke mer | 0,5 % (faktisk 0,1 %) |
| Innhold av klorider, ikke mer | 0,001 % |
| Sulfatinnhold, ikke mer | 0,002 % |
| Tungmetaller, ikke mer | 0,0005 % (faktisk mindre enn 0,00005 %) |
| Klorforbindelser (som CL), ikke mer | 0,003 % |
| Arsenikk, ikke mer | 0,00015 % (faktisk mindre enn 0,00001 %) |
| Farge (APHA), ikke mer | 20 (faktisk mindre enn 10) |
Glyserin er en fargeløs, hygroskopisk, viskøs, luktfri, søtsmakende væske. Blandbar i alle forhold med vann, etanol, metanol, aceton, uløselig i kloroform og eter. Når glyserol blandes med vann, frigjøres varme og det oppstår sammentrekning (volumreduksjon). Når glyserol interagerer med halogenhydrogensyrer eller fosforhalogenider, dannes mono- eller dihalogenhydriner; med uorganiske og karboksylsyrer - komplette og ufullstendige estere, med dehydrering - akrolein. Glyserol kan oksideres, og avhengig av oksidasjonsmidlets betingelser og natur kan glyseraldehyd, glyserinsyre, tartronsyre, dihydroksyaceton, mesoksalsyre oppnås. Glyserin finnes i naturlig fett og oljer som blandede triglyserider av karboksylsyrer.
applikasjon Glyserin er mye brukt • i den farmasøytiske industrien, for eksempel for produksjon av nitroglyserin, medisinske salver; • i næringsmiddelindustrien, for eksempel i produksjon av likører, konfekt; • i kosmetikkindustrien, i produksjon av parfyme og kosmetikk • i produksjon av glyptalharpiks; • som et mykgjøringsmiddel for tekstiler, lær, papir; • som en komponent i emulgatorer, frostvæsker, smøremidler, skokrem, såper og lim, • som råstoff i produksjon av polyalkoholer, som brukes i ulike skum. • som mykner for cellofan o.l.
Ved hvilken temperatur fryser vann i varmerør i et bolighus
Hvis temperaturen i huset forblir -10 i flere dager, og det er vann i rørene, kan det fryse, noe som vil føre til brudd på rørene. Mange har sikkert sett moderne varmebatterier med vannavløpsfunksjon. Nesten alle moderne batterier er utstyrt med evnen til å tømme vann. Dette gjøres for at i nødstilfelle, når temperaturen i huset er -10, fryser ikke vannet og river ikke rørene. Hvis situasjonen har kommet til dette, sympatiserer vi veldig med deg, mest sannsynlig må du bytte batteriene, siden under frysing av vann har det sannsynligvis oppstått mikrosprekker som gjør videre drift av disse batteriene farlig.
Hvorfor kan vann fryse i rør. Hvis det i løpet av fyringssesongen, akkurat når batteriene fylles med vann, oppstår et sammenbrudd og vannet kjøles ned, og temperaturen synker raskt ute, kan dette føre til at rørene fryser.
Vi har allerede svart på spørsmålet ved hvilken temperatur vann fryser, som et eksperiment, ta et lite glass, fyll det halvveis med vann og legg det i fryseren i flere timer, to timer er nok til at vannet delvis blir til is.
Vann er et av de viktigste stoffene på planeten vår. Den har mange egenskaper som gjør den til en viss grad unik. En av de mest kjente egenskapene som selv et lite barn vet om, er frysing av vann.Det er kjent at 0 grader Celsius er krystalliseringstemperaturen til vann. Men ikke alt er så enkelt. Vi vil vurdere noen av finessene i denne prosessen videre.

Tetthet av glyserinløsning ved 25
Det aritmetiske gjennomsnittet av tetthetene av alkohol og glyserol.
209,4. 1.047. 25.265.0. 1.060. ... Se hva som er tettheten til vandige løsninger av glyserin i andre ordbøker E236 Fil Maursyre.svg Strukturformel for maursyre Maursyre metansyre er den første ...
Hva er tettheten av glyserin ved 17 grader Celsius?
8
Tetthet ved 25 C, g cm. ... En løsning av glyserin i en konsentrasjon på 25 % eller mer avslører ikke mikrobiell forurensning, i mer fortynnede løsninger formerer mikroorganismer seg godt i den.
3,14
Hvilken væske har høyere tetthet, glyserin eller alkohol? forklare
Ssss
TK-april på nettstedet i hele Russland. Konsentrasjon, tetthet og brytningsindeks for løsninger av glyserol 15 С. … 1,0594. 1,3633. 25.1.0620.
Beregn molmassen til begge stoffene. For alkohol er det mindre (92 g/mol mot 46 g/mol for alkohol), og tettheten er tilsvarende lavere. Når det gjelder etylalkohol.
Hva er vitsen med slike spørsmål? Informasjon finnes i søkemotorer
Det aritmetiske gjennomsnittet av tetthetene til komponentene i blandingen.
Bestem hvilken masse glyserol med en tetthet på 1,26 g ml som skal tas for å fremstille en vandig løsning c.42. ... 111 g ftalsyreanhydrid og 46 g glyserin med en tetthet på 28 V legges i et glassbeger med en kapasitet på 0,25 l.
Hvordan beregne tettheten og viskositeten til en væske som inneholder vann, alkohol og glyserin?
Til dette selges reometre. du trenger ikke telle noe. bare fryse.
trietylenglykol. propylenglykol. Glyserol. … propylenglykol 40 %. -25 C. ... Tettheten til vandige løsninger av etylenglykol ved forskjellige temperaturer.
Du må vite prosentandelen av alle komponentene i blandingen (minst!)
Aldri. Er, se etter data mottatt av noen.
Vennligst hjelp, vil et stykke is flyte i bensin, parafin, glyserin? Hvorfor?
Det vil være i glyserin, det flyter ikke i whisky - tettheten er omtrent det samme som bensin
Det øker også tettheten til den ferdige løsningen og forbedrer kvaliteten på boblene. ... Glyserinløsning 25g flaskeTula Pharmaceutical Factory LLC. … Natriumtetraboratløsning i glyserin hetteglass 20 % 30 g, Samara FF, Samara Russland.
Is er mindre tett enn olje, så det blir det.
Sammenlign tettheten av is med tettheten til disse væskene. hvis tettheten av is er mindre, vil den flyte, hvis den er mer, vil den synke.
Vet ikke. avhenger av hvilket stykke. hvis det er nok luft i isen til å holde den på overflaten, vil den flyte, og hvis ikke, så vil den ikke. prøv selv. parafin er billig.
Avhengig av hvilken temperatur denne isen avkjøles til
Kokepunktet for vandige løsninger av glyserin synker med en reduksjon i konsentrasjonen av glyserol med et innhold på 5% vann, kokepunktet er 160-161, dens tetthet er 1,26362 g cm3. … 25 25 C . ZnCl2.
Jeg har aldri sett is flyte i bensintanken og dunken. Og det er han absolutt))). Så han er nok på bunnen. Jeg så glyserin bare i et hetteglass og i varme))).
Oi!
X mengde fortynnet glyserol, g En tetthet av destillert glyserol, g ml ... Løsninger av glyserol med en konsentrasjon på 25 % og over er ikke utsatt for mikrobiell forurensning, mer fortynnede løsninger er ...
Vil et stykke is flyte i bensin, parafin, glyserin?
Finn ut tettheten og det er det!
Tetthet av vandige løsninger av alkoholer. Tettheter av vandige løsninger g cm3 ved 20 C er gitt for følgende stoffer: etanol, 1-propanol, 2-propanol, etylenglykol, glyserol, D-mannitol.
Ja)))
Hvis tettheten til isen er mindre enn væskens tetthet, vil isen flyte
Hva er tettheten til glyserin ved en temperatur på 24 gr. MED?
Glyserin grader Celsius020406080100120140169180Tetthet g/cm3126712591250123812241208118811631126
For en temperatur på 24 grader = bestemme ved interpolasjon mellom 20 og 40 grader
Beregn kokepunktet til en 8 % løsning av glyserol C3H6O3 i aceton. Svaret er 57,7oC. 4.En løsning, hvorav 100 ml inneholder 2,3 g ... Ta tettheten til løsningen lik én. Svar 608 Pa. Billett 14 25 1. Hvor mange gram BaCl2 2H2O ...
Spørsmål om kjemi))) Og fysikk. Hvilken væske er tettere enn vann og leder også elektrisitet, men ikke metall?
Glyserin, etylenglykoler, formamider, butyrolakton, nesten alle syrer, aminer. og mye mer.
Svovelsyrekonsentrasjon, masseprosent. Tetthet ved 25 C, g cm ... 25,60-0,1950 0,000 8 - relativ fuktighet, % - brytningsindeks for en vandig løsning av glyserol ved 25 C for linje D natrium - løsningstemperatur, C ...