Exploração

Nas baterias de fluxo de vanádio, ambos os eletrodos de referência são conectados adicionalmente a tanques de armazenamento e bombas para que grandes volumes de eletrólito possam circular pela célula. A circulação de eletrólito líquido é um pouco difícil e limita o uso de baterias de fluxo de vanádio em indústrias que exigem mobilidade, tornando-as eficazes em grandes edifícios estacionários.
Quando uma bateria de vanádio é carregada, os íons VO2+ no eletrodo de referência carregado positivamente se transformam em íons VO2+ quando os elétrons são separados do terminal positivo da bateria. Da mesma forma, no eletrodo de referência negativa, os elétrons convertem os íons V3+ em V2+. Durante a descarga, este processo é revertido, resultando em uma tensão de circuito aberto de 1,41 V a 25°C.
Outras propriedades úteis das baterias de fluxo de vanádio incluem uma resposta muito rápida às mudanças de carga e uma capacidade de sobrecarga extremamente alta. Uma pesquisa da Universidade de New South Wales mostrou que eles podem atingir tempos de resposta de menos de meio milissegundo em 100% de mudanças de carga e suportar 400% de sobrecarga por mais de 10 segundos. O tempo de resposta é na maioria dos casos limitado pelo equipamento elétrico. As baterias de vanádio à base de ácido sulfúrico só funcionam em temperaturas de 10-40C. Se a temperatura estiver abaixo dessa faixa, os íons de ácido sulfúrico cristalizam. A eficiência no movimento alternativo no uso diário permanece no nível de 65-75%.
Características de carga e descarga
Os algoritmos de carregamento dependem diretamente de como a bateria está organizada e a que tipo ela pertence. Por exemplo, algumas baterias podem reabastecer com segurança sua capacidade a partir de fontes de tensão constante. Outros trabalham apenas com uma fonte de corrente ajustável que pode alterar os parâmetros dependendo do nível de carga.
Um processo de carregamento mal organizado pode danificar a bateria. Em casos extremos, a bateria pode inflamar ou explodir. Existem baterias inteligentes equipadas com dispositivos de monitoramento de tensão. Os principais parâmetros que devem ser levados em consideração ao operar baterias galvânicas reversíveis são:
- Vida útil. Mesmo com o manuseio adequado, o número de ciclos de carga de uma bateria é limitado. Diferentes sistemas de bateria nem sempre se desgastam pelos mesmos motivos. Mas, em geral, a vida útil da bateria é limitada principalmente pelo número de ciclos completos de carga e descarga e, em segundo lugar, pela vida útil do projeto, sem referência à intensidade de uso.
- Hora de carregar. O design fundamental da bateria não implica carregar em uma velocidade arbitrariamente alta: a resistência interna da célula galvânica levará à conversão do excesso de corrente de carga em calor, o que pode danificar irreversivelmente o dispositivo. Do ponto de vista físico, o tempo de carregamento é limitado pela taxa máxima de difusão do material ativo através do eletrólito.De forma simplista, podemos supor que a restauração da capacidade total em uma hora é um bom indicador.
- Profundidade de descarga. Especificado como uma porcentagem da potência nominal. Descreve a capacidade utilizável. Para diferentes tipos de baterias, o nível de descarga operacional recomendado pode variar. Devido a mudanças na operação ou envelhecimento, o indicador de profundidade máxima perde seu valor original.
processo de difusão.
Devido ao processo de difusão, ao alinhamento da densidade do eletrólito na cavidade da caixa da bateria e nos poros da massa ativa das placas, a polarização do eletrodo pode ser mantida na bateria quando o circuito externo é desligado.
A taxa de difusão depende diretamente da temperatura do eletrólito, quanto maior a temperatura, mais rápido o processo ocorre e pode variar muito no tempo, de duas horas a um dia. A presença de dois componentes do potencial do eletrodo em condições transitórias levou à divisão em EMF de equilíbrio e não-equilíbrio da bateria. O equilíbrio EMF da bateria é afetado pelo conteúdo e concentração de íons de substâncias ativas no eletrólito, bem como pelas propriedades químicas e físicas das substâncias ativas. O papel principal na magnitude do EMF é desempenhado pela densidade do eletrólito e a temperatura praticamente não o afeta. A dependência de EMF na densidade pode ser expressa pela fórmula:
A fem da bateria não é igual à tensão da bateria, que depende da presença ou ausência de carga em seus terminais.
administrador25/07/2011
Um comentário
Nome *
Local
Este site usa o Akismet para combater o spam. Descubra como seus dados de comentários são processados.
« Tacômetro mecânico
Voltagem da bateria "
Tag
VAZ, VAZ avarias Sensores Ignição Dispositivos Injetores Esquemas de arranque Carros elétricos Fonte de alimentação vaz 2110 gazelle gazelle registradores de negócios reparação de automóveis
Entradas recentes
- Sensores no carro: tipos e finalidade
- O maior carro elétrico do mundo EDumper,
- Luzes de lazer.
- Vantagens e desvantagens das lâmpadas halógenas
- O dispositivo e o princípio de operação dos sensores de estacionamento
Arquivos
Arquivos Selecione De Setembro De 2019 Agosto De 2017 De Maio De 2017 De Março De Outubro De 2016 De Outubro De 2016 De Agosto De 2016 De Julho De 2016 De Julho De 2016 De Julho De 2015 2015 de Julho de 2015 2015 de Julho de 2015 de Julho de 2015 Janeiro 2015 Dezembro 2014 Novembro 2014 Outubro 2014 Setembro 2014 Agosto 2014 Julho 2014 Junho 2014 Maio 2014 Abril 2014 Fevereiro 2014 Janeiro 2014 Janeiro 2014 Dezembro 2013 Novembro 2013 Outubro 2013 Agosto 2013 Junho 2013 Maio 2013, Março 2012, 2012, 2013, 2012 2012, 2012, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011 Setembro de 2012, 2011, 2011, 2011, 2011, 2011, 2011
Categorias
- Bateria do acumulador
- Vídeo
- Gerador
- Sensores
- Diagnóstico
- Ignição
- notícias
- Equipamento
- Dispositivos
- Reparar
- Vela de ignição
- Iniciante
- Esquema
- Dispositivos
- carros elétricos
- Fonte de energia
Estamos nas redes sociais
Auto Electrician@ Todos os direitos reservados. Ao copiar materiais do site, você deve fornecer um link para o site.
Dispositivo e princípio de operação
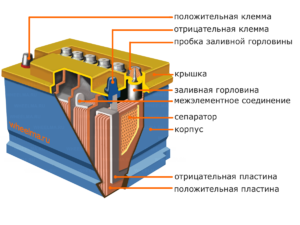
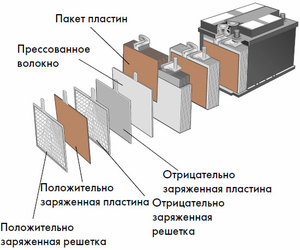
Cada uma dessas células tem um cátodo (eletrodo positivo) e um ânodo (negativo). Esses eletrodos são separados por um eletrólito que garante a troca de íons entre eles. Os materiais do eletrodo e a composição do eletrólito são escolhidos para fornecer força eletromotriz suficiente entre os terminais da bateria.
Como os eletrodos contêm um potencial limitado de energia química, a bateria se esgotará durante a operação. O tipo de células galvânicas, que é adaptado para reabastecimento após uma descarga parcial ou completa, é chamado de bateria. Um conjunto dessas células interconectadas é uma bateria.A operação da bateria envolve uma mudança cíclica de dois estados:
- Carregamento - a bateria funciona como um receptor de eletricidade, dentro das células a energia elétrica é realizada em transformações químicas.
- Descarga - o dispositivo funciona como uma fonte de corrente elétrica, convertendo a energia das reações químicas em energia elétrica.
Áreas de uso
A característica de capacidade ultra-alta das baterias redox de vanádio as torna adequadas para uso em indústrias que exigem alto armazenamento de energia. Por exemplo, ajudar a equilibrar o volume de produção de tais fontes de energia, como eólica ou solar, ou ajudar geradores a absorver grandes surtos de energia quando necessário, ou equilibrar oferta e demanda de energia para áreas remotas.
As características limitadas de autodescarga das baterias redox de vanádio as tornam úteis em indústrias onde as baterias devem ser armazenadas por longos períodos de tempo com manutenção e prontidão mínimas. Isso levou ao seu uso em alguns tipos de eletrônica militar, por exemplo, nos sensores do sistema de mineração GATOR. Sua capacidade de percorrer e permanecer em zero os torna adequados para aplicações solares e indústrias onde as baterias devem começar o dia vazias e recarregar com base na carga e no clima. Por exemplo, as baterias de íon de lítio são frequentemente danificadas quando podem descarregar abaixo de 20% de seu volume, portanto, geralmente operam na faixa de 20 a 100%, o que significa que podem usar apenas 20% de sua capacidade nominal.
Seu tempo de resposta extremamente rápido também os torna praticamente indispensáveis para fontes de alimentação ininterruptas, onde podem ser usados no lugar de baterias de chumbo-ácido e até geradores a diesel. Além disso, o tempo de resposta rápido os torna adequados para controle de frequência. No momento, nem o UPS nem as medidas de gerenciamento de frequência são eficazes por si só, mas é provável que a bateria seja capaz de encontrar aplicações nessas indústrias quando capitalizada de várias fontes de financiamento. Além disso, esses recursos tornam as baterias redox de vanádio uma solução eficaz de "peça única" para pequenas redes elétricas que dependem de operação confiável, controle de frequência e necessidades de comutação de carga (como alta penetração de energias renováveis, cargas altamente flutuantes ou o desejo de otimizar a eficiência do gerador alterando o tempo de resposta).
As maiores baterias redox de vanádio em funcionamento
Subestação "Minami Hyakita":
- Data de lançamento: dezembro de 2015
- Energia: 60 MWh
- Potência: 15 MW
- Tempo de trabalho: 4 horas
- País: Japão
Fedorento, Província de Liaoning
- Data de lançamento: N/A
- Energia: 10 MWh
- Potência: 5 MW
- Tempo de trabalho: 2 horas
- País: China
Parque Eólico Tomamae
- Data de lançamento: 2005
- Energia: 6 MWh
- Potência: 4 MW
- Tempo de trabalho: 1 hora e 30 minutos
- País: Japão
Projeto Zhangbei
- Data de lançamento 2016
- Energia: 8 MWh
- Potência: 2 MW
- Tempo de trabalho: 4 horas.
- País: China
Projeto SnoPUD MESA 2
- Data de lançamento: março de 2017
- Energia: 8 MWh
- Potência: 2 MW
- Tempo de trabalho: 4 horas.
- País: EUA
Subestação em Escondido
- Data de lançamento: 2017
- Energia: 8 MWh
- Potência: 2 MW
- Tempo de trabalho: 4 horas.
- País: EUA
Subestação em Pullman, Washington
- Data de lançamento: abril de 2015
- Energia: 4 MWh
- Potência: 1 MW
- Tempo de trabalho: 4 horas
- País: EUA
Em 2018, espera-se que o desenvolvimento de uma bateria redox de vanádio seja concluído na China. Sua energia será de 800 MWh, potência - 200 MW e tempo de operação - 4 horas.
Termos
- Sequencial - os elementos seguem um após o outro.
- A força eletromotriz (EMF) é a tensão gerada por uma bateria ou força magnética de acordo com a lei de Faraday.
- Paralelo - Os componentes elétricos são dispostos de modo que a corrente flua ao longo de dois ou mais caminhos.
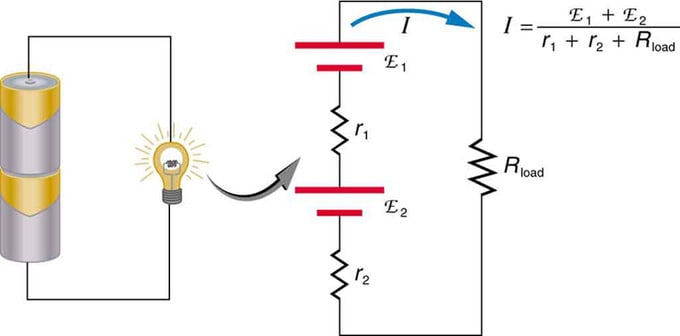
Se você estiver usando várias fontes de tensão, elas podem ser conectadas em série ou em paralelo. Com a versão em série, eles são sintonizados na mesma direção, a resistência interna é acrescida e a força eletromotriz é adicionada algebricamente. Tipos semelhantes são comuns em lanternas, brinquedos e uma variedade de outros aparelhos. As células são colocadas em série para aumentar a fem total.
Conexão serial de duas fontes de tensão na mesma direção. O diagrama mostra uma lanterna com duas células e uma lâmpada
Bateria - conexão múltipla de elementos volts. Mas há uma desvantagem na conexão serial, pois as resistências internas são adicionadas. Às vezes isso cria problemas. Digamos que você tenha duas baterias de 6V que você colocou em vez dos 12V normais. Como resultado, você adicionou não apenas o EMF, mas também a resistência interna de cada bateria.
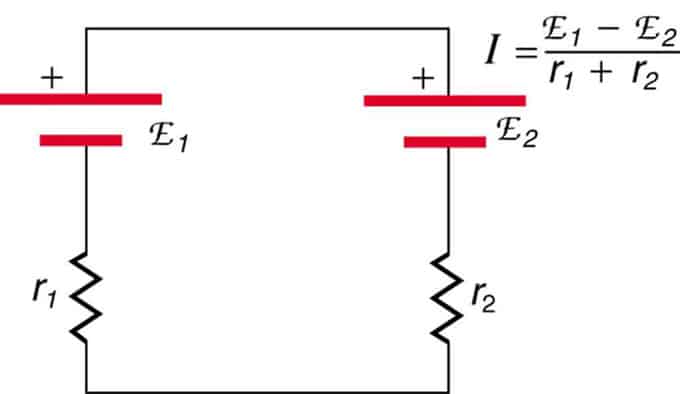
Se as células estiverem localizadas em oposição (uma localizada atrás da outra), o EMF total diminuirá.
São duas fontes de tensão conectadas em série com emissões opostas. A corrente flui na direção de maior CEM e é limitada pela soma das resistências internas. Um exemplo é um carregador. Deve ter mais fem que a bateria
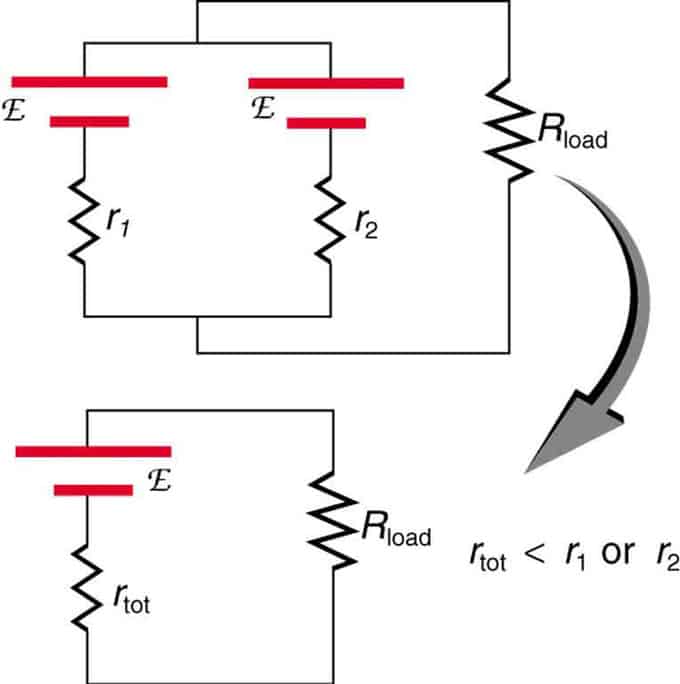
Se duas fontes com a mesma força eletromotriz estiverem localizadas em paralelo e conectadas à resistência de carga, a EMF total permanece a mesma das individuais. No entanto, a resistência interna total será reduzida. Acontece que a versão paralela pode gerar mais corrente.
Duas fontes de tensão com um único EMF são combinadas em conexão paralela. Eles formam um EMF, mas têm menos resistência total do que individualmente. Combinações semelhantes são usadas se você precisar obter mais corrente.
| Visão geral |
|
| Ligação em paralelo e em série de resistências |
|
| Regras de Kirchhoff |
|
| Voltímetros e amperímetros |
|
| Circuitos RC |
|
Visão histórica
O desenvolvimento da primeira célula galvânica é creditado ao físico italiano Alessandro Volta. Ele realizou uma série de experimentos com fenômenos eletroquímicos durante a década de 1790 e por volta de 1800 criou a primeira bateria, que seus contemporâneos chamavam de "coluna voltaica". O aparelho consistia na alternância de discos de zinco e prata separados por camadas de papel ou tecido que eram embebidas em solução de hidróxido de sódio.
Esses experimentos se tornaram a base para o trabalho de Michael Faraday sobre as leis quantitativas da eletroquímica. Ele descreveu o princípio de funcionamento da bateria e, com base no trabalho do cientista, foram criadas as primeiras células elétricas comerciais. A evolução posterior ficou assim:
- Em 1836, o químico britânico John Daniel apresentou um modelo melhorado da célula, consistindo de eletrodos de cobre e zinco imersos em ácido clorídrico. O elemento de Daniel foi capaz de fornecer tensão constante incomparavelmente mais eficiente do que os dispositivos de Volt.
- 1839 Mais progressos foram feitos pelo físico Grove com sua célula de dois fluidos, consistindo de zinco imerso em ácido sulfúrico diluído em um recipiente poroso. Este último separou o ácido sulfúrico de um recipiente contendo ácido nítrico com um cátodo de platina colocado nele. O ácido nítrico serviu como um agente oxidante para evitar a perda de voltagem devido ao acúmulo de hidrogênio no cátodo.O químico alemão Robert Bunsen substituiu a platina por carbono barato na célula Grove e, assim, promoveu a ampla aceitação desse tipo de bateria.
- Em 1859, Gaston Plante inventou a célula de chumbo-ácido, precursora da moderna bateria de carro. O dispositivo de Plante foi capaz de produzir uma corrente extraordinariamente grande, mas foi usado apenas para experimentos em laboratórios por quase duas décadas.
- 1895-1905 anos. Invenção de elementos alcalinos de níquel-cádmio e níquel-ferro. Isso possibilitou a criação de sistemas com um número significativo de ciclos de carga-descarga.
- Desde a década de 1930, começou o desenvolvimento de baterias alcalinas prata-zinco e mercúrio-zinco, que forneciam alta densidade de energia por unidade de peso e volume.
- Desde meados do século 20, os avanços na tecnologia de fabricação e o advento de novos materiais levaram a baterias ainda mais potentes e compactas. O mais notável foi a introdução de baterias de níquel-hidreto metálico e lítio no mercado.
Carregar baterias
Artigo principal: Carregador
À medida que a energia química se esgota, a tensão e a corrente caem e a bateria deixa de funcionar. Você pode carregar a bateria (bateria de baterias) de qualquer fonte DC com uma tensão mais alta, limitando a corrente. A mais comum é a corrente de carga (em amperes), proporcional a 1/10 da capacidade nominal condicional da bateria (em amperes-hora).
No entanto, com base na descrição técnica distribuída pelos fabricantes de baterias elétricas amplamente utilizadas (NiMH, NiCd), pode-se supor que este modo de carga, comumente referido como padrão, é calculado com base na duração de uma jornada de trabalho de oito horas, quando a bateria, descarregada no final da jornada de trabalho, é conectada ao carregador de rede antes do início de uma nova jornada de trabalho. O uso de tal modo de carga para esses tipos de baterias com uso sistemático permite manter um equilíbrio qualidade-custo na operação do produto. Assim, por sugestão do fabricante, este modo só pode ser utilizado para baterias de níquel-cádmio e níquel-hidreto metálico.
Muitos tipos de baterias têm limitações diferentes que devem ser levadas em consideração durante o carregamento e uso subsequente, por exemplo, as baterias NiMH são sensíveis à sobrecarga, as baterias de lítio são sensíveis à descarga excessiva, tensão e temperatura. As baterias NiCd e NiMH possuem o chamado efeito memória, que consiste em uma diminuição da capacidade quando o carregamento é realizado quando a bateria não está completamente descarregada. Além disso, esses tipos de baterias têm uma autodescarga perceptível, ou seja, perdem gradualmente a carga sem serem conectadas à carga. Para combater esse efeito, a recarga por gotejamento pode ser usada.
Métodos de carregamento da bateria
Vários métodos são usados para carregar baterias; Geralmente, o método de carregamento depende do tipo de bateria.
- Carga DC lenta
Carregue com uma corrente contínua proporcional a 0,1-0,2 da capacidade nominal condicional Q por cerca de 15-7 horas, respectivamente.
O método de carregamento mais longo e seguro. Adequado para a maioria dos tipos de baterias.
- carga rápida
Carregue com corrente contínua proporcional a 1/3 Q por cerca de 3-5 horas.
- Carga acelerada ou "delta-V"
Uma carga com uma corrente de carga inicial proporcional à capacidade nominal nominal da bateria, na qual a tensão da bateria é constantemente medida e a carga termina após a bateria estar totalmente carregada. O tempo de carregamento é de cerca de uma hora e meia. A bateria pode superaquecer e até destruí-la.
- carga reversa
É realizado alternando pulsos de carga longos com pulsos de descarga curtos. O método inverso é mais útil para carregar baterias NiCd e NiMH, que são caracterizadas pelos chamados.n. "efeito memória".