Punctul de îngheț al apei
Are loc procesul de congelare când este răcit la zero grade pe scara Celsius. Acest lucru nu se aplică tuturor apei. Moleculele se atașează de impurități, care sunt particule de praf, sare etc. Prin urmare, apa pură sau distilată, fără prezența tocmai a acestor impurități, sub influența temperaturilor scăzute din coloana Celsius, poate rămâne în stare lichidă mai mult timp decât apa obișnuită.
De asemenea, este interesant că, în timp ce alte substanțe scad în volum la îngheț, apa, dimpotrivă, crește. Acest lucru se datorează faptului că distanța dintre molecule se extinde în timpul tranziției la o stare solidă. În ciuda faptului că volumul crește, masa nu crește la îngheț și cântărește la fel de mult ca apa caldă.
Mulți oameni se întreabă de ce apa nu îngheață sub un strat gros de gheață. Orice fizician va răspunde că sub un strat de gheață, apa nu îngheață, deoarece suprafața gheții servește ca izolator termic.

De ce apa fierbinte îngheață mai repede decât apa rece?
Se știe că apa fierbinte sau caldă îngheață mai repede decât apa rece. Incredibil, dar adevărat. Această descoperire a fost făcută de Erasto Mpemba. El a efectuat experimente folosind masa înghețată și a descoperit că, dacă masa este caldă, atunci va îngheța mai repede. Motivul pentru aceasta, după cum au arătat studiile, este transferul ridicat de căldură al apei calde și calde.

Sunt legate punctul de îngheț al apei și altitudinea?
După cum știți, presiunea se schimbă la altitudine, astfel încât temperatura de tranziție la starea solidă a tuturor soluțiilor apoase la altitudine diferă de temperatura de pe o suprafață normală.
Exemple de schimbări de temperatură la altitudine:
- altitudinea 500 m - punctul de îngheț al apei nu este zero °C, ca în condiții normale, ci în prezența a deja un °C;
- înălțime 1500 m - cristalizarea are loc în prezența a aproximativ trei ° C etc.

Cum afectează presiunea procesul de cristalizare a apei
Dacă înțelegeți relația dintre presiunea și cristalizarea apei, atunci totul este destul de simplu.
Interesant! Cu cât presiunea este mai mare, cu atât rata de transformare a apei în cristale de gheață este mai mică și punctul de fierbere este mai mare!
Acesta este tot secretul și, dacă gândiți logic, atunci cu o scădere a presiunii, toți indicatorii merg în direcția opusă. Prin urmare, este dificil să gătești ceva la munte, deoarece temperatura la care fierbe apa nu ajunge la o sută de grade Celsius. În schimb, gheața se topește chiar și la temperaturi scăzute.
Temperatura de cristalizare a soluțiilor apoase
Apa este un solvent bun și, prin urmare, se combină ușor cu alte substanțe. Soluțiile rezultate, desigur, se vor îngheța în diferite condiții. Luați în considerare câteva opțiuni pentru criteriile de temperatură pentru înghețarea diferitelor soluții pe bază de apă.
Apă și alcool. Cu o cantitate mare de alcool în apă, procesul de congelare va începe în prezența unor temperaturi foarte scăzute. De exemplu, la un raport de 60% apă la 40% alcool, cristalizarea va începe în prezența a minus 22,5 ° C.
Apă și sare. Temperatura la care are loc înghețul este direct legată de gradul de salinitate al apei. Principiul este că, cu cât este mai multă sare în apă, cu atât temperatura de cristalizare este mai mică. Modul în care apa de mare îngheață este direct legat de conținutul de sare.
Apă și sifon. Temperatura de cristalizare a soluției este de 44 la sută, plus 7°C.
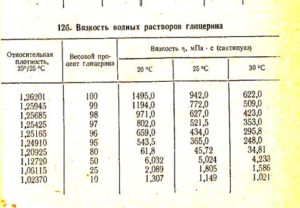
Apa și glicerina, într-un raport de 80% până la 20%, unde 80 este glicerina și 20 este apă, este necesară prezența a -20 ° C pentru a îngheța soluția.
Toate valorile temperaturii fluctuează în funcție de gradul de concentrare a soluțiilor străine sau a altor substanțe din apă.
Măsurarea vâscozității lichidelor cu un viscozimetru Ostwald
Pentru a determina coeficientul de vâscozitate ηhis al lichidului investigat cu ajutorul unui vâscozimetru capilar Ostwald (Fig. 6), este necesar să se cunoască:
- η0 este vâscozitatea apei,
- t0 este timpul curgerii apei între marcajele a și b,
- tx este timpul de curgere a lichidului investigat între reperele a și b,
- ρ0 este densitatea apei,
- ρx este densitatea lichidului investigat.
Orez. 6. Vâscozimetru capilar Ostwald (a, b, d - marcaje limitând nivelul lichidului, c - capilar).
Vâscozitatea lichidului investigat este determinată de formula (9).
Comandă de lucru
Sarcina 1. Determinați vâscozitatea soluțiilor cu diferite concentrații.
-
Se toarnă apă în piciorul viscozimetrului care nu are capilar (Fig. 6) până la marcajul d.
-
Cu o para, aspirați lichidul prin capilar pentru a marca a. După îndepărtarea perei, închideți orificiul genunchiului stâng al viscozimetrului (cu o mână, un dop, un tampon etc.) (vezi Fig. 6). Pregătiți și porniți cronometrul, deschizând orificiul genunchiului stâng și opriți-l când curge marcajul b, determinând astfel t0 - timpul de curgere a apei între reperele a și b.
-
Repetați măsurătorile de 4-5 ori, găsiți timpul mediu.
-
Efectuați pașii 1-3 pentru toate lichidele de testare.
-
Calculați coeficienții de vâscozitate ai lichidelor studiate folosind formula (9).
-
Introduceți datele în tabelul 1.
tabelul 1
| № | Concentrație, % | t1 | t2 | t3 | t4 | t5 | | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 | ||||||||
| 5 | ||||||||
| 6 |
Sarcina 2. Determinați concentrația unei soluții necunoscute.
-
Graficul raportului de vâscozitate față de concentrația soluției
-
Cunoscând vâscozitatea soluției necunoscute, determinați concentrația acesteia din grafic.
masa 2
Densitatea apei la diferite temperaturi
| ρ, kg/m3 | t, 0C | ρ, kg/m3 | t, 0C |
| 999,13 | 15 | 998,02 | 21 |
| 998,97 | 16 | 997,80 | 22 |
| 998,80 | 17 | 997,57 | 23 |
| 998,43 | 19 | 997,32 | 24 |
| 998,23 | 20 | 997,07 | 25 |
Tabelul 3
Vâscozitatea apei la diferite temperaturi
| η, Pa.s | t, 0C | η, Pa.s | t, 0C |
| 0,00114 | 15 | 0,00098 | 21 |
| 0,00111 | 16 | 0,00096 | 22 |
| 0,00108 | 17 | 0,00093 | 23 |
| 0,00103 | 19 | 0,00091 | 24 |
| 0,00100 | 20 | 0,00089 | 25 |
Tabelul 4
Densitatea soluțiilor de glicerină de diferite concentrații
| CU, % | ρ, kg/m3 | CU, % | ρ, kg/m3 |
| 5 | 1012,5 | 45 | 1112,5 |
| 10 | 1025,0 | 50 | 1125,0 |
| 15 | 1037,5 | 55 | 1137,5 |
| 20 | 1042,5 | 60 | 1150,0 |
| 25 | 1052,5 | 65 | 1162,5 |
| 30 | 1075,0 | 70 | 1175,0 |
| 35 | 1087,5 | 75 | 1187,5 |
| 40 | 1100,0 | 80 | 1200,0 |
Lucru independent pe tema:
– rezolvarea problemelor situaționale;
- ascultarea rezumatelor
Controlul final al cunoștințelor:
– rezolvarea problemelor la bilete;
– răspunsuri la biletele de control final;
- rezumat.
Temă pentru a înțelege subiectul lecției
Întrebări de control pe tema lecției:
1. Cum se numește vâscozitatea unui lichid?
2. Ce fel de flux de fluid se numește laminar?Turbulent?
3. Ce caracterizează formula Reynolds?
4. Scrieți formula lui Newton și explicați semnificația fizică a cantităților incluse în ea?
5. Care este coeficientul de vâscozitate dinamică? In ce unitati se masoara?
6. Ce fluide se numesc newtoniene? Ce determină coeficientul lor de vâscozitate?
7. Ce lichide se numesc non-newtoniene?Ce determină coeficientul lor de vâscozitate?
8. Scrieți formula Poiseuille, explicați semnificația fizică a cantităților incluse în ea.
9. Ce metode se folosesc pentru a determina vâscozitatea unui lichid?
10. Povestește despre proprietățile reologice ale sângelui și ale altor fluide biologice, despre utilizarea analizelor reologice în medicină.
11. Ce arată gradientul de viteză? Afișați grafic.
12. Ce fenomen se numește frecare internă?
Sarcini de testare pe această temă:
ESTE JUSTIFICATĂ APLICAREA GLICERINEI LA ÎNCĂLZIRE?
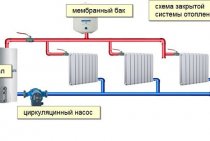
Lichidul de răcire pentru sistemele de încălzire se impun cerințe destul de mari. Trebuie să fie rezistent la foc și la explozie, să ofere performanțe termice bune și, de asemenea, să nu conțină aditivi interziși pentru utilizare. Etilenglicolul sau propilenglicolul este folosit ca bază pentru producția de fluid de transfer termic de înaltă calitate, care asigură, de asemenea, respectarea mediului.
Recent, pe piață au apărut lichidele de răcire antigel pe bază de glicerină. Acest produs este promovat în principal de firme mici, puțin cunoscute de pe piața antigel. Apare întrebarea: glicerina și lichidul de răcire - este adecvată unirea lor?
Și, într-adevăr, primele antigeluri care au apărut la noi în anii douăzeci ai secolului trecut au fost realizate pe bază de glicerină. Punctele slabe ale acestora erau fluiditatea insuficientă și vâscozitatea extrem de ridicată, pe care pompele nu le puteau face față. Au încercat să rezolve problema cu ajutorul alcoolului, inclusiv al alcoolului metilic. Cu toate acestea, odată cu îmbunătățirea fluidității, au apărut multe probleme. Cert este că metanolul este o otravă psihotropă puternică.Drept urmare, comportamentul șoferilor care adulmeca involuntar un astfel de antigel a sfidat uneori orice logică și a reprezentat un pericol pentru sănătatea și viața celorlalți. În plus, alcoolul metilic are un punct de fierbere scăzut și atunci când se evaporă, vâscozitatea produsului crește imediat. Problema a fost rezolvată numai când etilenglicolul a devenit baza lichidului de răcire. Și până la sfârșitul anilor treizeci, începutul anilor patruzeci, antigelurile cu etilenglicol i-au înlocuit aproape complet pe cei glicerin-metanol.
În plus, glicerina este instabilă termic, se descompune în timpul încălzirii prelungite, cu formarea unei substanțe volatile otrăvitoare - acroleina, care are un miros neplăcut ascuțit care provoacă ruperea. Produșii de descompunere sunt toxici, iar precipitarea mărește activitatea corozivă a lichidului de răcire. Ca urmare, cerințele pentru etanșări și piesele din cauciuc nepolar și materiale plastice sunt în creștere. Pe lângă vâscozitatea ridicată, glicerina face și spumă puternică, ceea ce duce la aerisirea sistemului și la o slabă disipare a căldurii.
Producătorii de lichide de răcire cu glicerină încearcă să compenseze toate dezavantajele de mai sus adăugând diverși aditivi, inclusiv alcooli alifatici - metanol, etanol, propanol. Acești alcooli pot reduce semnificativ vâscozitatea sau densitatea lichidului de răcire antigel. Dar fierb deja la temperaturi de peste 65 de grade, ceea ce duce la o deteriorare a performanței termice a lichidului de răcire. Acești alcooli sunt capabili să dizolve cauciucul și polimerii și sunt, de asemenea, predispuși la cavitație și evaporare puternică. În plus, metanolul este o otravă puternică și este interzisă utilizarea în producția de lichide antigel.
Asigurarea calității lichidelor de răcire cu glicerină, în special cu metanol, necesită adăugarea de pachete scumpe de aditivi la amestec. Și deși costul glicerinei este acum mai mic decât costul glicolilor, pachetul de aditivi pentru fabricarea fluidelor de transfer de căldură cu glicerină de calitate este mai scump decât pachetul de aditivi pentru antigel pe bază de etilenglicol și propilenglicol. Și dacă costul antigelului cu glicerină de pe piață este mai mic decât cel al glicolului, înseamnă că producătorul pur și simplu a economisit la calitate și nu a adăugat aditivii scumpi necesari produsului!
Deci alegerea este la latitudinea cumpărătorului: fie un lichid de răcire fiabil și dovedit pe bază de glicoli, fie un „porc în picătură” de glicerină.
Alegerea companiei noastre, la fel ca majoritatea producătorilor de top de antigel, este fundamental fără ambiguitate - glicerina nu poate fi folosită în forma sa pură, dar amestecată cu metanol este periculoasă și criminală!
Argumentul principal care confirmă poziția noastră cu privire la această problemă este că în orice instalație importantă și mare, utilizarea glicerinei în sistemele de încălzire și răcire NU este PERMISĂ de standardele existente!
MEG
Etilenglicolul este un produs al hidratării oxidului de etilenă în prezența acidului sulfuric sau fosforic. Se referă la alcooli polihidroxilici. Nu îngheață la temperaturi scăzute și scade punctul de îngheț al apei. Capabil să absoarbă apa din aer.
Se vinde in butoaie metalice si plastic, pana la 227 litri. La fel si cuburi de plastic 1000l.
Este necesar să depozitați substanța într-un recipient etanș din aluminiu sau oțel cu protecție anticorozivă într-un depozit închis fără încălzire. Perioada de valabilitate pentru clasa cea mai înaltă este de 12 luni, pentru clasa întâi - 3 ani de la data producției.
Denumirea indicatorului Norm
Aspect, miros Lichid limpede, incolor, cu textură uleioasă. Fara miros.
Solubil în apă, alcooli, toluen, benzen
Densitate 1,112 g/cm?.
Punct de topire 12,9 grade Celsius
Punct de fierbere 197,3 grade Celsius
Aplicație
Datorită capacității sale de a reduce punctul de îngheț, monoetilenglicolul este utilizat în producția de antigel și lichid de frână pentru mașini, precum și la fabricarea celofanului și poliuretanului. Într-o măsură mai mică, este utilizat în producția de cerneluri și cerneluri de imprimare.
Clasa de pericol
Se referă la substanțe combustibile. Autoaprinderea are loc la o temperatură de 380 de grade, un fulger de vapori când este încălzit la 120 de grade. Toxic. Ingestia nu este permisa. Vaporii sunt mai puțin nocivi.
Glicerol
Formula chimica: HOCH2CH(OH)CH2OH
Nume internațional: Glicerină
NR CAS: 56-81-5
Calificare: Imp. „h”, GOST 6259-75
Aspect: lichid limpede, inodor
Ambalare: Cutii de 25 kg, bidoane de 250 kg, 1500 cuburi
Conditii de depozitare: într-o încăpere uscată ventilată la o temperatură scăzută
Sinonime: 1,2,3-trioxipropan
Oferim Glicerina in cutii, butoaie, cuburi la preturi competitive.
| Specificație | |
| Greutate moleculară | 92.10 |
| Substanță de bază, nu mai puțin de | 99,5% (real 99,8%) |
| Conținut de cenușă, nu mai mult | 0,01% (de fapt, mai puțin de 0,1%) |
| Conținut de apă, nu mai mult | 0,5% (de fapt 0,1%) |
| Conținut de cloruri, nu mai mult | 0,001 % |
| Conținut de sulfat, nu mai mult | 0,002 % |
| Metale grele, nu mai mult | 0,0005% (de fapt, mai puțin de 0,00005%) |
| Compuși ai clorului (ca CL), nu mai mult | 0,003 % |
| Arsenic, nu mai mult | 0,00015% (real mai puțin de 0,00001%) |
| Culoare (APHA), nu mai mult | 20 (de fapt, mai puțin de 10) |
Glicerina este un lichid incolor, higroscopic, vâscos, inodor, cu gust dulce. Miscibil în orice raport cu apă, etanol, metanol, acetonă, insolubil în cloroform și eter. Când glicerolul este amestecat cu apă, căldura este eliberată și are loc contracția (reducerea volumului). Când glicerolul interacționează cu acizii hidrohalici sau halogenurile de fosfor, se formează mono- sau dihalohidrine; cu acizi anorganici si carboxilici - esteri completi si incompleti, cu deshidratare - acroleina. Glicerolul poate fi oxidat, iar în funcție de condițiile și natura agentului de oxidare se poate obține gliceraldehidă, acid gliceric, acid tartronic, dihidroxiacetonă, acid mezoxalic. Glicerina se găsește în grăsimi și uleiuri naturale sub formă de trigliceride amestecate de acizi carboxilici.
Aplicație Glicerina este utilizată pe scară largă • în industria farmaceutică, de exemplu pentru producerea de nitroglicerină, unguente medicinale; • în industria alimentară, de exemplu în producția de lichioruri, cofetărie; • în industria cosmetică, în fabricarea de parfumuri şi produse cosmetice • în producţia de răşini gliptale; • ca balsam pentru tesaturi, piele, hartie; • ca componentă a emulgatorilor, antigelului, lubrifianților, lustruirii pantofilor, săpunurilor și adezivilor, • ca materie primă în producția de polialcooli, care sunt utilizați în diferite spume. • ca plastifiant pentru celofan etc.
La ce temperatură îngheață apa în conductele de încălzire dintr-o clădire rezidențială
Dacă temperatura în casă rămâne -10 timp de câteva zile și există apă în țevi, atunci poate îngheța, ceea ce va duce la ruperea țevilor. Mulți au văzut probabil baterii moderne de încălzire cu funcție de evacuare a apei. Aproape toate bateriile moderne sunt echipate cu capacitatea de a scurge apa. Acest lucru se face astfel încât, în caz de urgență, când temperatura din casă este -10, apa să nu înghețe și să nu rupă țevile. Dacă situația a ajuns în acest sens, vă simpatizăm foarte mult, cel mai probabil va trebui să schimbați bateriile, deoarece în timpul înghețului apei, probabil au apărut microfisuri care fac periculoasă funcționarea în continuare a acestor baterii.
De ce apa poate îngheța în țevi. Dacă în timpul sezonului de încălzire, tocmai când bateriile se umplu cu apă, are loc o defecțiune și apa este răcită, iar temperatura scade rapid în exterior, acest lucru poate duce la înghețarea țevilor.
Am răspuns deja la întrebarea la ce temperatură îngheață apa, ca experiment, luați un pahar mic, umpleți-l pe jumătate cu apă și puneți-l la congelator timp de câteva ore, două ore sunt suficiente pentru ca apa să se transforme parțial în gheață.
Apa este una dintre cele mai esențiale substanțe de pe planeta noastră. Are o mulțime de proprietăți care îl fac, într-o oarecare măsură, unic. Una dintre cele mai faimoase proprietăți despre care știe chiar și un copil mic este înghețarea apei.Se știe că 0 grade Celsius este temperatura de cristalizare a apei. Dar nu totul este atât de simplu. Vom analiza în continuare câteva dintre subtilitățile acestui proces.

Densitatea soluției de glicerină la 25
Media aritmetică a densităților de alcool și glicerol.
209,4. 1.047. 25.265.0. 1.060. ... Vedeți care este Densitatea soluțiilor apoase de glicerină în alte dicționare E236 Fișier Formic acid.svg Formula structurală a acidului formic Acidul formic Acidul metanoic este primul ...
Care este densitatea glicerinei la 17 grade Celsius?
8
Densitatea la 25 C, g cm. ... O soluție de glicerină la o concentrație de 25% sau mai mult nu expune contaminarea microbiană; în soluții mai diluate, microorganismele se înmulțesc bine în ea.
3,14
Ce lichid are o densitate mai mare, glicerina sau alcoolul? explica
Ssss
TK-April pe site-ul în toată Rusia. Concentrația, densitatea și indicele de refracție al soluțiilor de glicerol 15 С. … 1,0594. 1,3633. 25.1.0620.
Calculați masa molară a ambelor substanțe. Pentru alcool, acesta este mai mic (92 g/mol față de 46 g/mol pentru alcool), iar densitatea este în mod corespunzător mai mică. Când vine vorba de alcool etilic.
Ce rost au astfel de întrebări? Informațiile se găsesc în motoarele de căutare
Media aritmetică a densităților componentelor amestecului.
Determinați ce masă de glicerol cu o densitate de 1,26 g ml trebuie luată pentru a prepara o soluție apoasă c.42. ... Într-un pahar de sticlă cu o capacitate de 0,25 l se pun 111 g de anhidridă ftalică și 46 g de glicerină cu o densitate de 28 V.
Cum se calculează densitatea și vâscozitatea unui lichid care conține apă, alcool și glicerină?
Pentru aceasta se vând reometre. nu trebuie sa numeri nimic. doar înghețați.
trietilen glicol. propilen glicol. Glicerol. … propilenglicol 40%. -25 C. ... Densitatea soluțiilor apoase de etilenglicol la diferite temperaturi.
Trebuie să știți procentul din toate componentele amestecului (cel puțin!)
În nici un caz. Este, căutați datele primite de cineva.
Vă rugăm să ajutați, va pluti o bucată de gheață în benzină, kerosen, glicerină? De ce?
Va fi în glicerină, nu plutește în whisky - densitatea este aproximativ aceeași cu cea a benzinei
De asemenea, crește densitatea soluției finite și îmbunătățește calitatea bulelor. ... Soluție de glicerină flacon 25gTula Pharmaceutical Factory LLC. … Soluție de tetraborat de sodiu în flacon de glicerină 20% 30g, Samara FF, Samara Rusia.
Gheața este mai puțin densă decât uleiul, așa că va fi.
Comparați densitatea gheții cu densitatea acestor lichide. dacă densitatea gheții este mai mică, atunci va pluti; dacă este mai mare, se va scufunda.
Nu stiu. depinde ce piesa. dacă există suficient aer în gheață pentru a o menține la suprafață, va pluti, iar dacă nu, atunci nu va pluti. incearca-l tu insuti. kerosenul este ieftin.
În funcție de temperatura la care se răcește această gheață
Punctul de fierbere al soluțiilor apoase de glicerină scade odată cu scăderea concentrației de glicerol cu un conținut de 5% apă, punctul de fierbere este de 160-161, densitatea sa este de 1,26362 g cm3. … 25 25 C . ZnCl2.
Nu am văzut niciodată gheață plutind în rezervorul de benzină și în recipient. Și cu siguranță este))). Deci, probabil, el este în partea de jos. Am văzut glicerina doar într-o fiolă și la căldură))).
Ooy!
X cantitate de glicerol diluat, g O densitate de glicerol distilat, g ml ... Soluțiile de glicerol la o concentrație de 25% și mai mult nu sunt supuse contaminării microbiene, mai multe soluții diluate sunt ...
Va pluti o bucată de gheață în benzină, kerosen, glicerină?
Află densitatea și gata!
Densitatea soluțiilor apoase de alcooli. Densitățile soluțiilor apoase g cm3 la 20 C sunt date pentru următoarele substanțe: etanol, 1-propanol, 2-propanol, etilenglicol, glicerol, D-manitol.
Da)))
Dacă densitatea gheții este mai mică decât densitatea lichidului, atunci gheața va pluti
Care este densitatea glicerinei la o temperatură de 24 gr. CU?
Glicerina Grade Celsius020406080100120140169180Densitate g/cm3126712591250123812241208118811631126
Pentru o temperatura de 24 de grade = se determina prin interpolare intre 20 si 40 de grade
Calculați punctul de fierbere al unei soluții 8% de glicerol C3H6O3 în acetonă. Răspunsul este 57,7oC. 4.O soluție, din care 100 ml conține 2,3 g... Se ia densitatea soluției egală cu unu. Raspuns 608 Pa. Tichetul 14 25 1. Câte grame de BaCl2 2H2O ...
Întrebări despre chimie))) și fizică. Care lichid este mai dens decât apa și, de asemenea, conduce electricitatea, dar nu metalul?
Glicerina, etilenglicoli, formamide, butirolactonă, aproape toți acizii, amine. și mult mai mult.
Concentrația acidului sulfuric, % în masă. Densitatea la 25 C, g cm... 25,60-0,1950 0,000 8 - umiditate relativă,% - indicele de refracție al unei soluții apoase de glicerol la 25 C pentru linia D sodiu - temperatura soluției, C...