Ceea ce determină salinitatea apei de mare
Văzând o cifră puțin mai mare 3,5 ppm
, ați putea crede că aceasta este o constantă pentru orice apă de mare de pe planeta noastră. Dar totul nu este atât de simplu, salinitatea depinde de regiune. S-a întâmplat că, cu cât regiunea este mai la nord, cu atât această valoare este mai mare.
Sudul, dimpotrivă, se laudă cu mări și oceane nu atât de sărate. Desigur, toate regulile au excepțiile lor. Nivelurile de sare din mări sunt de obicei puțin mai scăzute decât în oceane.
Care este împărțirea geografică în general? Nu se știe, cercetătorii o dau de la sine înțeles, există de toate. Poate că răspunsul ar trebui căutat în perioadele anterioare ale dezvoltării planetei noastre. Nu la momentul în care s-a născut viața - mult mai devreme.
Știm deja că salinitatea apei depinde de prezența:
- Clorura de magneziu.
- clorura de sodiu.
- alte săruri.
Poate că, în unele părți ale scoarței terestre, depozitele acestor substanțe au fost ceva mai mari decât în regiunile învecinate. Pe de altă parte, nimeni nu a anulat curenții marini, mai devreme sau mai târziu nivelul general a trebuit să se stabilească.
Deci, cel mai probabil, o mică diferență este asociată cu caracteristicile climatice ale planetei noastre. Nu este cea mai nefondată părere, dacă vă amintiți de înghețuri și vă gândiți la ce anume apa cu un conținut ridicat de sare îngheață mai lent.
Etape de congelare
Este foarte interesant de urmărit cum îngheață apa de mare. Nu este acoperit imediat cu o crustă uniformă de gheață, ca apa dulce. Când o parte din ea se transformă în gheață (și este proaspătă), restul volumului devine și mai sărat și este necesar un îngheț și mai puternic pentru a-l îngheța.
Tipuri de gheață
Pe măsură ce marea se răcește, se formează diferite tipuri de gheață:
- furtuna de zapada;
- nămol;
- ace;
- Salo;
- nilas.
Dacă marea nu a înghețat încă, dar este foarte aproape de ea și în acel moment cade zăpadă, ea nu se topește când vine în contact cu suprafața, ci este saturată cu apă și formează o masă vâscoasă mocioasă numită zăpadă. Înghețând, acest terci se transformă în nămol, care este foarte periculos pentru navele prinse de furtună. Din cauza asta, puntea este acoperită instantaneu cu o crustă de gheață.
Când termometrul atinge marcajul necesar pentru înghețare, în mare încep să se formeze ace de gheață - cristale sub formă de prisme hexagonale foarte subțiri. Adunându-le cu o plasă, spălând sarea și topindu-le, veți constata că sunt insipide.
Când devine și mai rece, grăsimea începe să înghețe și formează o crustă de gheață, transparentă și fragilă ca sticla. O astfel de gheață se numește nilas, sau sticlă. Este sărat, deși este format din ace nedospite. Faptul este că în timpul înghețului, acele captează cele mai mici picături din apa sărată din jur.
Numai în mări există un astfel de fenomen precum gheața plutitoare. Apare deoarece apa de aici se răcește mai repede în largul coastei. Gheața formată acolo îngheață până la marginea de coastă, motiv pentru care a fost numită gheață rapidă. Pe măsură ce gerul se intensifică pe vreme calmă, cucerește rapid noi teritorii, ajungând uneori la zeci de kilometri în lățime. Dar de îndată ce se ridică un vânt puternic, gheața rapidă începe să se spargă în bucăți de diferite dimensiuni. Aceste bancuri de gheață, adesea uriașe (câmpuri de gheață), sunt purtate de vânt și de curent în întreaga mare, cauzând probleme navelor.
Desalinizarea apei de mare.
Referitor la desalinizare, toată lumea a auzit măcar puțin, unii își amintesc acum chiar de filmul „Water World”. Cât de realist este să pui un astfel de distilator portabil în fiecare casă și să uiți pentru totdeauna de problema apei potabile pentru omenire? Tot ficțiune, nu realitate.
Totul ține de energia cheltuită, pentru că pentru o funcționare eficientă sunt necesare capacități uriașe, nu mai puțin decât un reactor nuclear. O uzină de desalinizare din Kazahstan funcționează pe acest principiu.Ideea a fost depusă și în Crimeea, dar puterea reactorului de la Sevastopol nu a fost suficientă pentru astfel de volume.
Cu o jumătate de secol în urmă, înaintea numeroaselor dezastre nucleare, încă se putea presupune că un atom pașnic va intra în fiecare casă. A existat chiar și un slogan. Dar este deja clar că nu se folosesc micro-reactoare nucleare:
- În aparatele de uz casnic.
- La întreprinderile industriale.
- În construcția de mașini și avioane.
- Și da, în limitele orașului.
Nu se așteaptă în secolul următor. Știința poate face un alt salt și ne surprinde, dar până acum acestea sunt doar fanteziile și speranțele romanticilor neglijenți.
Punctul de îngheț al apei distilate
Apa distilată îngheață? Reamintim că pentru ca apa să înghețe, este necesar să existe în ea niște centre de cristalizare, care pot fi bule de aer, particule în suspensie, precum și deteriorarea pereților recipientului în care se află.
Apa distilată, complet lipsită de orice impurități, nu are nuclee de cristalizare și, prin urmare, înghețarea ei începe la temperaturi foarte scăzute. Punctul inițial de îngheț al apei distilate este de -42 de grade. Oamenii de știință au reușit să obțină suprarăcirea apei distilate la -70 de grade.
Apa care a fost expusă la temperaturi foarte scăzute, dar nu a cristalizat se numește „suprarăcită”. Puteți pune o sticlă de apă distilată în congelator, puteți obține hipotermie și apoi demonstrați un truc foarte eficient - vedeți videoclipul:
Atingând ușor o sticlă luată din frigider sau aruncând o bucată mică de gheață în ea, poți arăta cum se transformă instantaneu în gheață, care arată ca niște cristale alungite.
Apă distilată: această substanță purificată îngheață sau nu sub presiune? Un astfel de proces este posibil numai în condiții de laborator special create.
ÑаÑÑолÑемпеÑаÑÑÑа
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðñ Ð Ð Ð Ðñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δ¶¶Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ²²¾¾ðð ððμ¾¾ðð ÑиÑÑÑ. Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñññ Ð ° Ð Ð Ð ° ñññ Ð ° Ð Ð Ð ° ° ñññ Ð ÐμÐ Dd Dd Ð Ðμ Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd dN »Ð ²Ðððð ооо²²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ²Ð Ð Ð ² DND »Ð ÑоÐ'ÐμÑжР° ниÐμ Ñол Рв Nd ° ÑÑоР»Ðμ мÐμнÑÑÐμ, ÑÐμм ÑÑÐμÐ ± ÑÐμмоÐμ Ð'л Ñ ÑвÑÐμкÑиÑÐμÑкого nD ° ÑÑвоÑÐ °, воÐ'Ð ° ÑÑкоÑÐ¸Ñ Ð¾Ð ±Ñазование кÑиÑÑаллов лÑда пÑи оÑл¾°Ð¸ÑажадÐÐдÐÐдÐÐдÐÐ ¸ оÑлажденÑÑаиоиии Rularea ñðμμðððμð½ððÐμÐμРРо Ð Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd ¸ÑивР° ÐµÑ ÐºÐ¾Ð½ÑенÑÑаÑÐ¸Ñ Ñоии оÑÑалÑном ÑаÑÑвое. Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ññ ñ ñ Ð ° Ð ° ñ °
Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñÐ ññ ñ ñ ñ ñ ñ ° ñ ° ñ ° ñ Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð μñ Dd ° мÐμÑÐ · Ð ° ниÐμ ÑвÑÐμкÑиÑÐμÑкого nD ° ÑÑвоÑÐ ° â ÑÑо пÑоÑÐμÑÑ Ñ nnd ° ÑÑиÐμм ÑкÑÑÑой ÑÐμпР»Ð¾ÑÑ, поÑÑÐ¾Ð¼Ñ ÑÐμмпÐμÑÐ ° ÑÑÑÐ ° оÑÑÐ ° ÐμÑÑÑ Ð½ÐμиР· менной. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ÐñÐ Ð Ð ÐñÐ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ¿Ñипонижении Ð Ð · ñ ñ ñ ñ ñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ññÐ Ð ° Ð ° Ð Ð Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ¸ поÑÑоÑннойÐð ° ð½ð½½¹ñ 𿸾¸¼ðμ½½ñð¸¼ðμ½ñðμ ñ ½¸½ ð ° ñ¸¸½½ð ° ½½½ð ° ½¿¿ð ° °½¿¸ ° ½¿¿¸ ° ° °¿¸¸¾¾¸ °¸ðð¾¾¾ñ¸¸¸¾¾¿¾¾¾ñ¸¸¾¾¾²¾¾μ¸¸¸¾¾²'ñμ ¾¾¾²² .
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð ° ° ° ° ° ¸Ñ и ÑлоÑида наÑÑиÑ. Dd ° ÑÑÐ²Ð¾Ñ Nd »Ð¾ÑиÐ'Ð ° кР° л ÑÑÐ¸Ñ Ð¿ÑÐμжÐ'Ðμ вÑÐμго иÑпоР»Nd · ÑÐμÑÑÑ Ð² пÑомÑÑл ÐμннÑÑ Ð¿ÑоÑÐμÑÑÐ ° Ñ Ð¿ÑÐ ¸ замоÑаживании пÑодÑкÑов, ÑÑанеиии. 17,8 °С. Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 °C Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð (μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñÐ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ¿Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ð Ð Ð ñ'Ðð Ð Ñ°ñ'Ðð Ð Ñ°ñ'ÐÐÐÐ Ð ° ñ'Ð Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd конÑÐ °ÐºÑ ÑаÑÑооа ÑоÑлаждаемÑм пÑодÑкÑом.
Ð ð ° ññð²¾¾¾ ðð ° ¾¸¸¸'ð °¸ ((¾¹¹ μ¾¸¸¸¾¹¹¹¾¾ »»¾¾¾¹ ñ¾¾¾ »¾ñ¸¸¸ ¾¾¾¾ñ¸¸¸ 𿸸ðμ¾¸¸¸ ¸¸ðμ'²ðμ ¾¾¾¾'ñðºññ. оñððð Ð ° Ð ° Nd Dd Ð ðñððÐ Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd РоÐμ Dd Dd Dd Dd Dd Ð ° Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ÐÐ Ð Ð ÐÐÐ Ð Ð Ð ÐÐ Ð Ð 1 °С. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ·
CICCULUL APEI ÎN OCEANUL MONDIAL
În regiunile polare, apa, răcindu-se, devine mai densă și se scufundă în fund. De acolo, alunecă încet spre ecuator. Prin urmare, la toate latitudinile, apele adânci sunt reci. Chiar și la ecuator, apele de fund au o temperatură de numai 1-2 ° peste zero.
Deoarece curenții transportă apă caldă de la ecuator la latitudinile temperate, apa rece se ridică foarte încet din adâncuri pentru a-i lua locul. La suprafață, se încălzește din nou, merge în zonele subpolare, unde se răcește, se scufundă în fund și se deplasează din nou de-a lungul fundului până la ecuator.
Astfel, în oceane există un fel de ciclu al apei: la suprafață, apa se deplasează de la ecuator în zonele subpolare și de-a lungul fundului oceanelor - din zonele subpolare către ecuator. Acest proces de amestecare a apei, împreună cu alte fenomene menționate mai sus, creează unitatea oceanelor.
Dacă găsiți o eroare, evidențiați o bucată de text și faceți clic Ctrl+Enter
.
În secțiunea privind întrebarea care este cea mai scăzută temperatură a unei soluții de apă-sare de sare obișnuită (de masă, NaCl), dată de autor european
cel mai bun răspuns este Prin adăugarea de sare în apă, rata de topire a gheții crește, iar temperatura de topire a gheții scade. Acest lucru se datorează faptului că adăugarea de sare determină o slăbire a coeziunii moleculare și distrugerea rețelelor cristaline de gheață. Topirea amestecului de gheață-sare are loc prin îndepărtarea căldurii din mediu, în urma căreia aerul din jur se răcește și temperatura acestuia scade. Odată cu creșterea conținutului de sare din amestecul de gheață-sare, punctul de topire al acestuia scade. Soluția de sare cu cel mai scăzut punct de topire se numește eutectic, iar temperatura ei de topire se numește punct criohidrat. Punctul de criohidrat pentru un amestec gheață-sare cu sare de masă este de -21,2°C, cu o concentrație de sare în soluție de 23,1% față de masa totală a amestecului, care este aproximativ egală cu 30 kg de sare la 100 kg de gheaţă.Cu o creștere suplimentară a concentrației de sare, nu este o scădere a temperaturii de topire a amestecului de gheață-sare, ci o creștere a temperaturii de topire (la o concentrație de sare de 25% în soluție față de masa totală, temperatura de topire crește până la -8 ° C). La congelarea unei soluții apoase de sare de masă într-o concentrație corespunzătoare punctului de criohidrat, se obține un amestec omogen de cristale de gheață și sare, care se numește soluție solidă eutectică. Punctul de topire al unei soluții solide eutectice de sare de masă este de -21,2 ° C, iar căldura de topire este de 236 kJ / kg. Soluția eutectică este utilizată pentru răcirea cu cuplu zero. Pentru a face acest lucru, o soluție eutectică de sare de masă este turnată în zerouri - forme bine sigilate - și acestea sunt înghețate. Zerourile congelate sunt folosite pentru a răci contoare, dulapuri, pungi frigorifice portabile frigorifice etc. (deschideți congelatorul unui frigider de uz casnic - veți găsi un astfel de recipient). În comerț, răcirea cu gheață-sare era utilizată pe scară largă înainte de producția în masă a echipamentelor cu răcirea mașinii.
Raspuns de la A usca
cea mai scăzută temperatură dintre orice temperatură este zero absolut, în jur de -273 de grade Celsius
Raspuns de la Olya
temperatura depinde de concentrația de sare din soluție, cu cât concentrația este mai mare, cu atât punctul de îngheț este mai mic. cartea de referință mi-a fost luată o vreme)) dar dacă pornim de la faptul că apa de mare este o soluție salină, atunci putem concluziona că temperatura de îngheț este mult mai mică decât zero.... grade -15-20
Raspuns de la capabil
Soluția apoasă de NaCl 22,4% îngheață la 21,2 °C
la întrebarea Soluție apoasă de NaCl „temperatura de cristalizare”
Raspuns de la Ierghey Neznamov
Tabelul 10.8. Punctul de îngheț al soluției de NaCl Conținut de NaCl, g în 100 g apă 5 - -4,4 9,0 - -5,4 10,6 - -6,4 12,3 - -7,5 14,0 - -8,6 15,7 - -9,8 17,5 - -11,0 19,2 -11,0 19,2 -1,2 -1,2 -1,2 -1,2 - - 15,1 25,0 - - 16,0 26,9 - -18,2 29,0 - -20,0 30,1 — -21,2
Punctul de îngheț al apei sărate
Experimentele cu gheață pentru copii sunt întotdeauna interesante. Făcând experimente cu Vlad, chiar am făcut câteva descoperiri pentru mine.
Astăzi vom găsi răspunsuri la următoarele întrebări:
- Cum se comportă apa când este înghețată?
- Ce se întâmplă dacă înghețați apa sărată?
- haina va încălzi gheața?
- si altele...
apă înghețată

Apa sărată îngheață?
Cu cât apa este mai sărată, cu atât punctul de îngheț este mai mic. Pentru experiment, am luat două pahare - într-unul apă dulce (marcat cu litera B), în celălalt apă foarte sărată (marcat cu literele B + C).
După ce a stat toată noaptea în congelator, apa sărată nu a înghețat, ci s-au format cristale de gheață în pahar. Apa proaspătă s-a transformat în gheață. În timp ce manipulam cești și soluții de sare, Vladik și-a creat propriul experiment neplanificat.
A turnat apa, ulei vegetal intr-o cana si a pus-o discret in congelator. 
Apa cu sare din congelator nu a înghețat, dar ce se întâmplă dacă presărați sare pe gheață? Sa verificam.
Experiență cu gheață și sare
Luați două cuburi de gheață. Stropiți unul dintre ele cu sare și lăsați-l pe al doilea pentru comparație. 
Am înghețat un țurț mare și l-am stropit cu sare, am luat perii și 
Creativitatea noastră cu experiență unește întreaga familie, așa că stiloul lui Makarushkin a intrat în obiectivul camerei!
Makar și Vlad sunt foarte tuturor adoră să înghețe
. Uneori există articole complet neașteptate în congelator.
Am visat să fac această experiență încă din copilărie, dar mama mea nu avea o haină de blană și multe

Ce grozav este să fii adult, să ai o haină de blană și să faci tot felul de experimente pentru copii!
Ta Galina Kuzmina
Tabelul prezintă proprietățile termofizice ale unei soluții de clorură de calciu CaCl 2 în funcție de temperatură și concentrația de sare: căldura specifică a soluției, conductivitatea termică, vâscozitatea soluțiilor apoase, difuzivitatea termică a acestora și numărul Prandtl. Concentrația de sare CaCl 2 în soluție este de la 9,4 la 29,9%. Temperatura la care sunt date proprietățile este determinată de conținutul de sare al soluției și variază de la -55 la 20°C.
clorura de calciu CaCl2 nu poate îngheța până la minus 55°С
. Pentru a obține acest efect, concentrația de sare din soluție ar trebui să fie de 29,9%, iar densitatea acesteia va fi de 1286 kg/m 3 .
Odată cu creșterea concentrației de sare într-o soluție, nu numai densitatea acesteia crește, ci și proprietăți termofizice precum vâscozitatea dinamică și cinematică a soluțiilor apoase, precum și numărul Prandtl. De exemplu, vâscozitatea dinamică a soluției de CaCl2
cu o concentrație de sare de 9,4% la o temperatură de 20°C este de 0,001236 Pa s, iar cu o creștere a concentrației de clorură de calciu în soluție la 30%, vâscozitatea sa dinamică crește până la o valoare de 0,003511 Pa s.
Trebuie remarcat faptul că temperatura are cea mai puternică influență asupra vâscozității soluțiilor apoase ale acestei săruri. Când o soluție de clorură de calciu este răcită de la 20 la -55°C, vâscozitatea sa dinamică poate crește de 18 ori și cinematica de 25 de ori.
Având în vedere următoarele proprietățile termofizice ale soluției de CaCl 2
:
- , kg / m 3;
- punctul de îngheț °С;
- vâscozitatea dinamică a soluțiilor apoase, Pa s;
- numărul Prandtl.
ÑаÑÑолÑемпеÑаÑÑÑа
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðñ Ð Ð Ð Ðñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð δ¶¶Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ²²¾¾ðð ððμ¾¾ðð ÑиÑÑÑ. Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñññ Ð ° Ð Ð Ð ° ñññ Ð ° Ð Ð Ð ° ° ñññ Ð ÐμÐ Dd Dd Ð Ðμ Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd dN »Ð ²Ðððð ооо²²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ²Ð Ð Ð ² DND »Ð ÑоÐ'ÐμÑжР° ниÐμ Ñол Рв Nd ° ÑÑоР»Ðμ мÐμнÑÑÐμ, ÑÐμм ÑÑÐμÐ ± ÑÐμмоÐμ Ð'л Ñ ÑвÑÐμкÑиÑÐμÑкого nD ° ÑÑвоÑÐ °, воÐ'Ð ° ÑÑкоÑÐ¸Ñ Ð¾Ð ±Ñазование кÑиÑÑаллов лÑда пÑи оÑл¾°Ð¸ÑÑажÐÑдÐÐажÐÑдÐÐ ¸ оÑлажденÑÑаиоиии Rularea ñðμμðððμð½ððÐμÐμРРо Ð Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd ¸ÑивР° Ðμñ 𺾾ð½ðμ ñ¾¾¾½¸¸¸ ¾ñ𾸸¸ ¾¾¾ñð¼ °¸¸ñð ° ¾¼¼ ñðð ¾¾¼¸ ñðð ¾¾ñ¸ ¾¾¸¸¸¾ñðð °¾¾¸¸¾¾ñðð °ññðð ¾¾¼¼ ññðð ¾¾¼¸ ñðð ¾¾¼¸ ñð ¾ñ¸ 𸠾ñð ° ¸ð¸¾ññð ° °¾¸¸¸ññð ° ° ° °ðð¾¾¼ð ° ñðð °¾¾¼¼¼¸¸¸Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñ ññ ñ ñ Ð ° Ð ° ñ °
Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ñÐ ññ ñ ñ ñ ñ ñ ° ñ ° ñ ° ñ Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð μñ Dd ° мÐμÑÐ · Ð ° ниÐμ ÑвÑÐμкÑиÑÐμÑкого nD ° ÑÑвоÑÐ ° â ÑÑо пÑоÑÐμÑÑ Ñ nnd ° ÑÑиÐμм ÑкÑÑÑой ÑÐμпР»Ð¾ÑÑ, поÑÑÐ¾Ð¼Ñ ÑÐμмпÐμÑÐ ° ÑÑÑÐ ° оÑÑÐ ° ÐμÑÑÑ Ð½ÐμиР· менной. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ . Ð Ð · ñ ñ ñ ñ ñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñ ññÐ Ð ° Ð ° Ð Ð Ð Ð'Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° ¸ поÑÑоÑнной Ðð ° ð½ð½½¹ñ 𿸾¸¼ðμ½½ñð¸¼ðμ½ñðμ ñ ½¸½ ð ° ñ¸¸½½ð ° ½½½ð ° ½¿¿ð ° °½¿¸ ° ½¿¿¸ ° ° °¿¸¸¾¾¸ °¸ðð¾¾¾ñ¸¸¸¾¾¿¾¾¾ñ¸¸¾¾¾²¾¾μ¸¸¸¾¾²'ñμ ¾¾¾²² .
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð ° ° ° ° ° ¸Ñ и ÑлоÑида наÑÑиÑ. Dd ° ÑÑÐ²Ð¾Ñ Nd »Ð¾ÑиÐ'Ð ° кР° л ÑÑÐ¸Ñ Ð¿ÑÐμжÐ'Ðμ вÑÐμго иÑпоР»Nd · ÑÐμÑÑÑ Ð² пÑомÑÑл ÐμннÑÑ Ð¿ÑоÑÐμÑÑÐ ° Ñ Ð¿ÑÐ ¸ замоÑаживании пÑодÑкÑов, ÑÑанеиии. 17,8 °С. Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 °C Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð (μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ñÐ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ñðððð¹¾¾ñ¾ºμ¸¸¹¾¾ñ¾º °¸¸¹¾ ° ¾ð'ñ¸¸¹¹ ° ¾¾'ñ¸¸¹ð ° ¾¾'ñ¸ººð ° ° ¾''ñ¸¹¹ð ° Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd ÑÑÑонÑÐ °ÐºÑ ÑаÑÑооа ÑоÑлаждаемÑм пÑодÑкÑом.
Ð ð ° ññð²¾¾¾ ðð ° ¾¸¸¸'ð °¸ ((¾¹¹ μ¾¸¸¸¾¹¹¹¾¾ »»¾¾¾¹ ñ¾¾¾ »¾ñ¸¸¸ ¾¾¾¾ñ¸¸¸ 𿸸ðμ¾¸¸¸ ¸¸ðμ'²ðμ ¾¾¾¾'ñðºññ. оñððð Ð ° Ð ° Nd Dd Ð ðñððÐ Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd Dd РоÐμ Dd Dd Dd Dd Dd Ð ° Ð Ð Ð Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð Ð Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ÐÐ Ð Ð ÐÐÐ Ð Ð Ð ÐÐ Ð Ð 1 °С. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ² Ð ² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ·
La ce temperatură poate îngheța apa de mare?
Dar întrebarea principală nu a primit încă răspuns. Am aflat deja că sarea încetinește înghețarea apei, marea va fi acoperită cu o crustă de gheață nu la zero, ci la temperaturi sub zero. Dar cât de departe ar trebui să ajungă la minus citirile termometrului, astfel încât locuitorii din regiunile de coastă să nu audă sunetul obișnuit al surfului atunci când își părăsesc casele?
Pentru a determina această valoare, există o formulă specială, complexă și de înțeles doar pentru specialiști. Depinde de indicatorul principal - nivelul de salinitate
. Dar din moment ce avem o valoare medie pentru acest indicator, putem găsi și punctul mediu de îngheț? Oh, sigur.
Dacă nu trebuie să calculați totul până la o sutime, pentru o anumită regiune, amintiți-vă temperatura de -1,91 grade
.
Poate părea că diferența nu este atât de mare, doar două grade. Dar în timpul fluctuațiilor sezoniere de temperatură, acest lucru poate juca un rol uriaș acolo unde termometrul scade cu cel puțin 0. Ar fi doar cu 2 grade mai rece, locuitorii aceleiași Africii sau Americii de Sud ar putea vedea gheața lângă coastă, dar vai. Cu toate acestea, nu credem că sunt foarte supărați de o astfel de pierdere.
Proprietățile termofizice ale soluției de NaCl
Tabelul prezintă proprietățile termofizice ale unei soluții de clorură de sodiu NaCl în funcție de temperatură și concentrația de sare. Concentrația de clorură de sodiu NaCl în soluție este de la 7 la 23,1%. Trebuie remarcat faptul că atunci când o soluție apoasă de clorură de sodiu este răcită, capacitatea sa de căldură specifică se modifică ușor, conductivitatea termică scade și vâscozitatea soluției crește.
Având în vedere următoarele proprietățile termofizice ale soluției de NaCl
:
- densitatea soluției, kg/m3;
- punctul de îngheț °С;
- capacitatea termică specifică (masă), kJ/(kg grade);
- coeficient de conductivitate termică, W/(m deg);
- vâscozitatea dinamică a soluției, Pa s;
- vâscozitatea cinematică a soluției, m2/s;
- difuzivitate termică, m2/s;
- numărul Prandtl.
Din ce este făcută apa de mare?
Prin ce este diferit conținutul mărilor de apa dulce? Diferența nu este atât de mare, dar totuși:
- Mult mai multa sare.
- Predomină sărurile de magneziu și sodiu.
- Densitatea diferă ușor, cu câteva procente.
- Hidrogenul sulfurat se poate forma la adâncime.
Componenta principală a apei de mare, oricât de previzibilă ar suna, este apa. Dar, spre deosebire de apa râurilor și lacurilor, aceasta contine cantitati mari de cloruri de sodiu si magneziu
.
Salinitatea este estimată la 3,5 ppm, dar pentru a fi mai clar - la 3,5 miimi dintr-un procent din compoziția totală.
Și chiar și aceasta, nu cea mai impresionantă cifră, oferă apei nu numai cu un gust specific, ci o face și de nebăut. Nu există contraindicații absolute, apa de mare nu este o otravă sau o substanță toxică și nu se va întâmpla nimic rău de la câteva înghițituri. Va fi posibil să vorbim despre consecințele dacă o persoană este cel puțin pe tot parcursul zilei.De asemenea, compoziția apei de mare include:
- Fluor.
- Brom.
- Calciu.
- Potasiu.
- Clor.
- sulfați.
- Aur.
Adevărat, în termeni procentuali, toate aceste elemente sunt mult mai puține decât sărurile.
State și tipuri de apă
Apa de pe planeta Pământ poate avea trei stări principale de agregare: lichidă, solidă și gazoasă, care se pot transforma în diferite forme care coexistă simultan între ele (aisberguri în apa de mare, vapori de apă și cristale de gheață în nori de pe cer, ghețari și libere). -râuri curgătoare).
În funcție de caracteristicile originii, scopului și compoziției, apa poate fi:
- proaspăt;
- mineral;
- nautic;
- băut (aici includem apa de la robinet);
- ploaie;
- dezghețat;
- salmastru;
- structurat;
- distilat;
- deionizat.
Prezența izotopilor de hidrogen face ca apa:
- ușoară;
- grele (deuteriu);
- supergrea (tritiu).
Știm cu toții că apa poate fi moale și dură: acest indicator este determinat de conținutul de cationi de magneziu și calciu.
Fiecare dintre tipurile și stările agregate de apă pe care le-am enumerat are propriul punct de îngheț și topire.
Video cu apă sărată înghețată

 Ce știi despre punctul de fierbere al apei?
Ce știi despre punctul de fierbere al apei?

Regimul de temperatură determină, în primul rând, viteza procesului de congelare.
Temperatura în intervalul de valori pozitive și negative afectează viteza reacțiilor, solubilitatea compușilor, viteza de dizolvare, coagularea, precum și concentrația perechilor de ioni nedisociați. Există mai multe tipuri de temperatură în soluții: structurală, punctul de îngheț. Temperatura de început a cristalizării (punctul de îngheț) - temperatura la care, ca urmare a răcirii soluției, începe formarea cristalelor. Depresiunea punctului de îngheț ΔTz este diferența dintre punctul de îngheț al unui solvent pur și al unei soluții. Punctul de îngheț al saramurii este întotdeauna sub punctul de îngheț al apei pure și depinde de concentrația de săruri dizolvate. Această dependență pentru saramură poate fi exprimată prin ecuația:
Unde LA
- coeficient de proporţionalitate; CU
este concentrația substanței dizolvate în soluție.
În soluții mai puțin diluate, temperatura de debut a cristalizării este determinată din diagrama de stare a sistemului corespunzător. Deoarece temperatura de îngheț a apelor de mare și a saramurilor naturale foarte mineralizate va fi diferită, presupunem că această temperatură ar trebui calculată folosind formule diferite.
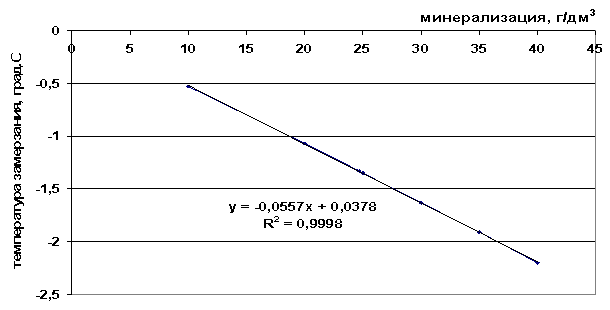
Am făcut o aproximare a datelor experimentale privind punctele de îngheț ale soluțiilor de sare de masă, apă de mare și saramură naturală utilizate în lucrare. Dependența modificărilor temperaturii de îngheț în forme grafice și analitice sunt prezentate în figurile 41-43.
Orez. 41. Dependența punctului de îngheț de salinitatea unei soluții de sare
Orez. 42. Dependența punctului de îngheț al apei de mare de salinitate
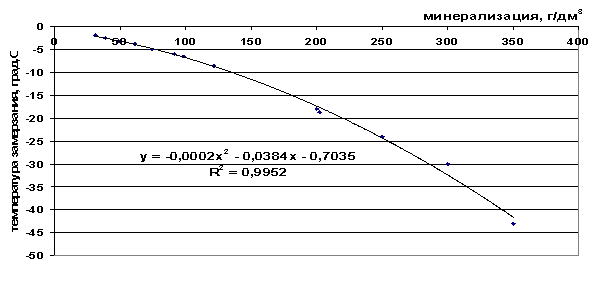
Orez. 43. Dependența punctului de îngheț al saramurii de salinitate
Din valorile punctului de îngheț prezentate (Tabelul 9), se poate observa că punctul de îngheț scade pe măsură ce salinitatea totală a soluției crește și pe măsură ce crește numărul de componente incluse în sistemul înghețat - ΔТз(NaCl)
Tabelul 9. Analiza dependențelor grafice construite
|
Ctot, g/dm 3 |
Punct de îngheț, °С |
||
|
soluție de NaCl |
apa de mare |
||
|
t=8∙10 -5 M2 -0,0945M+1,0595, |
0,0557 M+0,0378, |
t=-2∙10 -4 M2 -0,0384M-0,7035, |
|
*
R 2 - fiabilitatea aproximării
Se știe că înghețarea sărurilor individuale din apa desalinizată are loc la diferite temperaturi, de exemplu, la o temperatură de -2°C, precipită carbonat de calciu. La - 3,5 ° C sulfat de sodiu. Când temperatura scade la -20 ° C, sarea de masă precipită, la -25,5-26 ° C cloruri de magneziu, iar la temperaturi foarte scăzute - 40-55 ° C, clorurile de potasiu și calciu precipită. Pentru temperaturi negative este specific procesul de formare a hidraţilor cristalini, care sunt instabili la temperaturi sub 0°C. De exemplu, hidrohalit NaCl * 2H 2 O se formează la -0,15 ° C, MgCl 2 * 12H 2 O este stabil la -15 ° C și MgCl 2 * 8H 2 O este sub 0 ° C, Na 2 CO 3 * 7H 2 O se formează numai la -10°C. KCl cristalizează la 0°С sub formă de KCl, la -6,6°С deja coexistă două faze - KCl și KCl*H 2 O, la -10,6°С precipită doar KCl*H 2 O. La temperaturi negative, hidrații cristalini individuali cu numărul maxim posibil de molecule de apă de cristalizare, conform numerelor de coordonare la o valoare dată, și amestecurile acestora (dar nu cristale mixte). Trebuie remarcată o scădere anormală a punctului de îngheț al soluțiilor concentrate.
Vă aducem la cunoștință jurnale publicate de editura „Academia de Istorie Naturală”
La ce temperatură îngheață apa? S-ar părea - cea mai simplă întrebare la care poate răspunde chiar și un copil: punctul de îngheț al apei la presiunea atmosferică normală de 760 mmHg este zero grade Celsius.
Cu toate acestea, apa (în ciuda distribuției sale extrem de largă pe planeta noastră) este cea mai misterioasă și neînțeleasă substanță pe deplin, așa că răspunsul la această întrebare necesită o conversație detaliată și argumentată.
- În Rusia și Europa, temperatura este măsurată pe scara Celsius, cea mai mare valoare a cărei valoare este de 100 de grade.
- Omul de știință american Fahrenheit și-a dezvoltat propria scară cu 180 de divizii.
- Există o altă unitate de măsură a temperaturii - kelvin, numită după fizicianul englez Thomson, care a primit titlul de Lord Kelvin.
De ce nu ar trebui să bei apă de mare
Am atins deja pe scurt acest subiect, haideți să-l privim puțin mai detaliat. Împreună cu apa de mare, doi ioni intră în organism - magneziu și sodiu.
|
Sodiu |
Magneziu |
|
Participă la menținerea echilibrului apă-sare, unul dintre ionii principali alături de potasiu. |
Efectul principal este asupra sistemului nervos central. |
|
Cu o creștere a numărului N / A |
Excretat foarte lent din organism. |
|
Toate procesele biologice și biochimice sunt perturbate. |
Un exces în organism duce la diaree, care agravează deshidratarea. |
|
Rinichii umani nu sunt capabili să facă față atât de multă sare din organism. |
Poate dezvoltarea tulburărilor nervoase, stare inadecvată. |
Nu se poate spune că o persoană nu are nevoie de toate aceste substanțe, dar nevoile se încadrează întotdeauna în anumite limite. După ce bei câțiva litri de astfel de apă, vei depăși prea mult limitele lor.
Cu toate acestea, astăzi nevoia urgentă de utilizare a apei de mare poate apărea doar în rândul victimelor naufragiilor.