Vykorisťovanie

V vanádových prietokových batériách sú obidve referenčné elektródy dodatočne pripojené k zásobníkom a čerpadlám, takže cez článok môžu cirkulovať veľmi veľké objemy elektrolytu. Cirkulácia tekutého elektrolytu je trochu obtiažna a obmedzuje použitie vanádiových prietokových batérií v odvetviach vyžadujúcich mobilitu, vďaka čomu sú účinné vo veľkých stacionárnych budovách.
Keď sa vanádiová batéria nabíja, ióny VO2+ v kladne nabitej referenčnej elektróde sa zmenia na ióny VO2+, keď sa elektróny oddelia od kladnej svorky batérie. Podobne v zápornej referenčnej elektróde elektróny premieňajú ióny V3+ na V2+. Počas vybíjania je tento proces obrátený a poskytuje napätie naprázdno 1,41 V pri 25 °C.
Medzi ďalšie užitočné vlastnosti vanádiových prietokových batérií patrí veľmi rýchla odozva na zmeny zaťaženia a extrémne vysoká kapacita preťaženia. Výskum na Univerzite v Novom Južnom Walese ukázal, že dokážu dosiahnuť časy odozvy menej ako pol milisekúnd pri 100% zmenách zaťaženia a odolať 400% preťaženiu po dobu viac ako 10 sekúnd. Doba odozvy je vo väčšine prípadov obmedzená elektrickým zariadením. Vanádové batérie na báze kyseliny sírovej fungujú len pri teplotách 10-40C. Ak je teplota pod týmto rozsahom, ióny kyseliny sírovej kryštalizujú. Účinnosť pri vratnom pohybe pri každodennom používaní zostáva na úrovni 65-75%.
Vlastnosti nabíjania a vybíjania
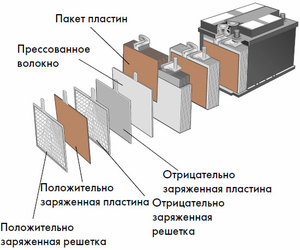
Algoritmy nabíjania priamo závisia od toho, ako je batéria usporiadaná a do akého typu patrí. Niektoré batérie dokážu napríklad bezpečne doplniť svoju kapacitu zo zdrojov konštantného napätia. Iné pracujú len s regulovaným zdrojom prúdu, ktorý môže meniť parametre v závislosti od úrovne nabitia.
Nesprávne organizovaný proces nabíjania môže poškodiť batériu. V extrémnych prípadoch sa môže batéria vznietiť alebo explodovať. Existujú inteligentné batérie vybavené zariadeniami na monitorovanie napätia. Hlavné parametre, ktoré by sa mali brať do úvahy pri prevádzke reverzibilných galvanických batérií, sú:
- Dĺžka života. Aj pri správnom zaobchádzaní je počet cyklov nabíjania batérie obmedzený. Rôzne systémy batérií sa nie vždy opotrebujú z rovnakých dôvodov. Vo všeobecnosti je však životnosť batérie limitovaná predovšetkým počtom cyklov úplného nabitia a vybitia a po druhé konštrukčnou životnosťou bez ohľadu na intenzitu používania.
- Doba nabíjania. Základná konštrukcia batérie neznamená nabíjanie ľubovoľne vysokou rýchlosťou: vnútorný odpor galvanického článku povedie k premene prebytočného nabíjacieho prúdu na teplo, ktoré môže nenávratne poškodiť zariadenie. Z fyzikálneho hľadiska je doba nabíjania obmedzená maximálnou rýchlosťou difúzie aktívneho materiálu cez elektrolyt.Zjednodušene môžeme predpokladať, že obnovenie plnej kapacity za jednu hodinu je dobrým ukazovateľom.
- Hĺbka výboja. Udáva sa ako percento menovitého výkonu. Popisuje využiteľnú kapacitu. Pre rôzne typy batérií sa môže odporúčaná prevádzková úroveň vybitia líšiť. V dôsledku zmien prevádzky alebo starnutia stráca indikátor maximálnej hĺbky svoju pôvodnú hodnotu.
difúzny proces.
Procesom difúzie, vyrovnaním hustoty elektrolytu v dutine puzdra batérie a v póroch aktívnej hmoty platní, môže byť polarizácia elektród v batérii zachovaná, keď je vonkajší obvod vypnutý.
Rýchlosť difúzie priamo závisí od teploty elektrolytu, čím vyššia je teplota, tým rýchlejšie proces prebieha a môže sa značne meniť v čase, od dvoch hodín až po deň. Prítomnosť dvoch zložiek elektródového potenciálu v prechodných podmienkach viedla k rozdeleniu na rovnovážne a nerovnovážne EMF batérie. Rovnovážnu EMP batérie ovplyvňuje obsah a koncentrácia iónov účinných látok v elektrolyte, ako aj chemické a fyzikálne vlastnosti účinných látok. Hlavnú úlohu vo veľkosti EMF hrá hustota elektrolytu a teplota ju prakticky neovplyvňuje. Závislosť EMF od hustoty možno vyjadriť vzorcom:
EMF batérie sa nerovná napätiu batérie, ktoré závisí od prítomnosti alebo neprítomnosti záťaže na jej svorkách.
admin25/07/2011
Komentár
Názov *
stránky
Táto stránka používa Akismet na boj proti spamu. Zistite, ako sa spracúvajú údaje o vašich komentároch.
« Mechanický tachometer
Napätie batérie »
Tagy
Poruchy VAZ, VAZ Senzory Zapaľovanie Vstrekovacie Zariadenia Štartovacie Schémy Elektrické autá Napájanie vaz 2110 gazela gazela obchodné registrátory autoopravovňa
Nedávne záznamy
- Senzory v aute: typy a účel
- Najväčší elektromobil na svete EDumper,
- Laserové svetlá.
- Výhody a nevýhody halogénových žiaroviek
- Zariadenie a princíp činnosti parkovacích senzorov
Archívy
Archívy Vybrať September 2019 August 2017 Júl 2017 Jún 2017 máj 2017 Apríl 2017 Marec 2017 12. 2016 2016 Október 2016 September 2016 August 2016 Júl 2016 Jún 2016 May 2016 Apríl 2016 Marec 2016 Február 2016 November 2015 Október 2015 August 2015 Júl 2015 Jún 2015 máj 2015 január 2015 december 2014 november 2014 október 2014 september 2014 august 2014 júl 2014 jún 2014 máj 2014 apríl 2014 február 2014 január 2014 december 2013 13. november 2013 október 2013 22. august 2013 13. máj 2013 , 2012, 2012, 2011, 2012, 2011, 2012, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, 2011, September 2012, 2011, 2011, 2011, 2011, 2011, 2011
Kategórie
- Akumulátorová batéria
- Video
- Generátor
- Senzory
- Diagnostika
- Zapaľovanie
- správy
- Vybavenie
- Zariadenia
- Oprava
- Zapaľovacia sviečka
- Štartér
- Schéma
- Zariadenia
- elektromobily
- Zdroj
Sme na sociálnych sieťach
Auto Electrician@ Všetky práva vyhradené. Pri kopírovaní materiálov lokality musíte uviesť odkaz na lokalitu.
Zariadenie a princíp činnosti
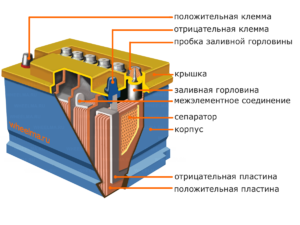
Každý takýto článok má katódu (kladnú elektródu) a anódu (negatívnu). Tieto elektródy sú oddelené elektrolytom, ktorý zabezpečuje výmenu iónov medzi nimi. Materiály elektród a zloženie elektrolytu sú zvolené tak, aby poskytovali dostatočnú elektromotorickú silu medzi svorkami batérie.
Keďže elektródy obsahujú obmedzený potenciál chemickej energie, batéria sa počas prevádzky vybije. Typ galvanických článkov, ktorý je prispôsobený na doplnenie po čiastočnom alebo úplnom vybití, sa nazýva batéria. Zostava takýchto vzájomne prepojených článkov je batéria.Prevádzka batérie zahŕňa cyklickú zmenu dvoch stavov:
- Nabíjanie - batéria funguje ako prijímač elektriny, vo vnútri článkov sa elektrická energia realizuje v chemických zmenách.
- Vybíjanie - zariadenie funguje ako zdroj elektrického prúdu premenou energie chemických reakcií na elektrickú energiu.
Oblasti použitia
Mimoriadne vysoká kapacita vanádiových redoxných batérií ich robí vhodnými na použitie v odvetviach vyžadujúcich veľké skladovanie energie. Napríklad pomoc pri vyrovnávaní objemu výroby takých zdrojov energie, ako je veterná alebo solárna energia, alebo pomoc generátorom absorbovať veľké prepätia v prípade potreby, alebo vyrovnávanie ponuky a dopytu po energii v odľahlých oblastiach.
Obmedzené vlastnosti samovybíjania vanádiových redoxných batérií ich robia užitočnými v odvetviach, kde sa batérie musia skladovať po dlhú dobu s minimálnou údržbou a pripravenosťou. To viedlo k ich použitiu v niektorých typoch vojenskej elektroniky, napríklad v senzoroch ťažobného systému GATOR. Ich schopnosť cyklovať a zostať na nule ich robí vhodnými pre solárne aplikácie a priemyselné odvetvia, kde batérie musia začať deň vybité a dobíjať sa v závislosti od zaťaženia a počasia. Napríklad lítium-iónové batérie sa často poškodia, keď sa nechajú vybiť pod 20 % svojho objemu, takže najčastejšie pracujú v rozsahu 20 až 100 %, čo znamená, že dokážu využiť len 20 % svojej menovitej kapacity.
Vďaka extrémne rýchlemu času odozvy sú prakticky nevyhnutné pre neprerušiteľné zdroje napájania, kde ich možno použiť namiesto olovených batérií a dokonca aj dieselových generátorov. Tiež rýchla doba odozvy ich robí vhodnými na riadenie frekvencie. V súčasnosti nie sú opatrenia UPS ani frekvenčného manažmentu samy osebe účinné, ale je pravdepodobné, že batéria bude môcť nájsť uplatnenie v týchto odvetviach, ak bude kapitalizovaná z rôznych zdrojov financovania. Navyše tieto schopnosti robia z vanádových redoxných batérií efektívne „jednodielne“ riešenie pre malé energetické siete, ktoré závisia od spoľahlivej prevádzky, frekvenčného riadenia a potrieb prepínania záťaže (ako je vysoká penetrácia obnoviteľných zdrojov, veľmi kolísavá záťaž alebo túžba po optimalizovať účinnosť generátora posunutím času odozvy).
Najväčšie pracovné vanádové redoxné batérie
Stanica "Minami Hyakita":
- Dátum spustenia: december 2015
- Energia: 60 MWh
- Výkon: 15 MW
- Pracovný čas: 4 hodiny
- Krajina: Japonsko
Smradľavý, provincia Liaoning
- Dátum spustenia: N/A
- Energia: 10 MWh
- Výkon: 5 MW
- Pracovný čas: 2 hodiny
- Krajina: Čína
Veterná farma Tomamae
- Dátum spustenia: 2005
- Energia: 6 MWh
- Výkon: 4 MW
- Pracovný čas: 1 hodina 30 minút
- Krajina: Japonsko
Projekt Zhangbei
- Dátum spustenia 2016
- Energia: 8 MWh
- Výkon: 2 MW
- Pracovný čas: 4 hodiny.
- Krajina: Čína
Projekt SnoPUD MESA 2
- Dátum spustenia: marec 2017
- Energia: 8 MWh
- Výkon: 2 MW
- Pracovný čas: 4 hodiny.
- Krajina: USA
Stanica v Escondido
- Dátum spustenia: 2017
- Energia: 8 MWh
- Výkon: 2 MW
- Pracovný čas: 4 hodiny.
- Krajina: USA
Rozvodňa v Pullman, Washington
- Dátum spustenia: apríl 2015
- Energia: 4 MWh
- Výkon: 1 MW
- Pracovný čas: 4 hodiny
- Krajina: USA
Do roku 2018 sa očakáva ukončenie vývoja vanádovej redoxnej batérie v Číne. Jeho energia bude 800 MWh, výkon - 200 MW a doba prevádzky - 4 hodiny.
Podmienky
- Sekvenčné – prvky nasledujú jeden po druhom.
- Elektromotorická sila (EMF) je napätie generované batériou alebo magnetickou silou v súlade s Faradayovým zákonom.
- Paralelné - Elektrické komponenty sú usporiadané tak, že prúd prúdi pozdĺž dvoch alebo viacerých ciest.
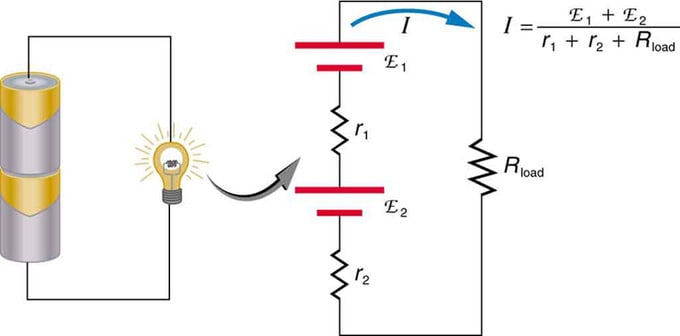
Ak používate viacero zdrojov napätia, môžu byť zapojené do série alebo paralelne. Pri sériovej verzii sú ladené rovnakým smerom, vnútorný odpor je plusový a elektromotorická sila sa pridáva algebraicky. Podobné typy sú bežné v baterkách, hračkách a rôznych iných zariadeniach. Bunky sú umiestnené v sérii, aby sa zvýšilo celkové emf.
Sériové pripojenie dvoch zdrojov napätia v rovnakom smere. Diagram zobrazuje svietidlo s dvoma bunkami a jednou lampou
Batéria - viacnásobné pripojenie voltových prvkov. Pri sériovom zapojení je ale jedna nevýhoda, keďže sa pridávajú vnútorné odpory. Niekedy to spôsobuje problémy. Povedzme, že máte dve 6V batérie, ktoré vložíte namiesto bežných 12V. V dôsledku toho ste pridali nielen EMF, ale aj vnútorný odpor z každej batérie.
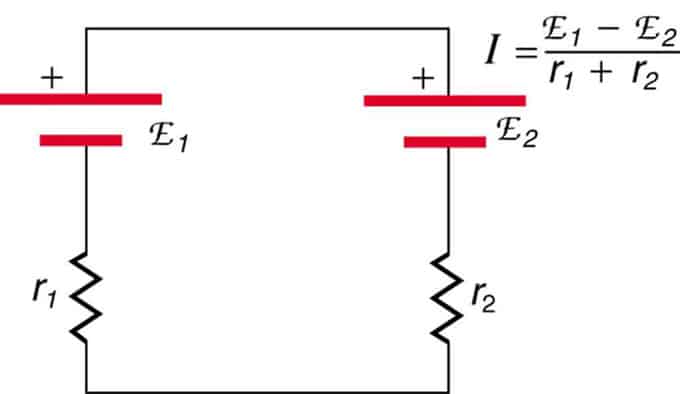
Ak sú bunky umiestnené v opozícii (jedna je umiestnená za druhou), potom sa celkové emf zníži.
Ide o dva zdroje napätia zapojené do série s opačnými emisiami. Prúd tečie v smere väčšieho EMF a je obmedzený súčtom vnútorných odporov. Príkladom je nabíjačka. Musí mať viac EMF ako batéria
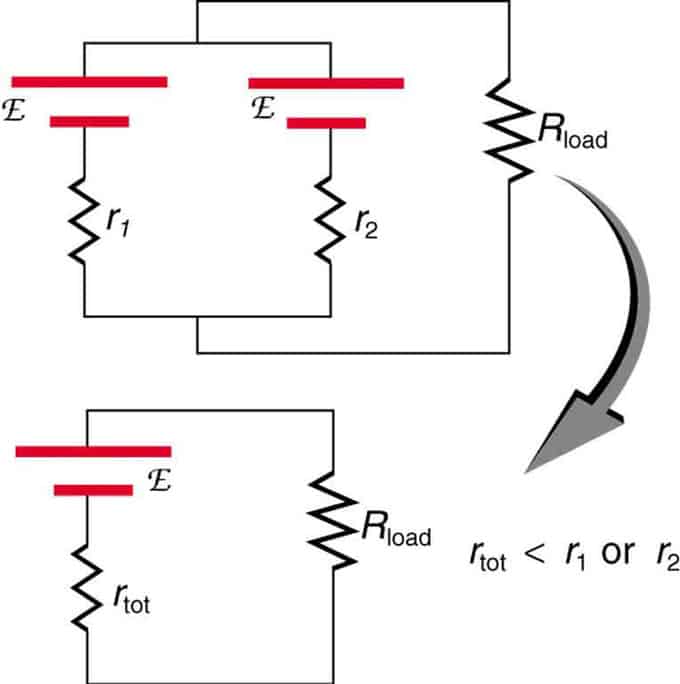
Ak sú dva zdroje s rovnakou elektromotorickou silou umiestnené paralelne a pripojené k zaťažovaciemu odporu, potom celkový EMF zostáva rovnaký ako jednotlivé. Celkový vnútorný odpor sa však zníži. Ukazuje sa, že paralelná verzia môže generovať väčší prúd.
Dva zdroje napätia s jedným EMF sú kombinované v paralelnom zapojení. Tvoria jeden EMF, ale majú menší celkový odpor ako jednotlivo. Podobné kombinácie sa používajú, ak potrebujete dosiahnuť väčší prúd.
| Prehľad |
|
| Paralelné a sériové zapojenie rezistorov |
|
| Kirchhoff pravidlá |
|
| Voltmetre a ampérmetre |
|
| RC obvody |
|
Historický prehľad
O vývoj prvého galvanického článku sa zaslúžil taliansky fyzik Alessandro Volta. V 90. rokoch 18. storočia uskutočnil sériu experimentov s elektrochemickými javmi a okolo roku 1800 vytvoril prvú batériu, ktorú jeho súčasníci nazývali „voltaický stĺp“. Zariadenie pozostávalo zo striedajúcich sa zinkových a strieborných kotúčov oddelených vrstvami papiera alebo látky, ktoré boli namočené v roztoku hydroxidu sodného.
Tieto experimenty sa stali základom pre prácu Michaela Faradaya o kvantitatívnych zákonoch elektrochémie. Opísal princíp fungovania batérie a na základe práce vedca vznikli prvé komerčné elektrické články. Ďalší vývoj vyzeral takto:
- V roku 1836 predstavil britský chemik John Daniel vylepšený model článku pozostávajúci z medených a zinkových elektród ponorených do kyseliny chlorovodíkovej. Danielov prvok dokázal zabezpečiť konštantné napätie neporovnateľne efektívnejšie ako Voltove prístroje.
- 1839 Ďalší pokrok dosiahol fyzik Grove so svojou dvojtekutinovou bunkou, pozostávajúcou zo zinku ponoreného v zriedenej kyseline sírovej v poréznej nádobe. Ten oddelil kyselinu sírovú z nádoby obsahujúcej kyselinu dusičnú, v ktorej bola umiestnená platinová katóda. Kyselina dusičná slúžila ako oxidačné činidlo, aby sa zabránilo strate napätia v dôsledku akumulácie vodíka na katóde.Nemecký chemik Robert Bunsen nahradil platinu lacným uhlíkom v článku Grove a tým podporil široké prijatie tohto typu batérie.
- V roku 1859 Gaston Plante vynašiel olovený článok, predchodcu modernej autobatérie. Planteho prístroj dokázal vyprodukovať nezvyčajne veľký prúd, no takmer dve desaťročia sa používal len na experimenty v laboratóriách.
- 1895-1905 rokov. Vynález nikel-kadmiových a nikel-železných alkalických prvkov. To umožnilo vytvárať systémy so značným počtom cyklov nabíjania a vybíjania.
- Od 30. rokov 20. storočia sa začal vývoj strieborno-zinkových a ortuťovo-zinkových alkalických batérií, ktoré poskytovali vysokú hustotu energie na jednotku hmotnosti a objemu.
- Od polovice 20. storočia pokroky vo výrobnej technológii a nástup nových materiálov viedli k ešte výkonnejším a kompaktnejším batériám. Najpozoruhodnejšie bolo uvedenie nikel-metal hydridových a lítiových batérií na trh.
Nabíjanie batérií
Hlavný článok: Nabíjačka
Keď sa chemická energia vyčerpá, napätie a prúd klesne a batéria prestane fungovať. Batériu (batériu batérií) môžete nabíjať z akéhokoľvek jednosmerného zdroja s vyšším napätím pri obmedzení prúdu. Najbežnejší je nabíjací prúd (v ampéroch), úmerný 1/10 podmienenej menovitej kapacity batérie (v ampérhodinách).
Na základe technického popisu distribuovaného výrobcami široko používaných elektrických batérií (NiMH, NiCd) však možno predpokladať, že tento režim nabíjania, bežne označovaný ako štandardná, sa vypočítava na základe trvania osemhodinového pracovného dňa, kedy sa batéria vybitá na konci pracovného dňa pripojí k sieťovej nabíjačke pred začiatkom nového pracovného dňa. Použitie takéhoto režimu nabíjania pre tieto typy batérií so systematickým používaním vám umožňuje udržiavať rovnováhu medzi kvalitou a nákladmi pri prevádzke produktu. Na návrh výrobcu je teda tento režim použiteľný len pre nikel-kadmiové a nikel-metal hydridové batérie.
Mnoho typov batérií má rôzne obmedzenia, ktoré je potrebné brať do úvahy pri nabíjaní a následnom používaní, napríklad NiMH batérie sú citlivé na prebitie, lítiové batérie sú citlivé na nadmerné vybitie, napätie a teplotu. Batérie NiCd a NiMH majú takzvaný pamäťový efekt, ktorý spočíva v znížení kapacity pri nabíjaní, keď batéria nie je úplne vybitá. Tieto typy batérií majú tiež znateľné samovybíjanie, to znamená, že postupne strácajú náboj bez toho, aby boli pripojené k záťaži. Na boj proti tomuto efektu je možné použiť kvapkacie dobíjanie.
Spôsoby nabíjania batérie
Na nabíjanie batérií sa používa niekoľko metód; Vo všeobecnosti spôsob nabíjania závisí od typu batérie.
- Pomalé jednosmerné nabíjanie
Nabíjajte jednosmerným prúdom úmerným 0,1-0,2 podmienenej menovitej kapacity Q po dobu asi 15-7 hodín, resp.
Najdlhší a najbezpečnejší spôsob nabíjania. Vhodné pre väčšinu typov batérií.
- rýchle nabíjanie
Nabíjajte jednosmerným prúdom úmerným 1/3 Q po dobu asi 3-5 hodín.
- Zrýchlené alebo "delta-V" nabíjanie
Nabíjanie s počiatočným nabíjacím prúdom úmerným nominálnej kapacite batérie, pri ktorom sa neustále meria napätie batérie a nabíjanie končí po úplnom nabití batérie. Doba nabíjania je približne hodinu a pol. Batéria sa môže prehriať a dokonca ju zničiť.
- prenesenie daňovej povinnosti
Vykonáva sa striedaním dlhých nabíjacích impulzov s krátkymi vybíjacími impulzmi. Reverzný spôsob je najužitočnejší pre nabíjanie NiCd a NiMH akumulátorov, ktoré sa vyznačujú tzv.n. „pamäťový efekt“.