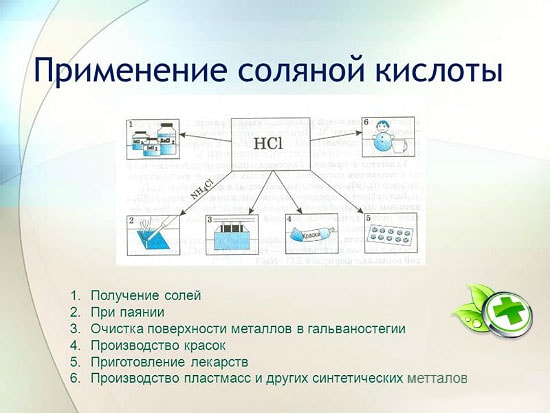
Употреба хлороводоничне киселине
Хлороводонична киселина има широку примену у индустрији за вађење метала из руда, кисељење метала итд. Такође се користи у производњи течности за лемљење, у таложењу сребра и као саставни део царске воде.
Обим употребе хлороводоничне киселине у индустрији је мањи него код азотне киселине. Ово је због чињенице да хлороводонична киселина изазива корозију челичне опреме. Поред тога, његове испарљиве паре су прилично штетне и такође изазивају корозију металних производа. Ово се мора узети у обзир приликом складиштења хлороводоничне киселине. Хлороводонична киселина се складишти и транспортује у резервоарима и бурадима обложеним гумом, тј. у посудама чија је унутрашња површина прекривена гумом отпорном на киселину, као иу стакленим боцама и посуђем од полиетилена.
Хлороводонична киселина се користи за производњу хлорида цинка, мангана, гвожђа и других метала, као и амонијум хлорида. Хлороводонична киселина се користи за чишћење површина метала, судова, бунара од карбоната, оксида и других седимената и загађивача. У овом случају се користе посебни адитиви - инхибитори који штите метал од растварања и корозије, али не одлажу растварање оксида, карбоната и других сличних једињења.
ХЦл се користи у индустријској производњи синтетичких смола, гуме. Користи се као сировина у производњи метил хлорида из метил алкохола, етил хлорида из етилена и винил хлорида из ацетилена.
Прва помоћ и методе лечења
Ако се пронађу знаци тровања, потребно је позвати хитну помоћ. Код куће је дозвољено обављање активности које имају за циљ побољшање стања жртве. Прва помоћ код тровања хлороводоничном киселином треба да се спроведе брзо како би се смањио ризик од негативних последица.
Догађаји:
- Ако једињење соли доспе на кожу, оштећена места се исперу са пуно хладне воде. Време обраде је најмање пола сата.
- У случају тровања парама, жртви се обезбеђује приступ свежем ваздуху, отварају се прозори, откопчава се уска одећа.
- Препоручује се праћење стања пацијента, у одсуству знакова живота, спроводи се реанимација.
- Жртва од испарења сме да пије топли чај, воду. Препоручује се испирање носа и уста хладном водом.
- У случају предозирања услед гутања киселине, на стомак се ставља пакет леда да би се спречило или смањило могуће крварење.
- Нису дозвољени лекови. Дозвољено је дати пацијенту чашу воде (можете минерално алкалну). Течност за пиће је потребна у малим гутљајима.
- Није дозвољено прање стомака, покушајте да изазовете повраћање код куће. Таква прва помоћ може довести до развоја опекотина грла, крварења.
Лечење се спроводи у медицинској установи под надзором специјалиста.
терапија:
- Чишћење стомака сондом,
- Употреба капаљки са лековитим растворима,
- Преписивање лекова за ублажавање болова
- Употреба лекова који имају за циљ обнављање функционисања органа и система,
- Ако је потребно, инхалација кисеоника и вештачка вентилација плућа,
- Спровођење терапије реанимације у одсуству знакова живота,
- Избор витамина и посебне исхране.
Лечење се спроводи на интензивној нези, а затим у болници. Трајање зависи од стања пацијента и степена тровања.
Опекотине и тровања
Колико год да је овај лек ефикасан, опасан је. Хлороводонична киселина, у зависности од концентрације, може изазвати хемијске опекотине од четири степена:
- Постоји само црвенило и бол.
- Постоје пликови са бистром течношћу и отоком.
- Формирана некроза горњих слојева коже.Пликови се пуне крвљу или замућеним садржајем.
- Лезија достиже тетиве и мишиће.
Ако је супстанца некако ушла у очи, потребно их је испрати водом, а затим раствором соде. Али у сваком случају, прва ствар коју треба учинити је позвати хитну помоћ.
Гутање киселине изнутра је испуњено акутним боловима у грудима и стомаку, отицањем ларинкса, повраћањем крвавих маса. Као резултат, тешке патологије јетре и бубрега.
А први знаци тровања у пару су сув чест кашаљ, гушење, оштећење зуба, пецкање у слузокожи и бол у стомаку. Прва хитна помоћ је прање и испирање уста водом, као и приступ свежем ваздуху. Праву помоћ може пружити само токсиколог.
Особине хемијског спектра
Киселина ступа у интеракцију са многим металима, солима. Сматра се прилично јаким и у рангу је са дивокозом. Главна реакција се манифестује у свим групама метала који се налазе лево од водоника (магнезијум, гвожђе, цинк - електрични потенцијали).
Раствор хлороводоника у разблаженом облику реагује са солима, али само са онима које формирају мање јаке киселине. Свима познати натријум и калцијум карбонат, након интеракције са њим, разлажу се на воду и угљен-моноксид.
Азотна киселина
- квалитативна реакција на физиолошки раствор. Да бисте га добили, потребно је додати сребрни нитрат у овај реагенс, као резултат тога ће се формирати бели талог, из којег се добија азотна супстанца.
Уз помоћ ове мешавине воде и водоника изводе се многи занимљиви експерименти. На пример, разблажите га амонијаком. Као резултат, добићете бели дим, густ, који има конзистенцију малих кристала. Метиламин, анилин, манган диоксид, калијум карбонат су реагенси на које утиче и киселина.
Како и зашто се користи
Можда је ово с правом једна од важних супстанци које се налазе и неопходне у скоро свим гранама људског живота.
Локализација области апликације:
- металургија. Површинско чишћење од оксидираних подручја, растварање рђе, третман пред лемљењем, калајисање. Хлороводонична киселина помаже у издвајању малих инклузија метала из руда. Цирконијум и титан се добијају методом претварања оксида у хлориде.
- Индустрија прехрамбене технологије. Раствор ниске концентрације се користи као адитив за храну. Желатин, фруктоза за дијабетичаре садржи чист емулгатор. Обична сода такође има висок садржај ове супстанце. На паковању робе видећете га под именом Е507.
- Област медицине. Са недовољним индикатором киселог окружења у стомаку и проблемима са цревима. Низак Пх доводи до рака. Чак и уз правилну исхрану, витамине у изобиљу, опасност не нестаје, потребно је извршити тестове за добијање сока из желудачног тракта, јер се у недовољно киселој средини корисне супстанце практично не апсорбују, варење је поремећено.
- Раствор соли се користи као инхибитор - заштита од прљавштине и инфекција, антисептичко дејство. За производњу лепљивих смеша, керамичких производа. Испира измењиваче топлоте.
- Процедура за пречишћавање воде за пиће такође није потпуна без учешћа хлора.
- Производња гуме, бељење платнених подлога.
- Са овим раствором можете да бринете о својим сочивима.
- Вода за испирање уста код куће
- Супстанца је одличан проводник струје.
Како долази до тровања
Хлороводонична киселина је безбојна течност са карактеристичним оштрим мирисом. Једна од најјачих киселина, способна да раствори неке метале. Лако се претвара у гас.
Хлороводоник се користи у текстилној индустрији, кожарству, металургији племенитих метала, у производњи лепка, киселина.
Супстанца је присутна у стомаку у минималној концентрацији. Киселина доприноси нормализацији процеса варења, штити тело од штетних бактерија и микроорганизама.
У концентрацији већој од 24%, хлороводонична киселина може нанети неповратну штету људском телу. Паре настале при контакту са ваздухом изазивају иритацију органа визуелног и респираторног система.
Постоји неколико фактора који могу изазвати развој тровања.
Фактори:
Тровање паром је могуће када радите у просторијама са слабом вентилацијом,
Гутање из немара, чешће код деце,
Улазак хлороводоничне киселине на епидермис, слузокоже у случају непоштовања правила за употребу реагенса.
Тровање супстанцом код куће код одраслих настаје као резултат употребе без заштитне опреме коже, очију и органа респираторног система. До интоксикације може доћи када се киселина нетачно преноси из једног контејнера у други.
Фармакодинамика и фармакокинетика
Шта је киселост желуца? Ово је карактеристика концентрације хлороводоничне киселине у желуцу. Киселост се изражава у пХ
. Нормално, киселина треба да се производи у саставу желудачног сока и да активно учествује у процесима варења. Формула хлороводоничне киселине: ХЦл
. Произведен је од париеталних ћелија које се налазе у фундицним жлездама, уз учешће Х+/К+-АТПаза
. Ове ћелије облажу фундус и тело желуца. Сама киселост желудачног сока је променљива и зависи од броја паријеталних ћелија и интензитета процеса неутрализације супстанце алкалним компонентама желудачног сока. Концентрација произведена до - ви сте стабилни и једнаки су 160 ммол/л. Здрава особа треба нормално да производи не више од 7 и најмање 5 ммол супстанце на сат.
Са недовољном или прекомерном производњом хлороводоничне киселине настају болести дигестивног тракта, погоршава се способност апсорпције одређених микроелемената, као што је гвожђе. Лек стимулише лучење желудачног сока, смањује пХ
. Активира пепсиноген
, претвара га у активни ензим пепсин
. Супстанца има благотворно дејство на кисели рефлекс желуца, успорава прелазак непотпуно сварене хране у црева. Процеси ферментације садржаја дигестивног тракта се успоравају, бол и подригивање нестају, гвожђе се боље апсорбује.
Након оралне примене, лек се делимично метаболише пљувачком и желудачном слузи, садржајем дуоденума 12. Невезана супстанца продире у дуоденум, где је потпуно неутралисана својим алкалним садржајем.
Још једна употреба киселине у свакодневном животу
Са киселим саставом, лако можете очистити каменац и рђу са фајансе водовода, уклонити уринарни камен и друге загађиваче. За већи ефекат, у агенс се додаје инхибитор (на пример, уротропин), који успорава хемијску реакцију.
Поступак се спроводи на следећи начин: киселина се разблажи водом док се не постигне концентрација од 5% и додаје се инхибитор брзином од 0,5 г на 1 литар течности. Површина се третира добијеном композицијом и остави 30-40 минута (у зависности од степена контаминације), након чега се испере водом.
Благи раствор киселине се такође користи за уклањање мрља од бобица, мрља од мастила или рђе са тканина. Да би се то урадило, материјал се неко време натопи у композицију, након чега се темељно испере и опере на уобичајен начин.
Уклањање каменца у чајнику
У ту сврху се користи 3-5% раствор хлороводоничне киселине, који се сипа у котлић и загрева на 60-80°Ц.°
Ц током 1-2 сата или док се наслаге каменца не распадну. Након тога, вага постаје лабава и лако се уклања дрвеном лопатицом.
Ефикасност методе је због чињенице да реагенс реагује са магнезијум и калцијум карбонатима и претвара их у растворљиве соли. Угљен-диоксид који се ослобађа истовремено уништава слој каменца и чини га лабавим. Након уклањања наслага соли, посуђе се темељно опере чистом водом.
Важна тачка!
Ова метода није прикладна за уклањање каменца са емајлираних или алуминијумских котлића од напуклих и напуклих: то ће кородирати метал и озбиљно га оштетити.
Добијање супстанце
Сада можемо разговарати о томе шта они раде да формирају хлороводоничну киселину.
Прво, сагоревањем водоника у хлору, добија се главна компонента, гасовити хлороводоник. који се затим раствара у води. Резултат ове једноставне реакције је формирање синтетичке киселине.
Ова супстанца се такође може добити из отпадних гасова. То су хемијски отпадни (бочни) гасови. Настају различитим процесима. На пример, приликом хлорисања угљоводоника. Хлороводоник у њиховом саставу се назива отпадним гасом. И тако добијена киселина, респективно.
Треба напоменути да се последњих година повећава удео отпадних гасова у укупном обиму његове производње. А киселина настала као резултат сагоревања водоника у хлору се истискује. Међутим, поштено, треба напоменути да садржи мање нечистоћа.
Употреба у производњи
Има широку примену у металуршкој, прехрамбеној и медицинској индустрији.
- металургија. Користи се за лемљење, калајисање и чишћење метала.
- Прехрамбена индустрија. Примена у производњи регулатора киселости хране, на пример, Е507.
- Елецтротипе. Користи се за кисељење.
- Лек. Своју примену налази у производњи вештачког желудачног сока.
Укључено у синтетичке боје. Користи се у производњи средстава за чишћење и детерџента. Али у течностима намењеним за домаћу употребу, концентрација сумпорне киселине је занемарљива.
Како се хлороводонична киселина производи у лабораторији
Производња супстанце је велика, продаја је бесплатна. У условима лабораторијских експеримената, раствор се производи дејством високе концентрације сумпорне киселине на обичну кухињску со (натријум хлорид).
Постоје 2 методе за растварање хлороводоника у води:
- Водоник се сагорева у хлору (синтетички).
- Повезани (отпусни гас). Његова суштина је у спровођењу органског хлорисања, дехидрохлорисања.
Супстанца је погодна за синтезу током пиролизе отпада из органохлор. Ово се дешава као резултат распада угљоводоника са потпуним недостатком кисеоника. Такође можете користити хлориде метала, који су сировине неорганских супстанци. Ако нема концентроване сумпорне киселине (електролита), узимајте разблажену.
Што се тиче екстракције реагенса у природним условима, најчешће се ова хемијска смеша може наћи у водама вулканског отпада. Хлороводоник је компонента минерала силвин (калијум хлорид, изгледа као кости за игре), бишофита. Све су то методе за екстракцију супстанце у индустрији.
Код људи, овај ензим се налази у желуцу. Раствор може бити киселина или база. Једна од најчешћих метода екстракције се зове сулфат.
Хемијска својства
Хлороводонична киселина, хлороводоник или хлороводонична киселина - раствор ХЦл
у води. Према Википедији, супстанца припада групи неорганских јаких једнобазних то-т. Пуно име једињења на латинском: хлороводонична киселина.
Формула хлороводоничне киселине у хемији: ХЦл
. У молекулу, атоми водоника се комбинују са атомима халогена - Цл
. Ако узмемо у обзир електронску конфигурацију ових молекула, може се приметити да једињења учествују у формирању молекуларних орбитала 1с
-водоникове орбитале и обоје 3с
и 3п
-орбитале атома Цл
. У хемијској формули хлороводоничне киселине 1с-
, 3с-
и 3р
-атомске орбитале се преклапају и формирају 1, 2, 3 орбитале. У чему 3с
-орбитала није обавезујућа. Постоји померање електронске густине на атом Цл
а поларитет молекула се смањује, али се енергија везивања молекуларних орбитала повећава (ако је посматрамо заједно са другим водоник халогениди
).
Физичка својства хлороводоника. То је бистра, безбојна течност која се дими када је изложена ваздуху. Моларна маса хемијског једињења = 36,6 грама по молу. У стандардним условима, на температури ваздуха од 20 степени Целзијуса, максимална концентрација супстанце је 38% по тежини. Густина концентроване хлороводоничне киселине у оваквом раствору је 1,19 г/цм³. Генерално, физичка својства и карактеристике као што су густина, моларност, вискозитет, топлотни капацитет, тачка кључања и пХ
, јако зависе од концентрације раствора. Ове вредности су детаљније размотрене у табели густина. На пример, густина хлороводоничне киселине 10% = 1,048 кг по литру. Када се очврсне, супстанца се формира кристални хидрати
различите композиције.
Хемијска својства хлороводоничне киселине. Са чиме реагује хлороводонична киселина? Супстанца ступа у интеракцију са металима који стоје испред водоника у низу електрохемијских потенцијала (гвожђе, магнезијум, цинк и други). У овом случају се формирају соли и гасовите Х
. Олово, бакар, злато, сребро и други метали десно од водоника не реагују са хлороводоничном киселином. Супстанца реагује са металним оксидима дајући воду и растворљиву со. Натријум хидроксид под дејством то-ти формира и воде. Реакција неутрализације је карактеристична за ово једињење.
Разређена хлороводонична киселина реагује са металним солима, које настају слабијим киселинама. На пример, пропионска киселина
слабије од соли. Супстанца не реагује са јачим киселинама. и натријум карбонат
ће се формирати након реакције са ХЦл
хлорид, угљен моноксид и вода.
За хемијско једињење карактеристичне су реакције са јаким оксидантима, со манган диоксид
, калијум перманганат
: 2КМнО4 + 16ХЦл = 5Цл2 + 2МнЦл2 + 2КЦл + 8Х2О
. Супстанца реагује са амонијак
, који производи густ бели дим, који се састоји од веома малих кристала амонијум хлорида. Минерал пиролузит такође реагује са хлороводоничном киселином, јер садржи манган диоксид
: МнО2+4ХЦл=Цл2+МнО2+2Х2О
(реакција оксидације).
Постоји квалитативна реакција на хлороводоничну киселину и њене соли. Када супстанца ступи у интеракцију са сребро нитрат
бели талог сребро хлорид
и формирана азотна киселина
. Једначина реакције интеракције метиламин
са хлороводоником изгледа овако: ХЦл + ЦХ3НХ2 = (ЦХ3НХ3)Цл
.
Супстанца реагује са слабом базом анилин
. После растварања анилина у води, смеши се додаје хлороводонична киселина. Као резултат, база се раствара и формира анилин хидрохлорид
(фениламонијум хлорид
): (С6Н5НХ3)Цл
. Реакција интеракције алуминијум карбида са хлороводоничном киселином: Ал4Ц3+12ХЦЛ=3ЦХ4+4АлЦл3
. Једначина реакције калијум карбонат
са којим то изгледа овако: К2ЦО3 + 2ХЦл = 2КЦл + Х2О + ЦО2.
Апликација
у металургији за вађење руда, уклањање рђе, каменца, прљавштине и оксида, лемљење и калајисање;
у производњи синтетичких гума и смола;
у галванизацији;
као регулатор киселости у прехрамбеној индустрији;
за добијање металних хлорида;
за добијање хлора;
у медицини за лечење недовољне киселости желудачног сока;
као средство за чишћење и дезинфекцију.
- (ХЦл), водени раствор хлороводоника, безбојни гас оштрог мириса. Добија се дејством сумпорне киселине на обичну со, као нуспроизвод хлорисања угљоводоника, или реакцијом водоника и хлора. Хлороводонична киселина се користи за ... ... Научно-технички енциклопедијски речник
Хлороводонична киселина
- - ХЦл (СЦ) (хлороводонична киселина, хлороводонична киселина, хлороводоник) је раствор хлороводоника (ХЦл) у води, адитив против смрзавања. То је безбојна течност оштрог мириса, без суспендованих честица. ... ... Енциклопедија појмова, дефиниција и објашњења грађевинских материјала
ХЛОРОВОДОНИЧНА КИСЕЛИНА
- (хлороводонична киселина) раствор хлороводоника у води; јака киселина. Безбојна течност која дими на ваздуху (техничка хлороводонична киселина је жућкаста због нечистоћа Фе, Цл2 итд.). Максимална концентрација (на 20°Ц) је 38% масе, ... ... Велики енциклопедијски речник
ХЛОРОВОДОНИЧНА КИСЕЛИНА
- (Ацидум муриатицум, Ацид, хидроцхлорицум), раствор хлороводоника (ХЦ1) у води. У природи се јавља у води одређених извора вулканског порекла, а налази се и у желудачном соку (до 0,5%). Хлороводоник се може добити ... Велика медицинска енциклопедија
ХЛОРОВОДОНИЧНА КИСЕЛИНА
- (хлороводонична киселина, хлороводонична киселина) јака једнобазна испарљива киселина оштрог мириса, водени раствор хлороводоника; максимална концентрација је 38% по маси, густина таквог раствора је 1,19 г/цм3. Користи се у ... ... Руској енциклопедији заштите рада
ХЛОРОВОДОНИЧНА КИСЕЛИНА
- (хлороводонична киселина) ХЦл водени раствор хлороводоника, јака једнобазна киселина, испарљива, оштрог мириса; нечистоће гвожђа, хлор боје жућкасто. Концентрисани С. за продају садржи 37% ... ... Велика политехничка енциклопедија
хлороводонична киселина
— именица, број синонима: 1 ацид (171) Речник синонима АСИС. В.Н. Трисхин. 2013 ... Речник синонима
ХЛОРОВОДОНИЧНА КИСЕЛИНА
Модерна енциклопедија
Хлороводонична киселина
- ВОДОНИЧНА КИСЕЛИНА, водени раствор хлороводоника ХЦл; димљива течност оштрог мириса. Хлороводонична киселина се користи за добијање разних хлорида, кисељење метала, прераду руда, у производњи хлора, соде, каучука итд. ... ... Илустровани енциклопедијски речник
хлороводонична киселина
- (хлороводонична киселина), раствор хлороводоника у води; јака киселина. Безбојна течност која "дими" у ваздуху (техничка хлороводонична киселина је жућкаста због нечистоћа Фе, Цл2 итд.). Максимална концентрација (на 20°Ц) 38% масе, ... ... Енциклопедијски речник
Која је опасност од интоксикације
Хлороводонична киселина је посебна опасност за људско тело. У случају тровања таквом супстанцом могу се развити озбиљне компликације и кршење функционалности тела.
компликације:
- Повреда јетре, као резултат токсичног хепатитиса,
- Крварење у стомаку због уништених зидова органа,
- Стање шока од бола када киселина уђе у велико подручје,
- У случају контакта са очима, оштећење вида,
- Озбиљни поремећај у раду бубрега,
- Респираторна инсуфицијенција, гушење, кратак дах,
- Развој коме.
Сличне последице се развијају постепено у зависности од степена тровања.
Закључак
Ако се придржавате мера предострожности и безбедносних правила, хлороводонична киселина ће постати незаменљив помоћник у свакодневном животу. И можете га купити по најповољнијим ценама у нашој компанији.
Као киселине. Образовни програм предвиђа памћење од стране ученика имена и формула шест представника ове групе. И, гледајући табелу коју пружа уџбеник, у листи киселина примећујете ону која је прва и која вас је на првом месту заинтересовала – хлороводоничну киселину. Авај, у учионици у школи се не проучава ни имовина ни други подаци о њој. Стога, они који су жељни сазнања ван школског програма траже додатне информације у свим могућим изворима. Али често, многи не пронађу информације које су им потребне. И тако је тема данашњег чланка посвећена овој киселини.
Дефиниција
Хлороводонична киселина је јака једнобазна киселина. У неким изворима може се назвати хлороводоничном и хлороводоничном, као и хлороводоником.
Физичка својства
То је безбојна и димљива каустична течност у ваздуху (слика десно). Међутим, техничка киселина има жућкасту боју због присуства гвожђа, хлора и других адитива у њој. Његова највећа концентрација на температури од 20 ° Ц износи 38%. Густина хлороводоничне киселине са таквим параметрима је 1,19 г/цм 3 . Али ово једињење у различитим степенима засићености има потпуно различите податке.Са смањењем концентрације, нумеричка вредност моларности, вискозитета и тачке топљења се смањују, али се повећава специфични топлотни капацитет и тачка кључања. Очвршћавање хлороводоничне киселине било које концентрације даје различите кристалне хидрате.
Хемијска својства
Сви метали који долазе испред водоника у електрохемијском низу њиховог напона могу да ступе у интеракцију са овим једињењем, формирајући соли и ослобађајући гас водоник. Ако се замене металним оксидима, онда ће производи реакције бити растворљива со и вода. Исти ефекат ће бити у интеракцији хлороводоничне киселине са хидроксидима. Међутим, ако јој се дода било која со метала (на пример, натријум карбонат), чији је остатак узет из слабије киселине (угљене), онда хлорид овог метала (натријум), вода и гас који одговарају киселини формирају се остаци (у овом случају угљен-диоксид).
Признаница
Једињење о коме се сада говори настаје када се гасовити хлороводоник, који се може добити сагоревањем водоника у хлору, раствори у води. Хлороводонична киселина, која се добија овом методом, назива се синтетичком. Излазни гасови такође могу послужити као извор за добијање ове супстанце. И таква хлороводонична киселина ће се звати издувна киселина. Недавно је ниво производње хлороводоничне киселине овом методом много већи од њене производње синтетичким методом, иако ова друга даје једињење у чистијем облику. Све су то начини да се то добије у индустрији. Међутим, у лабораторијама, хлороводонична киселина се производи на три начина (прва два се разликују само по температури и продуктима реакције) коришћењем различитих врста хемијских интеракција, као што су:
- Дејство засићене сумпорне киселине на натријум хлорид на температури од 150 о Ц.
- Интеракција горе наведених супстанци у условима са температуром од 550 ° Ц и више.
- Хидролиза хлорида алуминијума или магнезијума.
Апликација
Хидрометалургија и електроформирање не могу без употребе хлороводоничне киселине, где је то потребно, за чишћење површине метала при калајисању и лемљењу и за добијање хлорида мангана, гвожђа, цинка и других метала. У прехрамбеној индустрији ово једињење је познато као адитив за храну Е507 - тамо је регулатор киселости неопходан да би се добила сода вода. Концентрована хлороводонична киселина се такође налази у желудачном соку било које особе и помаже у варењу хране. Током овог процеса смањује се његов степен засићености, јер. овај састав се разблажи храном. Међутим, са продуженим постом, концентрација хлороводоничне киселине у стомаку постепено се повећава. А пошто је ово једињење веома заједљиво, може довести до чира на желуцу.
Закључак
Хлороводонична киселина може бити и корисна и штетна за људе. Његов контакт са кожом доводи до тешких хемијских опекотина, а испарења овог једињења иритирају дисајне путеве и очи.
Али ако пажљиво рукујете овом супстанцом, може вам више пута бити од користи