Suyun donma noktası
Dondurma işlemi gerçekleşir sıfır dereceye kadar soğutulduğunda Celsius ölçeğinde. Bu her su için geçerli değildir. Moleküller kendilerini toz, tuz vb. parçacıklar olan safsızlıklara bağlar. Bu nedenle, saf veya damıtılmış su, bu safsızlıkların varlığı olmadan, Celsius sütunundaki düşük sıcaklıkların etkisi altında, normal sudan daha uzun süre sıvı halde kalabilir.
Diğer maddelerin donarken hacmi azalırken, suyun aksine artması da ilginçtir. Bunun nedeni, katı hale geçiş sırasında moleküller arasındaki mesafenin genişlemesidir. Hacim artmasına rağmen, donma sırasında kütle artmaz ve ılık su kadar ağırdır.
Birçok insan suyun neden kalın bir buz tabakasının altında donmadığını merak ediyor. Herhangi bir fizikçi, bir buz tabakasının altında, buzun yüzeyi bir ısı yalıtkanı görevi gördüğü için suyun donmadığını söyleyecektir.

Sıcak su neden soğuk sudan daha hızlı donar?
Sıcak veya ılık suyun soğuk sudan daha hızlı donduğu bilinmektedir. İnanılmaz ama gerçek. Bu keşif Erasto Mpemba tarafından yapılmıştır. Donmuş kütleyi kullanarak deneyler yaptı ve kütle sıcaksa daha hızlı donacağını buldu. Bunun nedeni, çalışmaların gösterdiği gibi, sıcak ve ılık suyun ısı transferinin yüksek olmasıdır.

Suyun donma noktası ve irtifa ilişkili midir?
Bildiğiniz gibi, yükseklikte basınç değişir, bu nedenle yükseklikte tüm sulu çözeltilerin katı hale geçiş sıcaklığı normal bir yüzeydeki sıcaklıktan farklıdır.
Yükseklikte sıcaklık değişimlerine örnekler:
- yükseklik 500 m - suyun donma noktası normal koşullar altında olduğu gibi sıfır ° C değil, zaten bir ° C varlığında;
- yükseklik 1500 m - kristalleşme yaklaşık üç ° C, vb. varlığında meydana gelir.

Basınç, suyun kristalleşme sürecini nasıl etkiler?
Basınç ve suyun kristalleşmesi arasındaki ilişkiyi anlarsanız, her şey oldukça basittir.
İlginç! Basınç ne kadar yüksek olursa, suyun buz kristallerine dönüşme hızı o kadar düşük ve kaynama noktası o kadar yüksek olur!
Bütün sır bu ve mantıklı düşünürseniz, baskıda bir azalma ile tüm göstergeler ters yöne gider. Bu nedenle, suyun kaynadığı sıcaklık yüz santigrat dereceye ulaşmadığından dağlarda bir şeyler pişirmek zordur. Tersine, buz düşük sıcaklıklarda bile erir.
Sulu çözeltilerin kristalleşme sıcaklığı
Su iyi bir çözücüdür ve bu nedenle diğer maddelerle kolayca birleşir. Ortaya çıkan çözümler, elbette, farklı koşullar altında donacaktır. Suya dayalı farklı çözeltileri dondurmak için birkaç sıcaklık kriteri seçeneği düşünün.
Su ve alkol. Suda çok miktarda alkol bulunduğunda, çok düşük sıcaklıkların varlığında donma işlemi başlayacaktır. Örneğin %60 su - %40 alkol oranında eksi 22.5 °C varlığında kristalleşme başlayacaktır.
Su ve tuz. Donmanın meydana geldiği sıcaklık, suyun tuzluluk derecesi ile doğrudan ilişkilidir. Prensip, suda ne kadar fazla tuz olursa, kristalleşme sıcaklığının o kadar düşük olmasıdır. Deniz suyunun nasıl donduğu, doğrudan tuz içeriği ile ilgilidir.
Su ve soda. Çözeltinin kristalleşme sıcaklığı yüzde 44 artı 7°C'dir.
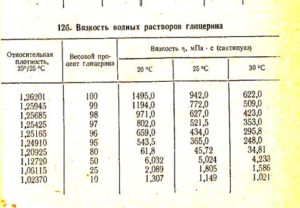
Su ve gliserin, %80 ila %20 oranında, 80 gliserin ve 20 su olmak üzere, çözeltiyi dondurmak için -20 °C'nin varlığı gereklidir.
Tüm sıcaklık değerleri, sudaki yabancı çözeltilerin veya diğer maddelerin konsantrasyon derecesine bağlı olarak dalgalanır.
Ostwald viskozimetresi ile sıvıların viskozitesinin ölçülmesi
Bir Ostwald kılcal viskozimetresi (Şekil 6) kullanılarak incelenen sıvının viskozite katsayısını ηhis belirlemek için şunları bilmek gerekir:
- η0 suyun viskozitesidir,
- t0, a ve b işaretleri arasındaki su akışının zamanıdır,
- tx, araştırılan sıvının a ve b işaretleri arasındaki akış süresidir,
- ρ0 suyun yoğunluğudur,
- ρx incelenen sıvının yoğunluğudur.
Pirinç. 6. Ostwald kılcal viskozimetre (a, b, d - sıvı seviyesini sınırlayan işaretler, c - kılcal).
İncelenen sıvının viskozitesi formül (9) ile belirlenir.
İş emri
Görev 1. Farklı konsantrasyonlarda çözeltilerin viskozitesini belirleyin.
-
Viskozimetrenin kılcal damarı olmayan (Şek. 6) ayağına d işaretine kadar su dökün.
-
Bir armutla, a'yı işaretlemek için kılcal damardan sıvıyı emdirin. Armutu çıkardıktan sonra, viskozimetrenin sol dizindeki deliği kapatın (el, mantar, çubuk vb. ile) (bkz. Şekil 6). Kronometreyi hazırlayın ve açın, sol dizin deliğini açın ve b işareti aktığında kapatın, böylece t0 - a ve b işaretleri arasındaki su akış süresini belirleyin.
-
Ölçümleri 4-5 kez tekrarlayın, ortalama süreyi bulun.
-
Tüm test sıvıları için 1-3 arasındaki adımları uygulayın.
-
Formül (9)'u kullanarak çalışılan sıvıların viskozite katsayılarını hesaplayın.
-
Tablo 1'deki verileri girin.
tablo 1
| № | Konsantrasyon, % | t1 | t2 | t3 | t4 | t5 | | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 | ||||||||
| 5 | ||||||||
| 6 |
Görev 2. Bilinmeyen bir çözeltinin konsantrasyonunu belirleyin.
-
Plot Viskozite Oranı ve Çözelti Konsantrasyonu
-
Bilinmeyen çözeltinin viskozitesini bilerek, konsantrasyonunu grafikten belirleyin.
Tablo 2
Farklı sıcaklıklarda suyun yoğunluğu
| ρ, kg/m3 | t, 0C | ρ, kg/m3 | t, 0C |
| 999,13 | 15 | 998,02 | 21 |
| 998,97 | 16 | 997,80 | 22 |
| 998,80 | 17 | 997,57 | 23 |
| 998,43 | 19 | 997,32 | 24 |
| 998,23 | 20 | 997,07 | 25 |
Tablo 3
Farklı sıcaklıklarda suyun viskozitesi
| η, Pa.s | t, 0C | η, Pa.s | t, 0C |
| 0,00114 | 15 | 0,00098 | 21 |
| 0,00111 | 16 | 0,00096 | 22 |
| 0,00108 | 17 | 0,00093 | 23 |
| 0,00103 | 19 | 0,00091 | 24 |
| 0,00100 | 20 | 0,00089 | 25 |
Tablo 4
Çeşitli konsantrasyonlarda gliserin çözeltilerinin yoğunluğu
| İLE, % | ρ, kg/m3 | İLE, % | ρ, kg/m3 |
| 5 | 1012,5 | 45 | 1112,5 |
| 10 | 1025,0 | 50 | 1125,0 |
| 15 | 1037,5 | 55 | 1137,5 |
| 20 | 1042,5 | 60 | 1150,0 |
| 25 | 1052,5 | 65 | 1162,5 |
| 30 | 1075,0 | 70 | 1175,0 |
| 35 | 1087,5 | 75 | 1187,5 |
| 40 | 1100,0 | 80 | 1200,0 |
Konuyla ilgili bağımsız çalışma:
– durumsal problemlerin çözümü;
- özetleri dinlemek
Bilginin son kontrolü:
– bilet sorunlarının çözülmesi;
– nihai kontrol biletlerine verilen yanıtlar;
- özetleme.
Dersin konusunu anlamak için ev ödevi
Dersin konusuyla ilgili kontrol soruları:
1. Bir sıvının viskozitesine ne denir?
2. Ne tür bir sıvı akışına laminer denir Türbülanslı?
3. Reynolds formülünü karakterize eden nedir?
4. Newton'un formülünü yazın ve içerdiği niceliklerin fiziksel anlamını açıklayın?
5. Dinamik viskozite katsayısı nedir? Hangi birimlerde ölçülür?
6. Hangi sıvılara Newtonian denir? Viskozite katsayılarını ne belirler?
7. Hangi sıvılara Newtonian olmayan denir, onların viskozite katsayısını ne belirler?
8. Poiseuille formülünü yazın, içerdiği niceliklerin fiziksel anlamını açıklayın.
9. Bir sıvının viskozitesini belirlemek için hangi yöntemler kullanılır?
10. Kan ve diğer biyolojik sıvıların reolojik özelliklerini, tıpta reolojik analizlerin kullanımını anlatır.
11. Hız gradyanı neyi gösterir? Grafiksel olarak göster.
12. Hangi fenomene iç sürtünme denir?
Konuyla ilgili görevleri test edin:
ISITMADA GLİSERİN UYGULAMASI GEREKLİ Mİ?
Isıtma sistemleri için soğutucuya oldukça yüksek gereksinimler uygulanır. Yangına ve patlamaya dayanıklı olmalı, iyi bir termal performans sağlamalı ve ayrıca kullanımı yasaklanmış katkı maddeleri içermemelidir. Etilen glikol veya propilen glikol, aynı zamanda çevre dostu olmasını sağlayan yüksek kaliteli ısı transfer sıvısının üretimi için temel olarak kullanılır.
Son zamanlarda, piyasada gliserin bazlı antifriz soğutucuları ortaya çıktı. Bu ürün, esas olarak antifriz pazarındaki küçük, az bilinen firmalar tarafından tanıtılmaktadır. Soru ortaya çıkıyor: gliserin ve soğutucu - sendikaları uygun mu?
Ve gerçekten de, geçen yüzyılın yirmili yıllarında ülkemizde ortaya çıkan ilk antifrizler gliserin bazında yapıldı. Zayıflıkları yetersiz akışkanlık ve pompaların kaldıramayacağı aşırı yüksek viskoziteydi. Metil alkol de dahil olmak üzere alkol yardımıyla sorunu çözmeye çalıştılar. Ancak akışkanlığın artmasıyla birlikte birçok sorun ortaya çıktı. Gerçek şu ki metanol güçlü bir psikotropik zehirdir.Sonuç olarak, bu tür antifrizi istemeden koklayan sürücülerin davranışları bazen herhangi bir mantığa meydan okuyor ve başkalarının sağlığı ve yaşamı için tehlike oluşturuyordu. Ayrıca metil alkolün kaynama noktası düşüktür ve buharlaştığında ürünün viskozitesi hemen artar. Sorun ancak etilen glikol soğutucunun temeli haline geldiğinde çözüldü. Otuzların sonunda, kırkların başında, etilen glikol antifrizleri neredeyse tamamen gliserin-metanolün yerini aldı.
Ek olarak, gliserin termal olarak kararsızdır, uzun süreli ısıtma sırasında zehirli bir uçucu madde oluşumu ile ayrışır - yırtılmaya neden olan keskin ve hoş olmayan bir kokuya sahip olan akrolein. Bozunma ürünleri toksiktir ve çökeltme, soğutma sıvısının aşındırıcı aktivitesini arttırır. Sonuç olarak, polar olmayan kauçuk ve plastikten yapılmış contalar ve parçalar için gereksinimler artmaktadır. Yüksek viskoziteye ek olarak, gliserin de yoğun bir şekilde köpürür, bu da sistemin havalandırılmasına ve zayıf ısı dağılımına yol açar.
Gliserin soğutucu üreticileri, alifatik alkoller - metanol, etanol, propanol dahil olmak üzere çeşitli katkı maddeleri ekleyerek yukarıdaki tüm dezavantajları telafi etmeye çalışıyorlar. Bu alkoller, antifriz soğutma sıvısının viskozitesini veya yoğunluğunu önemli ölçüde azaltabilir. Ancak zaten 65 derecenin üzerindeki sıcaklıklarda kaynarlar, bu da soğutucunun termal performansında bozulmaya neden olur. Bu alkoller, kauçuğu ve polimerleri çözebilir ve ayrıca kavitasyona ve güçlü buharlaşmaya eğilimlidir. Ayrıca metanol güçlü bir zehirdir ve antifriz sıvılarının üretiminde kullanılması yasaktır.
Özellikle metanol ile gliserin soğutucularının kalitesinin sağlanması, karışıma pahalı katkı paketlerinin eklenmesini gerektirir. Ve gliserin maliyeti şimdi glikollerin maliyetinden daha düşük olmasına rağmen, kaliteli gliserin ısı transfer sıvıları yapmak için katkı paketi, etilen glikol ve propilen glikol bazlı antifriz katkı paketinden daha pahalıdır. Ve piyasadaki gliserin antifrizinin maliyeti glikolün maliyetinden düşükse, bu üreticinin kaliteden tasarruf ettiği ve ürüne gerekli pahalı katkı maddelerini eklemediği anlamına gelir!
Bu nedenle seçim alıcıya kalmıştır: ya glikollere dayalı güvenilir ve kanıtlanmış bir soğutma sıvısı ya da bir gliserin "pig in a poke".
Önde gelen antifriz üreticilerinin çoğu gibi şirketimizin seçimi de temelde açık - gliserin saf haliyle kullanılamaz, ancak metanol ile karıştırılması tehlikeli ve suçtur!
Bu konudaki tutumumuzu doğrulayan ana argüman, önemli ve büyük herhangi bir tesiste, ısıtma ve soğutma sistemlerinde gliserin kullanımına mevcut standartlar tarafından İZİN VERİLMEZDİR!
MEG
Etilen glikol, sülfürik veya fosforik asit varlığında etilen oksit hidrasyonunun bir ürünüdür. Polihidrik alkolleri ifade eder. Düşük sıcaklıklarda donmaz ve suyun donma noktasını düşürür. Havadan su çekebilme özelliğine sahiptir.
227 litreye kadar metal ve plastik varillerde satılmaktadır. 1000l plastik küplerin yanı sıra.
Maddeyi, kapalı bir depoda, ısıtma olmadan, korozyon önleyici korumalı alüminyum veya çelikten yapılmış sızdırmaz bir kapta saklamak gerekir. En yüksek kalite için raf ömrü 12 aydır, birinci sınıf için üretim tarihinden itibaren 3 yıldır.
Göstergenin adı Norm
Görünüm, koku Yağlı bir dokuya sahip berrak, renksiz sıvı. Kokusuz.
Suda, alkollerde, toluen, benzende çözünür
Yoğunluk 1.112 g/cm?.
Erime noktası 12.9 santigrat derece
Kaynama noktası 197.3 santigrat derece
Uygulama
Donma noktasını düşürme kabiliyeti nedeniyle, monoetilen glikol, otomobiller için antifriz ve fren hidroliği üretiminde ve ayrıca selofan ve poliüretan imalatında kullanılır. Daha az oranda mürekkep ve matbaa mürekkeplerinin üretiminde kullanılmaktadır.
Tehlike Sınıfı
Yanıcı maddelere atıfta bulunur. Kendiliğinden tutuşma, 380 derecelik bir sıcaklıkta meydana gelir, 120 dereceye kadar ısıtıldığında bir buhar parlaması. Toksik. Yutmaya izin verilmez. Buharlar daha az zararlıdır.
gliserol
Kimyasal formül: HOCH2CH(OH)CH2OH
Uluslararası isim: Gliserin
CAS NUMARASI: 56-81-5
Vasıf: İth. "h", GOST 6259-75
Görünüm: şeffaf, kokusuz sıvı
Paketleme: 25 kg bidon, 250 kg bidon, 1500 küp
Depolama koşulları: düşük sıcaklıkta havalandırılmış kuru bir odada
Eş anlamlı: 1,2,3-trioksipropan
Gliserin'i teneke, fıçı, küp şeklinde rekabetçi fiyatlarla sunuyoruz.
| Şartname | |
| Moleküler ağırlık | 92.10 |
| Temel madde, en az | %99,5 (gerçek %99,8) |
| Kül içeriği, artık yok | %0.01 (aslında %0.1'den az) |
| Su içeriği, artık yok | %0.5 (aslında %0.1) |
| Klorür içeriği, artık yok | 0,001 % |
| Sülfat içeriği, artık yok | 0,002 % |
| Ağır metaller, artık yok | %0,0005 (aslında %0,0005'ten az) |
| Klor bileşikleri (CL olarak), artık yok | 0,003 % |
| Arsenik, artık yok | %0.00015 (gerçek %0.00001'den az) |
| Renkli (APHA), artık yok | 20 (aslında 10'dan az) |
Gliserin renksiz, higroskopik, viskoz, kokusuz, tatlı tadı olan bir sıvıdır. Su, etanol, metanol, aseton ile her oranda karışabilir, kloroform ve eterde çözünmez. Gliserol su ile karıştırıldığında ısı açığa çıkar ve büzülme meydana gelir (hacim azalması). Gliserol hidrohalik asitler veya fosfor halojenürler ile etkileşime girdiğinde mono- veya dihalohidrinler oluşur; inorganik ve karboksilik asitlerle - dehidrasyon ile tam ve eksik esterler - akrolein. Gliserol oksitlenebilir ve oksitleyici maddenin koşullarına ve doğasına bağlı olarak gliseraldehit, gliserik asit, tartronik asit, dihidroksiaseton, mezoksalik asit elde edilebilir. Gliserin, doğal katı ve sıvı yağlarda karboksilik asitlerin karışık trigliseritleri olarak bulunur.
Uygulama Gliserin, ilaç endüstrisinde • örneğin nitrogliserin, tıbbi merhemlerin üretimi için yaygın olarak kullanılmaktadır; • gıda endüstrisinde, örneğin likör, şekerleme üretiminde; • kozmetik endüstrisinde, parfüm ve kozmetik imalatında • gliftal reçinelerin üretiminde; • kumaşlar, deri, kağıt için yumuşatıcı olarak; • emülgatörlerin, antifrizlerin, yağlayıcıların, ayakkabı cilalarının, sabunların ve yapıştırıcıların bir bileşeni olarak, • çeşitli köpüklerde kullanılan polialkollerin üretiminde hammadde olarak. • selofan vb. için plastikleştirici olarak.
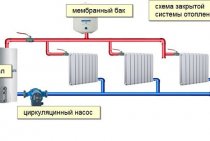
Bir konut binasındaki ısıtma borularında su hangi sıcaklıkta donar?
Evdeki sıcaklık birkaç gün boyunca -10'da kalırsa ve borularda su varsa, o zaman donabilir ve bu da boruların yırtılmasına neden olur. Birçoğu muhtemelen su tahliye işlevine sahip modern ısıtma pilleri gördü. Hemen hemen tüm modern piller, suyu tahliye etme özelliği ile donatılmıştır. Bu, acil bir durumda, evdeki sıcaklık -10 olduğunda, suyun donmaması ve boruların yırtılmaması için yapılır. Durum bu noktaya geldiyse, size çok sempati duyuyoruz, büyük olasılıkla pilleri değiştirmeniz gerekecek, çünkü suyun donması sırasında, muhtemelen bu pillerin daha fazla çalışmasını tehlikeli hale getiren mikro çatlaklar meydana geldi.
Su neden borularda donabilir? Isıtma mevsiminde, piller su doldururken arıza meydana gelir ve su soğur ve dışarıdaki sıcaklık hızla düşerse, bu boruların donmasına neden olabilir.
Suyun hangi sıcaklıkta donduğu sorusunu zaten cevapladık, bir deney olarak küçük bir bardak alın, yarısına kadar suyla doldurun ve birkaç saat dondurucuya koyun, suyun kısmen buza dönüşmesi için iki saat yeterlidir.
Su, gezegenimizdeki en temel maddelerden biridir. Onu bir dereceye kadar benzersiz kılan birçok özelliğe sahiptir. Küçük bir çocuğun bile bildiği en ünlü özelliklerden biri suyun donmasıdır.0 santigrat derecenin suyun kristalleşme sıcaklığı olduğu bilinmektedir. Ama her şey o kadar basit değil. Bu sürecin bazı inceliklerini daha ayrıntılı olarak ele alacağız.

25'te gliserin çözeltisinin yoğunluğu
Alkol ve gliserol yoğunluklarının aritmetik ortalaması.
209.4. 1.047. 25.265.0. 1.060. ... Diğer sözlüklerde gliserin sulu çözeltilerinin yoğunluğunun ne olduğunu görün E236 Dosya Formik asit.svg Formik asidin yapısal formülü Formik asit metanoik asit ilk ...
17 santigrat derecede gliserin yoğunluğu nedir?
8
25 C'de yoğunluk, g cm. ...% 25 veya daha fazla konsantrasyonda bir gliserin çözeltisi, mikrobiyal kontaminasyona maruz kalmaz, daha seyreltik çözeltilerde, mikroorganizmalar içinde iyi çoğalır.
3,14
Hangi sıvının yoğunluğu daha yüksektir, gliserin veya alkol? açıklamak
sss
Rusya genelinde sitede TK-Nisan. Gliserol 15 С çözeltilerinin konsantrasyonu, yoğunluğu ve kırılma indisi. … 1.0594. 1.3633. 25.1.0620.
Her iki maddenin molar kütlesini hesaplayın. Alkol için daha azdır (alkol için 92 g / mol ve 46 g / mol) ve yoğunluk buna bağlı olarak daha düşüktür. Etil alkole gelince.
Bu tür soruların amacı nedir? Bilgi arama motorlarında bulunur
Karışımın bileşenlerinin yoğunluklarının aritmetik ortalaması.
Sulu bir çözelti c.42 hazırlamak için 1.26 g ml yoğunluğa sahip hangi gliserol kütlesinin alınması gerektiğini belirleyin. ... 111 g ftalik anhidrit ve 28 V yoğunluğa sahip 46 g gliserin, 0.25 l kapasiteli bir cam behere yerleştirilir.
Su, alkol ve gliserin içeren bir sıvının yoğunluğu ve viskozitesi nasıl hesaplanır?
Bunun için reometreler satılmaktadır. hiçbir şey saymak zorunda değilsin. sadece dondur.
trietilen glikol. propilen glikol. Gliserol. … propilen glikol %40. -25 C. ... Çeşitli sıcaklıklarda etilen glikolün sulu çözeltilerinin yoğunluğu.
Karışımın tüm bileşenlerinin yüzdesini bilmeniz gerekir (en azından!)
Mümkün değil. Birisi tarafından alınan verileri arayın.
Lütfen yardım edin, bir parça buz benzin, gazyağı, gliserin içinde yüzer mi? niye ya?
Gliserin içinde olacak, viski içinde yüzmeyecek - yoğunluk benzinle hemen hemen aynı
Ayrıca bitmiş çözeltinin yoğunluğunu arttırır ve baloncukların kalitesini iyileştirir. ... Gliserin solüsyonu 25g şişe Tula Pharmaceutical Factory LLC. … Gliserin flakonda sodyum tetraborat solüsyonu 20% 30g, Samara FF, Samara Rusya.
Buz, yağdan daha az yoğundur, yani öyle olacaktır.
Buzun yoğunluğunu bu sıvıların yoğunluğuyla karşılaştırın. buzun yoğunluğu az ise yüzer, fazla ise batar.
Bilmemek. hangi parça olduğuna bağlı buzun içinde onu yüzeyde tutmaya yetecek kadar hava varsa yüzer, değilse yüzemez. kendin dene. gazyağı ucuzdur.
Bu buzun hangi sıcaklığa soğutulduğuna bağlı olarak
Sulu gliserin çözeltilerinin kaynama noktası,% 5 su içeriğine sahip gliserol konsantrasyonunda bir azalma ile azalır, kaynama noktası 160-161, yoğunluğu 1.26362 g cm3'tür. … 25 25 C . ZnCl2.
Benzin deposunda ve bidonunda yüzen buz görmedim. Ve kesinlikle öyle))). Yani muhtemelen en alttadır. Gliserini sadece bir şişede ve ısıda gördüm))).
Oy!
X miktarı seyreltilmiş gliserol, g Damıtılmış gliserol yoğunluğu, g ml ... % 25 ve üzeri konsantrasyondaki gliserol çözeltileri mikrobiyal kontaminasyona tabi değildir, daha seyreltik çözeltiler ...
Bir parça buz benzin, gazyağı, gliserin içinde yüzer mi?
Yoğunluğu öğrenin ve hepsi bu!
Alkollerin sulu çözeltilerinin yoğunluğu. Aşağıdaki maddeler için 20°C'de g cm3 sulu çözeltilerin yoğunlukları verilmiştir: etanol, 1-propanol, 2-propanol, etilen glikol, gliserol, D-mannitol.
Evet)))
Buzun yoğunluğu sıvının yoğunluğundan küçükse buz yüzer
24 gr sıcaklıkta gliserin yoğunluğu nedir? İLE?
Gliserin Derecesi Celsius020406080100120140169180Yoğunluk g/cm3126712591250123812241208118811631126
24 derecelik bir sıcaklık için = 20 ile 40 derece arasında enterpolasyonla belirleyin
Aseton içinde %8'lik bir gliserol C3H6O3 çözeltisinin kaynama noktasını hesaplayın. Cevap 57.7oC'dir. 4.100 ml'si 2.3 g içeren bir çözelti ... Çözeltinin yoğunluğunu bire eşit alın. Cevap 608 Pa. Bilet 14 25 1. BaCl2 2H2O kaç gram ...
Kimya Soruları))) Ve Fizik. Hangi sıvı sudan daha yoğundur ve ayrıca elektriği iletir, ancak metali iletmez?
Gliserin, etilen glikoller, formamidler, butirolakton, hemen hemen tüm asitler, aminler. ve daha fazlası.
Sülfürik asit konsantrasyonu, kütlece %. 25 C'de yoğunluk, g cm ... 25.60-0.1950 0.000 8 - bağıl nem,% - D hattı sodyum için 25 C'de sulu bir gliserol çözeltisinin kırılma indisi - çözelti sıcaklığı, C ...