Yếu tố quyết định độ mặn của nước biển
Thấy con số cao hơn một chút 3,5 ppm
, bạn có thể nghĩ rằng đây là một hằng số đối với bất kỳ nước biển nào trên hành tinh của chúng ta. Nhưng mọi thứ không đơn giản như vậy, độ mặn tùy thuộc vào từng vùng. Nó chỉ xảy ra rằng khu vực nằm càng xa về phía bắc, giá trị này càng lớn.
Ngược lại, miền nam tự hào có biển và đại dương không quá mặn. Tất nhiên, tất cả các quy tắc đều có ngoại lệ. Nồng độ muối trong biển thường thấp hơn một chút so với trong đại dương.
Sự phân chia địa lý nói chung là gì? Nó không được biết đến, các nhà nghiên cứu coi đó là đương nhiên, có tất cả mọi thứ. Có lẽ câu trả lời nên được tìm kiếm trong những thời kỳ trước của sự phát triển của hành tinh chúng ta. Không phải ở thời điểm mà sự sống được sinh ra - sớm hơn nhiều.
Chúng ta đã biết rằng độ mặn của nước phụ thuộc vào sự hiện diện của:
- magie clorua.
- natri clorua.
- các muối khác.
Có lẽ, ở một số vùng của vỏ trái đất, sự lắng đọng của các chất này có phần lớn hơn ở các vùng lân cận. Mặt khác, không có người hủy bỏ hải lưu, sớm muộn gì trình độ chung quy cũng phải chững lại.
Vì vậy, rất có thể, một sự khác biệt nhỏ có liên quan đến các đặc điểm khí hậu của hành tinh chúng ta. Không phải là ý kiến vô căn cứ nhất, nếu bạn nhớ các sương giá và xem xét những gì chính xác nước có hàm lượng muối cao đóng băng chậm hơn.
Giai đoạn đông lạnh
Rất thú vị khi xem cách nước biển đóng băng. Nó không ngay lập tức được bao phủ bởi một lớp vỏ băng đồng nhất, giống như nước ngọt. Khi một phần của nó biến thành đá (và nó còn tươi), phần còn lại của thể tích thậm chí còn trở nên mặn hơn và cần phải có một lớp sương giá mạnh hơn nữa để đóng băng nó.
Các loại đá
Khi nước biển nguội đi, các loại băng khác nhau hình thành:
- bão tuyết;
- bùn thải;
- kim tiêm;
- Salo;
- bản đồ.
Nếu nước biển chưa đóng băng mà ở rất gần, lúc đó tuyết rơi, không tan khi tiếp xúc với bề mặt mà bị bão hòa với nước và tạo thành một khối nhão nhớt gọi là tuyết. Để đông lại, cháo này thành cặn, rất nguy hiểm cho tàu gặp bão. Bởi vì nó, boong ngay lập tức được bao phủ bởi một lớp vỏ băng.
Khi nhiệt kế đạt đến mức cần thiết để đóng băng, kim băng bắt đầu hình thành trong nước biển - các tinh thể ở dạng lăng trụ lục giác rất mỏng. Dùng lưới thu gom chúng, rửa sạch muối cho tan, bạn sẽ thấy chúng vô vị.
Khi trời trở nên lạnh hơn, chất béo bắt đầu đông lại và tạo thành lớp vỏ băng, trong suốt và dễ vỡ như thủy tinh. Băng như vậy được gọi là nilas, hoặc chai. Nó có vị mặn, mặc dù nó được hình thành từ kim không men. Thực tế là trong quá trình đóng băng, những chiếc kim sẽ thu những giọt nước muối nhỏ nhất xung quanh.
Chỉ ở những vùng biển mới có hiện tượng như băng trôi. Nó phát sinh do nước ở đây nguội nhanh hơn ngoài khơi. Băng hình thành ở đó đóng băng đến rìa bờ biển, đó là lý do tại sao nó được gọi là băng nhanh. Khi băng giá gia tăng trong thời tiết lặng gió, nó nhanh chóng chiếm lấy các vùng lãnh thổ mới, đôi khi có chiều rộng lên tới hàng chục km. Nhưng ngay khi có gió mạnh nổi lên, băng nhanh chóng bắt đầu vỡ thành nhiều mảnh với nhiều kích cỡ khác nhau. Những tảng băng này, thường rất lớn (những cánh đồng băng), được mang theo gió và dòng điện đi khắp biển, gây ra sự cố cho tàu bè.
Khử mặn nước biển.
Về khử muối, chắc hẳn ai cũng đã nghe ít nhiều, thậm chí có người còn nhớ đến bộ phim “Water World”. Thực tế đến mức nào khi đặt một chiếc máy chưng cất di động như vậy trong mỗi ngôi nhà và mãi mãi quên đi vấn đề nước uống cho nhân loại? Vẫn là hư cấu, không phải hiện thực.
Đó là tất cả về năng lượng tiêu tốn, bởi vì để hoạt động hiệu quả cần phải có công suất lớn, không kém gì một lò phản ứng hạt nhân. Một nhà máy khử muối ở Kazakhstan hoạt động theo nguyên tắc này.Ý tưởng cũng đã được đệ trình ở Crimea, nhưng sức mạnh của lò phản ứng Sevastopol không đủ cho những khối lượng như vậy.
Nửa thế kỷ trước, trước vô số thảm họa hạt nhân, người ta vẫn có thể cho rằng một nguyên tử hòa bình sẽ xâm nhập vào mọi nhà. Thậm chí còn có một khẩu hiệu. Nhưng rõ ràng là không sử dụng các lò phản ứng vi mô hạt nhân:
- Trong các thiết bị gia dụng.
- Tại các xí nghiệp công nghiệp.
- Trong việc chế tạo ô tô và máy bay.
- Và có, trong giới hạn thành phố.
Không được mong đợi trong thế kỷ tới. Khoa học có thể có một bước nhảy vọt khác và khiến chúng ta ngạc nhiên, nhưng cho đến nay đây chỉ là những tưởng tượng và hy vọng của những câu chuyện lãng mạn bất cẩn.
Điểm đông đặc của nước cất
Nước cất có đóng băng không? Nhắc lại rằng để nước đông lại, cần phải có một số trung tâm kết tinh trong đó có thể là bọt khí, các hạt lơ lửng, cũng như làm hỏng thành bình chứa nó.
Nước cất, hoàn toàn không có bất kỳ tạp chất nào, không có hạt nhân kết tinh, và do đó sự đông đặc của nó bắt đầu ở nhiệt độ rất thấp. Điểm đóng băng ban đầu của nước cất là -42 độ. Các nhà khoa học đã cố gắng đạt được độ siêu lạnh của nước cất đến -70 độ.
Nước đã tiếp xúc với nhiệt độ rất thấp nhưng không kết tinh được gọi là "siêu lạnh". Bạn có thể đặt một chai nước cất vào ngăn đá, hạ thân nhiệt và sau đó biểu diễn một mẹo rất hiệu quả - xem video:
Bằng cách gõ nhẹ vào một cái chai được lấy ra khỏi tủ lạnh hoặc bằng cách ném một cục đá nhỏ vào đó, bạn có thể thấy nó biến thành đá ngay lập tức như thế nào, trông giống như những tinh thể dài ra.
Nước cất: chất tinh khiết này có bị đóng băng hay không dưới áp suất? Quá trình như vậy chỉ có thể thực hiện được trong các điều kiện phòng thí nghiệm được tạo ra đặc biệt.
ÑÐ ° ÑÑоР»ÑемпеÑÐ ° ÑÑÑÐ °
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ · α α ð ð ð ð ð ð ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð đồng Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nữa Ð. Ð nữa Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ð nay Ð Ð Ð Nhà Ð Nhà Ð tháng, Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ ðộ ð- ÑиÑÑÑ. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Nhà Ð doanh Ð doanh Ð. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð giờ Ðộ ñññ Ð- Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðơn Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðơn Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ð doanh Ð doanh Ðài »Ð ²ÐÐРооо²²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ²Ð Ð Ð ² DND »D ÑоÐ'ÐμÑжР° ниÐμ Ñол D в NĐ ° ÑÑоР»Ðμ мÐμнÑÑÐμ, ÑÐμм ÑÑÐμÐ ± ÑÐμмоÐμ Ð'л Ñ ÑвÑÐμкÑиÑÐμÑкого NĐ ° ÑÑвоÑÐ °, воÐ'Ð ° ÑÑкоÑÐ¸Ñ Ð¾Ð ± ÑÐ ° Ð · овР° ние кÑиÑÐ ° Ð »Ð» ов Ð »ÑдР° пÑи оÑл Ð ° жденÑÑÐ ° иР»Ð´Ð ° пÑÐ ¸ оÑÐ »Ð ° жденÑÑÐ ° иоиии Chạy ñðμμððμð½ððμÐμРо Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nó Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nữa Ð nữa Ð Ð nữa Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nữa Ð nữa Ð. еÑонÑенÑÑÐ ° ÑÐ¸Ñ Ñоии оÐÑÐ ° Ð »Ñном ÑÐ ° ÑÑвое. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð thời Ð tỷ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð được Ð. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð thời Ð tỷ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð được Ð. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð đang Ðang Ðang Ðộ Ðộ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Mẫu Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð năm Ð năm Ð. Ð Ð Ð Ð Ð μñ DD ° мÐμÑÐ · Ð ° ниÐμ ÑвÑÐμкÑиÑÐμÑкого NĐ ° ÑÑвоÑÐ ° á ÑÑо пÑоÑÐμÑÑ Ñ NND ° ÑÑиÐμм ÑкÑÑÑой ÑÐμпР»Ð¾ÑÑ, поÑÑÐ¾Ð¼Ñ ÑÐμмпÐμÑÐ ° ÑÑÑÐ ° оÑÑÐ ° ÐμÑÑÑ Ð½ÐμиР· менной. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð tức Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð tức Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð tức Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð điều Ð Ð nữa Ð Ð Ð Ð Ð Ð Ð ² Ð ¿Ñипонижении Ð · ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ñ nh ð ð ð ð ð ð ð ð ð ð ñ ñ nh ð ð ð ð ð ð ð ð ð ð ð ð ð ñ nh ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ñ nh ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ð năm Ð. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Mẫu Ð tỷ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ðảng Ð. Ð Ð Ð Ð Ð Ð ° ¸ поÑоÑннойÐÐ ° нн Ðй пÐоÐÐμÑÑ ÐÑимÐμнÐμÑÑÑ ² пР»Ð ° ÑÑинÑÐ ° ÑÑÑÑÑ ÑA Ñ ÑA ÑA ÑA ÑA Ñ .
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðộ Ðộ Ð Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ð? ¸Ñ и ÑÐ »Ð¾ÑидР° нР° ÑÑиÑ. Ð ° ÑÐÐ²Ð¾Ñ ÑÐ »Ð¾ÐиÐ'Ð ° кР° л ÑÑÐ¸Ñ Ð¿ÑÐμжÐ'Ðμ вÑÐμго оÐпоР»ÑÐ · ÑÐμÑÑÑ ÑAÑÑÐÑ ÑAÑ ÑO ¸ Ð · Ð ° моР° живР° нии пÑодÑкÑов, ÑÑÐ ° нении и Ñ.д. 17,8  ° С. Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ngủ Ð năm Ð. ((( Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 ° C Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Nhà Ð doanh Ð doanh Ð. (( Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð giờ Ð giờ Ð-Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay!! Ð (μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð rao Ð năm Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ð nay '' Ð Ð Ð Ð Ð Ð Ð Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ðảng Ð giờ Ðảng Ðồ Ðồ Ð. ° ÐºÑ ÑÐ ° ÑÑооР° ÑоÑÐ »Ð ° ждР° емÑм пÑодÑкÑом.
Ð ° ÑÐÐ²Ð¾Ñ ÑÐ »Ð¾ÐиÐ'Ð ° нР° ÑÑÐ¸Ñ (пиÑÐμвой Ñол и) нÐμ поÐÑÐ¸Ñ ÐиÑÐμвÑÐμ пÑоÐ'ÑкÑÑ. ¾¾ððð ° ° ðñððð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð đơn Ð đơn Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð năm năm Ð ((Ð dự Ðang Ðang Ðang) Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð nay · иÑеР»Ñно в21. 1  ° С. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Nhà Ð đơn Ð doanh Ð. (( Ð ·
CHU KỲ NƯỚC TRONG THẾ GIỚI ĐẠI DƯƠNG
Ở các vùng cực, nước khi nguội đi sẽ trở nên đặc hơn và chìm xuống đáy. Từ đó, nó từ từ trượt về phía xích đạo. Do đó, ở tất cả các vĩ độ, vùng biển sâu đều lạnh giá. Ngay cả ở xích đạo, các vùng nước đáy có nhiệt độ chỉ từ 1-2 ° trên không.
Vì các dòng chảy mang nước ấm từ xích đạo đến vĩ độ ôn đới, nước lạnh dâng lên rất chậm từ độ sâu để thế chỗ. Trên bề mặt, nó nóng lên trở lại, đi đến các vùng dưới cực, nơi nó nguội dần, chìm xuống đáy và lại di chuyển dọc theo đáy đến xích đạo.
Như vậy, trong các đại dương có một loại chu trình nước: trên bề mặt, nước di chuyển từ xích đạo đến các đới cận cực và dọc theo đáy đại dương - từ các đới cận cực đến xích đạo. Quá trình trộn nước này, cùng với các hiện tượng khác được đề cập ở trên, tạo nên sự thống nhất của các đại dương.
Nếu bạn tìm thấy lỗi, vui lòng đánh dấu một đoạn văn bản và nhấp vào Ctrl + Enter
.
Trong phần câu hỏi về nhiệt độ thấp nhất của dung dịch muối ăn thông thường (dạng bảng, NaCl) có thể đạt được do tác giả đưa ra Châu âu
câu trả lời tốt nhất là Bằng cách thêm muối vào nước, tốc độ tan chảy của nước đá tăng lên và nhiệt độ tan chảy của nước đá giảm xuống thấp hơn. Điều này là do việc thêm muối làm suy yếu liên kết phân tử và phá hủy mạng tinh thể của băng. Sự tan chảy của hỗn hợp muối đá diễn ra đồng thời với việc loại bỏ nhiệt ra khỏi môi trường, do đó không khí xung quanh lạnh đi và nhiệt độ của nó giảm xuống. Khi hàm lượng muối trong hỗn hợp muối đá tăng lên, nhiệt độ nóng chảy của nó giảm. Dung dịch muối có nhiệt độ nóng chảy thấp nhất được gọi là eutectic, và nhiệt độ nóng chảy của nó được gọi là điểm đông lạnh. Điểm cryohydrat của hỗn hợp muối đá với muối ăn là -21,2 ° C, với nồng độ muối trong dung dịch là 23,1% so với tổng khối lượng của hỗn hợp, xấp xỉ bằng 30 kg muối trên 100 kg Nước đá.Khi tăng thêm nồng độ muối không phải là giảm nhiệt độ nóng chảy của hỗn hợp muối đá mà là tăng nhiệt độ nóng chảy (ở nồng độ muối trong dung dịch là 25% so với tổng khối lượng thì nhiệt độ nóng chảy tăng đến -8 ° C) .Khi làm đông đặc dung dịch nước muối ăn có nồng độ tương ứng với điểm đông đặc thì thu được hỗn hợp đồng nhất của nước đá và tinh thể muối, được gọi là dung dịch rắn eutectic. Nhiệt độ nóng chảy của dung dịch rắn eutectic của natri clorua là -21,2 ° C, và nhiệt của phản ứng tổng hợp là 236 kJ / kg. Giải pháp eutectic được sử dụng để làm mát bằng không mô-men xoắn. Để làm điều này, một dung dịch muối ăn eutectic được đổ vào các số không - dạng kín - và chúng được đóng băng. Các số không đông lạnh được sử dụng để làm mát quầy, tủ, túi giữ lạnh di động, v.v. (mở ngăn đá của tủ lạnh gia đình - bạn sẽ tìm thấy một thùng chứa như vậy). với máy làm mát.
Câu trả lời từ khô
nhiệt độ thấp nhất của bất kỳ nhiệt độ nào là không tuyệt đối, khoảng -273 độ C
Câu trả lời từ Olya
nhiệt độ phụ thuộc vào nồng độ muối trong dung dịch, nồng độ càng cao thì điểm đông càng giảm. cuốn sách tham khảo đã được lấy đi của tôi một thời gian)) nhưng nếu chúng ta tiến hành từ thực tế rằng nước biển là một dung dịch mặn, thì chúng ta có thể kết luận rằng nhiệt độ đóng băng thấp hơn nhiều ... độ -15-20
Câu trả lời từ có khả năng
Dung dịch nước NaCl 22,4% đóng băng ở 21,2 ° C
cho câu hỏi Dung dịch nước NaCl "nhiệt độ kết tinh"
Câu trả lời từ Yergey Neznamov
Bảng 10.8. Điểm đông đặc của dung dịch NaCl Hàm lượng NaCl, g trong 100 g nước 5 - -4,4 9,0 - -5,4 10,6 - -6,4 12,3 - -7,5 14,0 - -8,6 15,7 - -9,8 17,5 - -11,0 19,3 - - 12,2 21,2 - -13,6 23,1 - - 15,1 25,0 - - 16,0 26,9 - -18,2 29,0 - -20,0 30,1 - -21,2
Điểm đóng băng của nước muối
Các thí nghiệm với nước đá đối với trẻ em luôn thú vị. Tiến hành các thí nghiệm với Vlad, tôi thậm chí còn thực hiện một số khám phá cho chính mình.
Hôm nay chúng ta sẽ tìm câu trả lời cho những câu hỏi sau:
- Nước hoạt động như thế nào khi bị đóng băng?
- Điều gì xảy ra nếu bạn đóng băng nước muối?
- áo khoác sẽ làm ấm băng?
- và một số người khác…
nước Đông cứng

Nước muối có bị đóng băng không?
Nước càng mặn, điểm đóng băng càng thấp. Đối với thí nghiệm, chúng tôi lấy hai cốc - một cốc đựng nước ngọt (được đánh dấu bằng chữ B), trong một cốc nước rất mặn (được đánh dấu bằng chữ B + C).
Sau khi đứng trong tủ đá cả đêm, nước muối không đóng băng mà hình thành các tinh thể đá trong ly. Nước ngọt chuyển thành đá. Trong khi tôi thao tác với cốc và dung dịch muối, Vladik đã tạo ra thí nghiệm ngoài kế hoạch của mình.
Anh đổ nước, dầu thực vật vào một chiếc cốc và kín đáo để vào ngăn đá. 
Nước muối trong ngăn đá không đóng băng, nhưng điều gì sẽ xảy ra nếu bạn rắc muối vào đá? Hãy kiểm tra.
Trải nghiệm với đá và muối
Lấy hai viên đá lạnh. Rắc một trong số chúng với muối, và để thứ hai để so sánh. 
Chúng tôi đóng băng một tảng băng lớn và rắc muối lên, lấy bàn chải và 
Sự sáng tạo đầy kinh nghiệm của chúng tôi đã gắn kết cả gia đình, vì vậy bút của Makarushkin đã lọt vào ống kính máy ảnh!
Makar và Vlad rất mọi người đều thích đóng băng
. Đôi khi có những món hoàn toàn không mong muốn trong tủ đông.
Tôi đã mơ ước được thực hiện trải nghiệm này từ khi còn nhỏ, nhưng mẹ tôi không có áo khoác lông, và nhiều

Thật tuyệt vời biết bao khi trở thành một người lớn, có một chiếc áo khoác lông thú và làm đủ thứ thí nghiệm cho trẻ em!
Galina Kuzmina của bạn
Bảng này cho thấy các tính chất nhiệt lý của dung dịch canxi clorua CaCl 2 phụ thuộc vào nhiệt độ và nồng độ muối: nhiệt dung riêng của dung dịch, độ dẫn nhiệt, độ nhớt của dung dịch nước, độ khuếch tán nhiệt của chúng và số Prandtl. Nồng độ% của muối CaCl 2 trong dung dịch từ 9,4 - 29,9%. Nhiệt độ tại đó các thuộc tính được xác định bởi hàm lượng muối của dung dịch và nằm trong khoảng từ -55 đến 20 ° C.
clorua canxi CaCl 2 có thể không đóng băng lên đến âm 55 ° С
. Để đạt được hiệu ứng này, nồng độ của muối trong dung dịch phải là 29,9% và khối lượng riêng của nó là 1286 kg / m3.
Với sự gia tăng nồng độ muối trong dung dịch, không chỉ tỷ trọng của nó tăng lên mà còn các đặc tính nhiệt lý như độ nhớt động lực học của dung dịch nước, cũng như số Prandtl. Ví dụ, độ nhớt động lực của dung dịch CaCl 2
với nồng độ muối 9,4% ở nhiệt độ 20 ° C là 0,001236 Pa s, và khi tăng nồng độ canxi clorua trong dung dịch lên 30% thì độ nhớt động lực của nó tăng đến giá trị 0,003511 Pa s.
Cần lưu ý rằng nhiệt độ có ảnh hưởng mạnh nhất đến độ nhớt của dung dịch nước muối này. Khi dung dịch canxi clorua được làm lạnh từ 20 đến -55 ° C, độ nhớt động lực của nó có thể tăng lên 18 lần và động học gấp 25 lần.
Đưa ra những điều sau đây tính chất nhiệt lý của dung dịch CaCl 2
:
- , kg / m 3;
- điểm đóng băng ° С;
- độ nhớt động lực học của dung dịch nước, Pa s;
- Số Prandtl.
ÑÐ ° ÑÑоР»ÑемпеÑÐ ° ÑÑÑÐ °
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ · α α ð ð ð ð ð ð ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ ñ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð đồng Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nữa Ð. Ð nữa Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ð nay Ð Ð Ð Nhà Ð Nhà Ð tháng, Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ ðộ ð- ÑиÑÑÑ. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Nhà Ð doanh Ð doanh Ð. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð giờ Ðộ ñññ Ð- Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðơn Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðơn Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ð doanh Ð doanh Ðài »Ð ²ÐÐРооо²²²²²² Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ² Ð ²Ð Ð Ð ² DND »D ÑоÐ'ÐμÑжР° ниÐμ Ñол D в NĐ ° ÑÑоР»Ðμ мÐμнÑÑÐμ, ÑÐμм ÑÑÐμÐ ± ÑÐμмоÐμ Ð'л Ñ ÑвÑÐμкÑиÑÐμÑкого NĐ ° ÑÑвоÑÐ °, воÐ'Ð ° ÑÑкоÑÐ¸Ñ Ð¾Ð ± ÑÐ ° Ð · овР° ние кÑиÑÐ ° Ð »Ð» ов Ð »ÑдР° пÑи оÑл Ð ° жденÑÑÐ ° иР»Ð´Ð ° пÑÐ ¸ оÑÐ »Ð ° жденÑÑÐ ° иоиии Chạy ñðμμððμð½ððμÐμРо Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nó Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nữa Ð nữa Ð Ð nữa Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nữa Ð nữa Ð. еÑонÑенÑÑÐ ° ÑÐ¸Ñ Ñоии оÐÑÐ ° Ð »Ñном ÑÐ ° ÑÑвое.Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð thời Ð tỷ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð được Ð. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ° Ð
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð thời Ð tỷ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð được Ð. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð đang Ðang Ðang Ðộ Ðộ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Mẫu Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð năm Ð năm Ð. Ð Ð Ð Ð Ð μñ DD ° мÐμÑÐ · Ð ° ниÐμ ÑвÑÐμкÑиÑÐμÑкого NĐ ° ÑÑвоÑÐ ° á ÑÑо пÑоÑÐμÑÑ Ñ NND ° ÑÑиÐμм ÑкÑÑÑой ÑÐμпР»Ð¾ÑÑ, поÑÑÐ¾Ð¼Ñ ÑÐμмпÐμÑÐ ° ÑÑÑÐ ° оÑÑÐ ° ÐμÑÑÑ Ð½ÐμиР· менной. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð tức Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð tức Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð tức Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð điều Ð Ð nữa Ð Ð Ð Ð Ð Ð Ð ² Ð ¿Ñипонижении Ð · ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ñ nh ð ð ð ð ð ð ð ð ð ð ñ ñ nh ð ð ð ð ð ð ð ð ð ð ð ð ð ñ nh ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ñ nh ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ð năm Ð. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Mẫu Ð tỷ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðảng Ðảng Ð. Ð Ð Ð Ð Ð Ð ° ¸ поÑоÑнной ÐÐ ° нн Ðй пÐоÐÐμÑÑ ÐÑимÐμнÐμÑÑÑ ² пР»Ð ° ÑÑинÑÐ ° ÑÑÑÑÑ ÑA Ñ ÑA ÑA ÑA ÑA Ñ .
Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ðộ Ðộ Ð Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ð? ¸Ñ и ÑÐ »Ð¾ÑидР° нР° ÑÑиÑ. Ð ° ÑÐÐ²Ð¾Ñ ÑÐ »Ð¾ÐиÐ'Ð ° кР° л ÑÑÐ¸Ñ Ð¿ÑÐμжÐ'Ðμ вÑÐμго оÐпоР»ÑÐ · ÑÐμÑÑÑ ÑAÑÑÐÑ ÑAÑ ÑO ¸ Ð · Ð ° моР° живР° нии пÑодÑкÑов, ÑÑÐ ° нении и Ñ.д. 17,8  ° С. Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð ngủ Ð năm Ð. ((( Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð 55 ° C Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Nhà Ð doanh Ð doanh Ð. (( Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð giờ Ð giờ Ð-Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay!! Ð (μ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð rao Ð năm Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ð nay '' Ð Ð Ð Ð Ð Ð Ð Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ðộ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð Ðảng Ð giờ Ðảng Ðồ Ðồ Ð. ° ÐºÑ ÑÐ ° ÑÑооР° ÑоÑÐ »Ð ° ждР° емÑм пÑодÑкÑом.
Ð ° ÑÐÐ²Ð¾Ñ ÑÐ »Ð¾ÐиÐ'Ð ° нР° ÑÑÐ¸Ñ (пиÑÐμвой Ñол и) нÐμ поÐÑÐ¸Ñ ÐиÑÐμвÑÐμ пÑоÐ'ÑкÑÑ. ¾¾ððð ° ° ðñððð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð đơn Ð đơn Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð năm năm Ð ((Ð dự Ðang Ðang Ðang) Ð ° Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð nay Ð Ð Ð Ð Ð Ð nay · иÑеР»Ñно в21. 1  ° С. Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð giờ Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Ð Nhà Ð đơn Ð doanh Ð. (( Ð ·
Nước biển có thể đóng băng ở nhiệt độ nào?
Nhưng câu hỏi chính vẫn chưa được trả lời. Chúng ta đã biết rằng muối làm chậm quá trình đóng băng của nước, biển sẽ được bao phủ bởi một lớp băng không phải ở nhiệt độ không mà ở nhiệt độ dưới 0. Nhưng các chỉ số nhiệt kế phải đến âm bao nhiêu để người dân vùng ven biển không nghe thấy tiếng sóng biển thường thấy khi họ rời khỏi nhà?
Để xác định giá trị này, có một công thức đặc biệt, phức tạp và chỉ có thể hiểu được đối với các bác sĩ chuyên khoa. Nó phụ thuộc vào chỉ số chính - độ mặn
. Nhưng vì chúng ta có giá trị trung bình cho chỉ số này, chúng ta cũng có thể tìm thấy điểm đóng băng trung bình không? Ồ chắc chắn rồi.
Nếu bạn không cần tính toán mọi thứ lên đến hàng trăm, cho một khu vực cụ thể, nhớ nhiệt độ ở -1,91 độ
.
Có vẻ như sự khác biệt không quá lớn, chỉ có hai độ. Nhưng trong những biến động nhiệt độ theo mùa, điều này có thể đóng một vai trò to lớn khi nhiệt kế rơi xuống ít nhất là 0. Nó sẽ chỉ mát hơn 2 độ, những người dân ở cùng châu Phi hoặc Nam Mỹ có thể nhìn thấy băng gần bờ biển, nhưng than ôi. Tuy nhiên, chúng tôi không nghĩ rằng họ rất khó chịu trước sự mất mát như vậy.
Tính chất nhiệt lý của dung dịch NaCl
Bảng cho biết các tính chất nhiệt lý của dung dịch natri clorua NaCl phụ thuộc vào nhiệt độ và nồng độ muối. Nồng độ của natri clorua NaCl trong dung dịch từ 7 đến 23,1%. Cần lưu ý rằng khi làm lạnh dung dịch nước natri clorua, nhiệt dung riêng của nó thay đổi một chút, độ dẫn nhiệt giảm và độ nhớt của dung dịch tăng lên.
Đưa ra những điều sau đây tính chất nhiệt lý của dung dịch NaCl
:
- tỷ trọng dung dịch, kg / m 3;
- điểm đóng băng ° С;
- nhiệt dung (khối lượng) riêng, kJ / (kg deg);
- hệ số dẫn nhiệt, W / (m deg);
- độ nhớt động lực học của dung dịch, Pa s;
- độ nhớt động học của dung dịch, m 2 / s;
- độ khuếch tán nhiệt, m 2 / s;
- Số Prandtl.
Nước biển được làm bằng gì?
Nội dung của biển khác với nước ngọt như thế nào? Sự khác biệt không quá lớn, nhưng vẫn:
- Nhiều muối hơn.
- Các muối magie và natri chiếm ưu thế.
- Mật độ khác nhau một chút, trong vòng một vài phần trăm.
- Hydro sunfua có thể hình thành ở độ sâu.
Thành phần chính của nước biển, dù nghe có thể đoán trước được như thế nào, là nước. Nhưng không giống như nước sông và hồ, nó chứa một lượng lớn natri và magie clorua
.
Độ mặn được ước tính là 3,5 ppm, nhưng để làm cho nó rõ ràng hơn - ở mức 3,5 phần nghìn của tổng số thành phần.
Và ngay cả con số này, không phải là con số ấn tượng nhất, cung cấp nước không chỉ với một hương vị cụ thể, mà còn khiến nó không thể uống được. Không có chống chỉ định tuyệt đối, nước biển không phải là chất độc hay chất độc hại, và không có gì xấu sẽ xảy ra từ một vài ngụm. Sẽ có thể nói về hậu quả nếu một người ở ít nhất suốt cả ngày. Ngoài ra, thành phần của nước biển bao gồm:
- Flo.
- Nước brom.
- Chất vôi.
- Kali.
- Clo.
- các muối sunfat.
- Vàng.
Đúng, tính theo tỷ lệ phần trăm, tất cả các nguyên tố này đều nhỏ hơn nhiều so với muối.
Các tiểu bang và các loại nước
Nước trên hành tinh Trái đất có thể có ba trạng thái tập hợp chính: lỏng, rắn và khí, có thể biến đổi thành các dạng khác nhau đồng thời tồn tại với nhau (tảng băng trôi trong nước biển, hơi nước và tinh thể băng trong các đám mây trên bầu trời, sông băng và tự do -các sông chảy).
Tùy thuộc vào đặc điểm của nguồn gốc, mục đích và thành phần, nước có thể là:
- tươi;
- khoáng sản;
- hải lý;
- uống (ở đây chúng tôi bao gồm nước máy);
- cơn mưa;
- rã đông;
- nước lợ;
- có cấu trúc;
- chưng cất;
- khử ion.
Sự hiện diện của các đồng vị hydro làm cho nước:
- nhẹ;
- nặng (đơteri);
- siêu lượn sóng (tritium).
Chúng ta đều biết rằng nước có thể mềm và cứng: chỉ số này được xác định bởi hàm lượng của các cation magiê và canxi.
Mỗi loại và trạng thái tổng hợp của nước mà chúng tôi đã liệt kê có điểm đóng băng và điểm nóng chảy riêng.
Video nước muối đóng băng

 Bạn biết gì về nhiệt độ sôi của nước?
Bạn biết gì về nhiệt độ sôi của nước?

Chế độ nhiệt độ xác định trước hết là tốc độ của quá trình cấp đông.
Nhiệt độ trong khoảng giá trị âm và dương ảnh hưởng đến tốc độ phản ứng, độ hòa tan của các hợp chất, tốc độ hòa tan, sự đông tụ, cũng như nồng độ của các cặp ion không phân ly. Có một số loại nhiệt độ trong dung dịch: cấu trúc, điểm đóng băng. Nhiệt độ bắt đầu kết tinh (điểm đóng băng) - nhiệt độ mà tại đó, do làm lạnh dung dịch, sự hình thành các tinh thể bắt đầu. Độ trầm cảm của điểm đóng băng ΔТз là hiệu số giữa điểm đóng băng của dung môi nguyên chất và dung dịch. Điểm đóng băng của nước muối luôn thấp hơn điểm đóng băng của nước tinh khiết và phụ thuộc vào nồng độ của muối hòa tan. Sự phụ thuộc này đối với nước muối có thể được biểu thị bằng phương trình:
ở đâu ĐẾN
- hệ số tương xứng; VỚI
là nồng độ của chất tan trong dung dịch.
Trong các dung dịch ít loãng hơn, nhiệt độ bắt đầu kết tinh được xác định từ giản đồ trạng thái của hệ tương ứng. Vì nhiệt độ đóng băng của nước biển và nước muối tự nhiên có khoáng chất cao sẽ khác nhau, chúng tôi giả định rằng nhiệt độ này nên được tính toán bằng các công thức khác nhau.
Chúng tôi đã thực hiện gần đúng dữ liệu thực nghiệm về điểm đóng băng của dung dịch muối ăn, nước biển và nước muối tự nhiên được sử dụng trong công việc. Sự phụ thuộc của sự thay đổi nhiệt độ đông đặc trong các dạng đồ thị và phân tích được trình bày trong Hình 41-43.
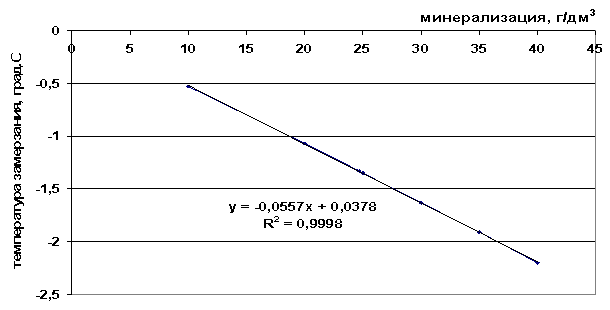
Cơm. 41. Sự phụ thuộc của điểm đóng băng vào độ mặn của dung dịch muối
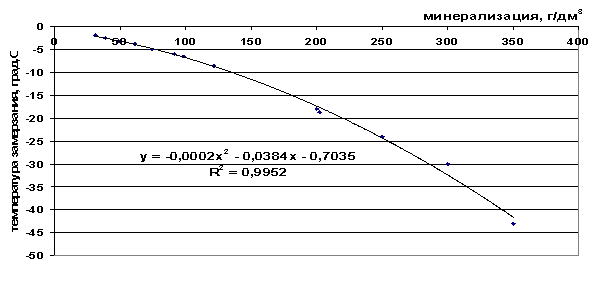
Cơm. 42. Sự phụ thuộc của điểm đóng băng của nước biển vào độ mặn
Cơm. 43. Sự phụ thuộc của điểm đóng băng của nước muối vào độ mặn
Từ các giá trị điểm đóng băng được trình bày (Bảng 9), có thể thấy rằng điểm đóng băng giảm khi tổng độ mặn của dung dịch tăng lên và khi số lượng các thành phần trong hệ thống đông lạnh tăng lên - ΔТз (NaCl)
Bảng 9. Phân tích các phụ thuộc đồ họa đã xây dựng
|
Ctot, g / dm 3 |
Điểm đóng băng, ° С |
||
|
Dung dịch NaCl |
nước biển |
||
|
t = 8 ∙ 10 -5 M 2 -0,0945M + 1,0595, |
0,0557M + 0,0378, |
t = -2 ∙ 10 -4 M 2 -0.0384M-0.7035, |
|
*
R 2 - độ tin cậy của phép gần đúng
Được biết, sự đóng băng của các muối riêng lẻ từ nước khử muối xảy ra ở các nhiệt độ khác nhau, ví dụ, ở nhiệt độ -2 ° C, canxi cacbonat kết tủa. Ở - 3,5 ° C natri sulfat. Khi nhiệt độ giảm xuống -20 ° C, muối ăn kết tủa, đến -25,5-26 ° C magie clorua, và ở nhiệt độ rất thấp - 40-55 ° C, kali và canxi clorua kết tủa. Đối với nhiệt độ âm, quá trình hình thành các hyđrat tinh thể, không ổn định ở nhiệt độ dưới 0 ° C, là đặc trưng. Ví dụ, hydrohalit NaCl * 2H 2 O được tạo thành ở -0,15 ° C, MgCl 2 * 12H 2 O ổn định ở -15 ° C và MgCl 2 * 8H 2 O dưới 0 ° C, Na 2 CO 3 * 7H 2 O chỉ được tạo thành ở -10 ° C. KCl kết tinh ở 0 ° С dưới dạng KCl, ở -6,6 ° С đã có hai pha cùng tồn tại - KCl và KCl * H 2 O, ở -10,6 ° С chỉ có KCl * H 2 O. Ở nhiệt độ âm, các hyđrat kết tinh riêng lẻ với số lượng phân tử nước kết tinh tối đa có thể, theo các số phối trí ở một giá trị nhất định, và hỗn hợp của chúng (nhưng không phải là hỗn hợp tinh thể). Cần lưu ý sự giảm bất thường về điểm đông đặc của các dung dịch đậm đặc.
Chúng tôi mang đến cho bạn sự chú ý của các tạp chí do nhà xuất bản "Học viện Lịch sử Tự nhiên" xuất bản
Nước đóng băng ở nhiệt độ nào? Có vẻ như - câu hỏi đơn giản nhất mà ngay cả một đứa trẻ cũng có thể trả lời: điểm đóng băng của nước ở áp suất khí quyển bình thường là 760 mmHg là 0 độ C.
Tuy nhiên, nước (mặc dù phân bố cực kỳ rộng trên hành tinh của chúng ta) là chất bí ẩn nhất và chưa được hiểu đầy đủ, vì vậy câu trả lời cho câu hỏi này cần một cuộc thảo luận chi tiết và hợp lý.
- Ở Nga và Châu Âu, nhiệt độ được đo trên thang độ C, giá trị cao nhất trong đó là 100 độ.
- Nhà khoa học Mỹ Fahrenheit đã phát triển quy mô của riêng mình với 180 bộ phận.
- Có một đơn vị đo nhiệt độ khác - kelvin, được đặt theo tên của nhà vật lý người Anh Thomson, người đã nhận được tước hiệu là Lord Kelvin.
Tại sao bạn không nên uống nước biển
Chúng tôi đã đề cập ngắn gọn về chủ đề này, chúng ta hãy xem xét nó chi tiết hơn một chút. Cùng với nước biển, hai ion đi vào cơ thể - magiê và natri.
|
Natri |
Magiê |
|
Tham gia vào việc duy trì sự cân bằng nước-muối, một trong những ion chính cùng với kali. |
Tác dụng chính trên hệ thần kinh trung ương. |
|
Với sự gia tăng về số lượng Na |
Đào thải rất chậm ra khỏi cơ thể. |
|
Tất cả các quá trình sinh học và sinh hóa đều bị xáo trộn. |
Cơ thể dư thừa sẽ dẫn đến tiêu chảy, làm trầm trọng thêm tình trạng mất nước. |
|
Thận của con người không có khả năng đối phó với quá nhiều muối trong cơ thể. |
Có lẽ sự phát triển của rối loạn thần kinh, thể trạng không đủ. |
Không thể nói rằng một người không cần tất cả những chất này, nhưng nhu cầu luôn phù hợp trong những giới hạn nhất định. Sau khi uống một vài lít nước như vậy, bạn sẽ đi quá xa giới hạn của chúng.
Tuy nhiên, ngày nay nhu cầu cấp thiết về việc sử dụng nước biển có thể chỉ nảy sinh ở những nạn nhân của vụ đắm tàu.