Devo mettere a terra lo scaldasalviette
Per prima cosa devi sapere che la messa a terra (la costruzione di anelli di terra con le tue mani) non è richiesta se:
- 1. Stai utilizzando uno scaldasalviette elettrico (tali scaldasalviette sono generalmente dotati di spine speciali in cui è presente un filo di terra, tutto questo è collegato a una presa e le prese stesse devono essere già collegate al circuito di terra) .
- 2. Vivi in una casa o in un appartamento privato e hai un sistema di riscaldamento separato.
La messa a terra del termoarredo è obbligatoria nei seguenti casi:
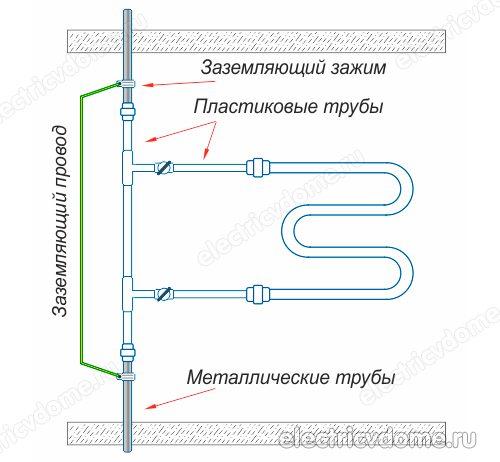
- 1. Se l'asciugatrice è collegata all'impianto di riscaldamento con un tubo di plastica. All'interno del tubo metallo-plastica è presente l'alluminio, che conduce corrente elettrica: alle giunzioni in cui si trovano i raccordi, il circuito elettrico è interrotto. Di conseguenza, un tale scaldasalviette deve essere collegato al circuito di terra o al montante dell'acqua calda.
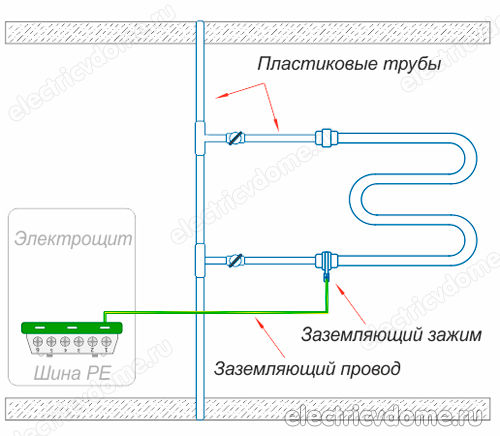
- 2. Se l'impianto dell'acqua calda è costituito da tubi di plastica.
Come mettere a terra uno scaldasalviette
Tutti gli scaldasalviette elettrici, come accennato in precedenza, sono collegati a una presa con messa a terra, mentre tali essiccatori hanno un filo di terra con un contatto separato sulla spina. Poiché i termoarredo sono solitamente installati nel bagno, è necessario ispezionare la presa a cui sarà collegato. Tale uscita deve trovarsi in una speciale custodia protettiva che impedisca all'umidità di entrare nella presa stessa.
Esistono 2 modi principali per mettere a terra uno scaldasalviette:
- 1. Mediante un sistema di equalizzazione del potenziale, che deve essere installato a mano, mettere a terra tale sistema alla massa comune del quadro elettrico. Questo dovrebbe essere fatto se vengono utilizzate comunicazioni fatte di polimeri (tubi di metallo-plastica) invece di comunicazioni metalliche in una casa o in un appartamento.
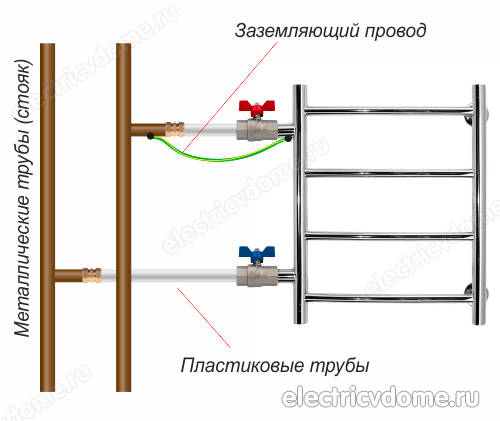
- 2. Collegare a terra direttamente il tubo del corpo dello scaldasalviette con un filo convenzionale ad un montante in acciaio.
Per implementare la messa a terra del termoarredo nel secondo modo, è necessario prima procurarsi un morsetto, dopo aver rimosso tutti i materiali isolanti da esso. Questo morsetto deve avere un terminale per il collegamento del filo. Quindi il morsetto viene fissato al tubo del corpo del termoarredo.
Viene preso un normale filo di rame, che dovrebbe avere una sezione trasversale di 4 mm2. Questo filo è collegato da un lato al morsetto a morsetto, l'altra estremità deve essere collegata o alla massa del quadro elettrico o ad un montante in acciaio. Inoltre, non dimenticare di collegare altri dispositivi nel tuo bagno al circuito di terra.
| Tali metodi non richiedono molto tempo per la loro implementazione, ma in cambio ottengono un funzionamento lungo e ininterrotto del termoarredo e in futuro la domanda "come mettere a terra il termoarredo" non causerà difficoltà. |
Gli amici guardano anche il video per ciò di cui hai bisogno per mettere a terra lo scaldasalviette.
Contenuti correlati sul sito:
- Sulla messa a terra in parole semplici
- Perché il bagno è a terra?
- Il design del dispositivo di messa a terra
Cause di elettrocorrosione
La comparsa delle correnti parassite di Foucault è un fenomeno piuttosto complesso e imprevedibile. Nei sistemi di approvvigionamento di acqua calda, e talvolta nel sistema di riscaldamento, tali correnti compaiono per molte ragioni che sembrano non essere correlate.
In generale, le correnti parassite si formano con una differenza di potenziale. Quando si costruisce una casa, tutte le strutture metalliche sono collegate a un circuito di terra comune e in precedenza nella costruzione utilizzavano la messa a terra lungo il circuito, ma ora si accontentano del metodo di equalizzazione del potenziale.
Quando i sistemi di plastica sono installati in un appartamento invece del sistema metallico esistente, la differenza di potenziale sorge a causa di un'interruzione del terreno (ad esempio, esiste un potenziale su uno scaldasalviette e uno completamente diverso su un montante). Da qui la differenza di potenziale, quindi le correnti vaganti. Possono verificarsi anche a causa di un cortocircuito, della mancanza di messa a terra degli elettrodomestici vicini, che si tratti di una lavatrice e così via.
Anche la presenza/assenza di binari del tram nelle immediate vicinanze gioca un ruolo. Le correnti vaganti si verificano anche quando si verifica una violazione dell'isolamento del cablaggio elettrico, un'interruzione della rete o una messa a terra dell'impianto di riscaldamento.
Tutto ciò porta alla corrosione elettrica degli impianti idraulici, inoltre è causata dalla vicinanza di due diversi materiali, in particolare inox e acciaio nero. Di conseguenza, il luogo attraverso il quale la carica passa nello scaldasalviette subisce una reazione elettrochimica, quindi lì si verificano danni. Tali problemi vengono solitamente risolti collegando direttamente a terra lo scaldasalviette stesso.
Quando si acquista uno scaldasalviette ad acqua, è necessario familiarizzare con le regole per il suo funzionamento, in particolare prestare attenzione se è necessario collegare a terra lo scaldasalviette o meno, per tener conto di questo punto durante il riparazione e non dopo che la riparazione è stata completata
Perché mettere a terra un portasciugamani riscaldato ad acqua
Dopo che i tubi di plastica hanno iniziato a sostituire quelli ordinari di metallo, hanno iniziato a ignorare la loro messa a terra, credendo erroneamente che un tubo di metallo e un tubo di metallo-plastica abbiano la stessa conduttività elettrica. Questo non è vero. Non c'è contatto tra il tubo metallo-plastica e l'alluminio: non sono collegati.
La pratica mostra che il 90 percento dei termoarredo inizia a perdere proprio nel caso di sostituzione dei sistemi di acqua calda in metallo con le loro controparti in plastica (ad esempio, polipropilene). I vecchi tubi di metallo vengono sostituiti con moderni tubi di plastica per ridurre le correnti parassite. Tuttavia, la corrosione continua a manifestarsi.
I primi sintomi di corrosione elettrica sono la comparsa di macchie di ruggine sullo scaldasalviette e la ruggine compare anche su dispositivi in acciaio inossidabile. In generale, tutti i prodotti elettrici in metallo a contatto con l'acqua sono soggetti a corrosione sia elettrochimica che galvanica. L'elettrocorrosione si verifica in presenza di correnti vaganti. Di conseguenza, il metallo viene contemporaneamente esposto alla corrente elettrica e all'acqua, dopodiché compaiono rotture del metallo e la corrosione inizia a diffondersi da lì.
Quando due metalli diversi entrano in contatto, uno dei quali è più reattivo dell'altro, entrambi i metalli entrano in una reazione chimica. L'acqua pura è un pessimo conduttore di corrente elettrica (dielettrico), ma a causa dell'elevata concentrazione di varie impurità, l'acqua si trasforma in una specie di elettrolita.
Non dimenticare che la temperatura ha una grande influenza sulla conducibilità elettrica: maggiore è la temperatura dell'acqua, migliore è la conduzione elettrica. Questo fenomeno è noto come "corrosione galvanica", è lei che metodicamente rende inutilizzabile lo scaldasalviette.
La necessità di una protezione anticorrosione
Proteggere il metallo dalle influenze che hanno un effetto distruttivo sulla sua superficie è uno dei compiti principali che devono affrontare coloro che lavorano con meccanismi, unità e macchine, navi e processi di costruzione.

Più attivamente viene utilizzato un dispositivo o una parte, più è probabile che venga esposto agli effetti distruttivi delle condizioni atmosferiche, ai liquidi che si incontrano durante il funzionamento.Molti rami della scienza e della produzione industriale stanno lavorando per proteggere il metallo dalla corrosione, ma i metodi principali rimangono invariati e consistono nella creazione di rivestimenti protettivi:
- metallo;
- non metallico;
- chimico.
I rivestimenti non metallici sono creati utilizzando composti organici e inorganici, il loro principio di funzionamento è abbastanza efficace e differisce da altri tipi di protezione. Per creare una protezione non metallica nella produzione industriale ed edile, vengono utilizzate pitture e vernici, calcestruzzo e bitume e composti ad alto peso molecolare, che sono stati adottati in modo particolarmente attivo negli ultimi anni, quando la chimica dei polimeri ha raggiunto grandi vette.

La chimica ha contribuito alla creazione di rivestimenti protettivi con metodi:
- ossidazione (creazione di un film protettivo sul metallo mediante film di ossido);
- fosfatazione (film di fosfato);
- nitrurazione (saturazione della superficie dell'acciaio con azoto);
- cementazione (composti con carbonio);
- bluing (composti con sostanze organiche);
- modificare la composizione del metallo introducendo additivi anticorrosivi);
- modifica dell'ambiente corrosivo circostante mediante l'introduzione di inibitori che lo influiscono.
La protezione dalla corrosione elettrochimica è il processo inverso della corrosione elettrochimica. A seconda dello spostamento del potenziale del metallo verso il lato positivo o negativo, ci sono protezione anodica e catodica. Collegando un protettore o una fonte di corrente continua a un prodotto metallico, si crea una polarizzazione catodica sulla superficie del metallo, che impedisce la distruzione del metallo attraverso l'anodo.
I metodi di protezione elettrochimica consistono in due opzioni:
- il rivestimento metallico è protetto da un altro metallo, che ha un potenziale più negativo (cioè il metallo di protezione è meno stabile di quello da proteggere), e questo si chiama anodizzazione;
- il rivestimento viene applicato da un metallo meno attivo, quindi è ed è chiamato catodico.

La protezione dalla corrosione anodica è, ad esempio, il ferro zincato. Fino a quando tutto lo zinco dello strato protettivo non sarà esaurito, il ferro sarà relativamente sicuro.
La protezione catodica è la nichelatura o la placcatura in rame. In questo caso, la distruzione dello strato protettivo porta alla distruzione dello strato che protegge. Attaccare un protettore per proteggere un prodotto in metallo non è diverso dalla reazione in altri casi. Il protettore funge da anodo e ciò che è sotto il suo protettorato rimane intatto, utilizzando le condizioni create per esso.
Cos'è la corrosione
Il processo di distruzione dello strato superiore di un materiale metallico sotto l'influenza di influenze esterne è chiamato corrosione in senso lato.

Il termine corrosione in questo caso è solo una caratteristica del fatto che la superficie del metallo entra in una reazione chimica e perde le sue proprietà originali sotto la sua influenza.
4 segni principali con cui puoi determinare che questo processo esiste:
- un processo che si sviluppa in superficie ed eventualmente penetra nel manufatto metallico;
- la reazione nasce spontanea dal fatto che la stabilità dell'equilibrio termodinamico tra l'ambiente ed il sistema degli atomi nella lega o nel monolite è disturbata;
- la chimica percepisce questo processo non semplicemente come una reazione di distruzione, ma come una reazione di riduzione e ossidazione: entrando in una reazione, alcuni atomi ne sostituiscono altri;
- le proprietà e le caratteristiche del metallo durante tale reazione subiscono cambiamenti significativi o si perdono dove si verifica.
Metodi di protezione dei metalli
La corrosione elettrochimica è uno dei principali ostacoli incontrati nel modo di attività umana. La protezione dall'impatto dei processi distruttivi e dal loro flusso sulla superficie di strutture e strutture è uno dei compiti permanenti e urgenti di qualsiasi produzione industriale e di qualsiasi attività domestica di una persona.

Sono stati sviluppati diversi metodi di tale protezione e tutti vengono utilizzati attivamente nel ciclo di vita quotidiano:
- Protezione elettrochimica - elettrolitica secondo il principio di funzionamento, l'uso di leggi chimiche, protegge il metallo utilizzando il principio dell'anodo, del catodo e del battistrada.
- Elaborazione di elettroscintille utilizzando varie installazioni: senza contatto, a contatto, anodico-meccaniche.
- La spruzzatura ad arco elettrico è il principale vantaggio nello spessore dello strato applicato e nella relativa economicità del processo.
- Un efficace trattamento anticorrosivo consiste nella rimozione dei contaminanti e nella pulizia della superficie trattata, seguita dall'applicazione di un anticorrosivo e quindi di un ulteriore strato protettivo sulla superficie.
Tutti questi metodi sono stati sviluppati nel processo dell'attività umana al fine di proteggere strumenti, veicoli e trasporti all'incrocio di diversi settori industriali e utilizzando risultati scientifici.
La corrosione elettrochimica, che è un processo naturale di distruzione della superficie metallica sotto l'influenza di fattori ambientali neutri o aggressivi, è un problema complesso. Le imprese di costruzione di macchine, trasporti e industriali, i veicoli ne subiscono perdite. E questo è un problema che richiede una risoluzione quotidiana.
Tipi di corrosione
A seconda del tipo di metallo e della reazione redox che si verifica con esso, la corrosione può essere:
- uniforme o irregolare;
- local e point (alcune sezioni per qualche motivo hanno reagito, mentre altre no);
- ulcerativo, noto anche come pitting;
- sottosuperficie;
- screpolature;
- intercristallino, che sorge lungo i confini del cristallo di metallo.
Inoltre, a seconda del tipo di fattori esterni che influenzano la superficie, la corrosione può essere chimica ed elettrochimica. La corrosione chimica si verifica a seguito di alcune reazioni sotto l'influenza di interazioni chimiche, ma senza la partecipazione della corrente elettrica, e può anche essere inerente al petrolio e al gas. L'elettrochimica si distingue per alcuni processi, è più complessa della chimica.

Nel video: corrosione dei metalli.
Cause e segni di corrosione elettrochimica
La corrosione elettrochimica differisce dalla corrosione chimica in quanto il processo di distruzione avviene nel sistema elettrolitico, che provoca la formazione di una corrente elettrica all'interno di questo sistema. Due processi coniugati, anodico e catodico, portano alla rimozione di atomi instabili dal reticolo cristallino del metallo. Durante il processo anodico, gli ioni vanno in soluzione e gli elettroni del processo anodico cadono in una trappola per una sostanza ossidante e sono legati da un depolarizzatore.
Pertanto, la depolarizzazione è la rimozione di elettroni liberi dai siti catodici e il depolarizzatore è la sostanza responsabile di questo processo. Le reazioni principali si verificano con la partecipazione di idrogeno e ossigeno come depolarizzatori.
Esistono molti esempi di corrosione elettrochimica di vario tipo, che colpisce le superfici metalliche in natura e sotto l'influenza di varie condizioni. L'idrogeno funziona in un ambiente acido, mentre l'ossigeno lavora in uno neutro.
Quasi tutti i metalli subiscono corrosione elettrochimica e su questa base sono divisi in 4 gruppi, viene determinato il valore del loro potenziale elettrodo:
- quelli attivi si corrodono anche in un ambiente dove non sono presenti agenti ossidanti;
- il medio-attivo entra in una reazione di ossidazione in un ambiente acido;
- quelli inattivi non reagiscono in assenza di agenti ossidanti sia in ambiente neutro che acido;
- non reagire - elevata stabilità (metalli nobili, palladio, oro, platino, iridio).
Ma la stessa reazione può avvenire anche in acqua, in soluzioni di basi, sali e acidi. Nella differenza altamente specializzata in corrosione atmosferica, suolo e aerazione, si distinguono marini e biologici (che si verificano sotto l'influenza di batteri).
C'è anche corrosione elettrica, che si verifica sotto l'influenza della corrente elettrica, ed è il risultato di correnti vaganti che si verificano quando la corrente elettrica viene utilizzata da una persona per svolgere determinate attività.
In questo caso, la superficie metallica omogenea viene distrutta a causa dell'instabilità termodinamica dell'ambiente. Ed eterogeneo - a causa della composizione del reticolo cristallino, in cui gli atomi di un metallo sono tenuti più stretti degli atomi di inclusioni estranee.Queste reazioni differiscono nella velocità di ionizzazione degli ioni e nella riduzione dei componenti ossidativi dell'ambiente.
La distruzione delle superfici metalliche durante la corrosione elettrochimica consiste nel verificarsi simultaneo di due processi: anodico e catodico, e la differenza tra i processi è che la dissoluzione avviene agli anodi, che sono a contatto con l'ambiente attraverso molti microelettrodi che fanno parte di la superficie di qualsiasi metallo e sono chiuso a me stesso.