YÊU CẦU
1. Phương pháp hóa lỏng trực tiếp than, bao gồm các giai đoạn sau:
(1) điều chế bùn than từ than thô và chất xúc tác;
(2) trộn bùn than với hydro và xử lý trước hỗn hợp, sau đó cung cấp cho hệ thống phản ứng để thực hiện phản ứng hóa lỏng;
(3) tách các sản phẩm phản ứng được rút khỏi bình phản ứng trong thiết bị phân tách (9, 10) để tạo thành pha lỏng và pha khí, trong đó pha lỏng được chưng cất phân đoạn trong cột chưng cất (11) ở áp suất khí quyển để thu được sản phẩm dưới dạng một phần nhiên liệu điêzen và một sản phẩm còn lại;
(4) đưa sản phẩm còn lại thu được trong cột áp suất khí quyển vào cột chưng cất chân không (12) để tách thành dịch cất và cặn;
(5) trộn phần nhiên liệu điêzen và phần chưng cất để tạo thành hỗn hợp, sau đó đưa hỗn hợp vào lò phản ứng xử lý nước tầng sôi tuần hoàn cưỡng bức (13) để thực hiện quá trình hydro hóa;
(6) phân đoạn các sản phẩm hydro hóa thành các sản phẩm dầu và dung môi cho hydro được tái chế đến giai đoạn (1).
2. Phương pháp theo điểm 1, trong đó giai đoạn (1) bao gồm các thao tác sau:
(a) chuyển than thô thành bột than với cỡ hạt nhất định sau khi làm khô và nghiền than thô trong thiết bị tiền xử lý; (b) xử lý nguyên liệu nạp xúc tác (3) và bột than trong thiết bị chuẩn bị chất xúc tác (4) để thu được bột xúc tác hóa lỏng than siêu mịn; (c) trộn trong thiết bị (5) để điều chế bùn của chất xúc tác hóa lỏng than và bột than với dung môi cho hydro (16) để tạo thành bùn than.
3. Phương pháp theo điểm 1, trong đó bước phản ứng hóa lỏng than bao gồm các bước sau:
(a) nạp bùn than sau khi trộn với hydro (6) và nung nóng sơ bộ vào lò phản ứng tầng sôi thứ nhất (7) với tuần hoàn cưỡng bức để thực hiện phản ứng hóa lỏng để thu được các sản phẩm phản ứng rời lò phản ứng; (b) đưa các sản phẩm phản ứng rời lò phản ứng tầng sôi thứ nhất (7), sau khi trộn chúng với hydro, đến thiết bị phản ứng tầng sôi thứ hai (8) với tuần hoàn cưỡng bức để tiếp tục phản ứng hóa lỏng, các lò phản ứng tầng sôi hoạt động ở phản ứng sau điều kiện: nhiệt độ phản ứng 430-465 ° C; áp suất phản ứng 15-19 MPa; tỷ lệ giữa lượng khí và chất lỏng 600-1000 nl / kg; tốc độ thể tích huyền phù than 0,7-1,0 t / m3 h; mức độ thêm chất xúc tác Fe / than khô = 0,5-1,0 trọng lượng.%.
4. Phương pháp theo điểm 1, trong đó giai đoạn (3) bao gồm các thao tác sau:
(a) đưa dòng sản phẩm phản ứng vào thiết bị tách nhiệt độ cao (9) để tách thành pha khí và pha lỏng, trong khi nhiệt độ trong thiết bị tách nhiệt độ cao được duy trì ở 420 ° C;
(b) đưa pha khí từ bộ tách nhiệt độ cao (9) sang bộ tách nhiệt độ thấp (10) để tách tiếp thành khí và lỏng, trong khi nhiệt độ trong bộ tách nhiệt độ thấp được duy trì ở nhiệt độ phòng.
5. Phương pháp theo điểm 2, trong đó -FeOOH được sử dụng làm chất xúc tác hóa lỏng, các hạt có đường kính 20-30 nm và chiều dài 100-180 nm, và chất xúc tác chứa lưu huỳnh theo tỷ lệ mol của S / Fe = 2.
6. Phương pháp theo điểm 1, trong đó quá trình hydro hóa ở giai đoạn (5) được thực hiện trong các điều kiện sau: nhiệt độ phản ứng 330-390 ° C; áp suất phản ứng 10-15 MPa; tỷ lệ giữa lượng khí và chất lỏng 600-1000 nl / kg; vận tốc vũ trụ 0,8-2,5 h-1.
7. Phương pháp theo điểm 1, trong đó dung môi cho hydro được tái chế là sản phẩm dầu mỏ hóa lỏng được hydro hóa có điểm sôi trong khoảng 220-450 ° C.
8. Quy trình theo điểm 1, trong đó cặn trong cột chưng cất chân không (12) có hàm lượng chất rắn từ 50-55% khối lượng.
9. Phương pháp theo điểm 1, trong đó hỗn hợp của phần nhiên liệu điêzen rời khỏi cột áp suất khí quyển và phần chưng cất từ cột chân không có điểm sôi là C 5 trong khoảng 530 ° С.
10.Quy trình theo điểm 1, trong đó lò phản ứng xử lý nước tầng sôi tuần hoàn cưỡng bức (13) là một lò phản ứng bên trong, trong đó một máy bơm tuần hoàn được lắp đặt gần đáy lò phản ứng và chất xúc tác trong lò phản ứng có thể được thay thế trong quá trình vận hành.
YÊU CẦU
1. Phương pháp đốt than, bao gồm làm khô, nghiền đến trạng thái phân tán mịn, trộn than xay với dòng khí chứa ôxy có hướng và đốt cháy, đặc trưng ở chỗ than đá được nung nóng đến nhiệt độ bán cốc ở ít nhất 500 ° C, các hydrocacbon ở thể khí dễ bay hơi được giải phóng khỏi nó, chúng được phân chia thành các phần lỏng và khí bằng cách ngưng tụ, và bán cốc thu được bằng cách đốt nóng than đá được trộn với dòng khí chứa oxy được điều hướng và đốt cháy.
2. Phương pháp theo điểm 1, có đặc điểm là việc làm khô than đá được thực hiện đồng thời với việc nghiền than.
3. Phương pháp theo điểm 1, có đặc điểm là than đã xay được nung nóng đến nhiệt độ bán cốc bằng cách trộn nó với chất mang nhiệt dạng khí.
4. Phương pháp theo điểm 1, có đặc điểm là than đá được nung đến nhiệt độ bán cốc bằng cách trộn nó với chất mang nhiệt rắn có nhiệt độ 800-1300 ° C.
5. Phương pháp theo điểm 3, có đặc điểm là chất mang nhiệt ở thể khí là khí được tạo thành trong quá trình đốt cháy ít nhất một phần hydrocacbon ở thể khí dễ bay hơi.
6. Phương pháp theo điểm 3, có đặc điểm là chất làm mát dạng khí là các khí được tạo thành trong quá trình đốt cháy ít nhất một phần của bán cốc thu được.
7. Phương pháp theo điểm 4, có đặc điểm là chất mang nhiệt rắn là bán cốc thu được.
8. Phương pháp theo điểm 4, có đặc điểm là chất mang nhiệt rắn là cát thạch anh.
9. Phương pháp theo điểm 4, có đặc điểm là chất mang nhiệt rắn là vật liệu phân tán bằng gốm.
10. Phương pháp theo điểm 4, có đặc điểm là chất mang nhiệt rắn là than.
11. Phương pháp theo điểm 4, đặc trưng ở chỗ chất mang nhiệt rắn là một oxit của một chất vô cơ có kích thước phần nhỏ từ 0,5-5 mm.
12. Phương pháp theo điểm 9, hoặc 10, hoặc 12, có đặc điểm là chất làm nguội sau khi sử dụng được tách khỏi bán cốc bằng sàng.
13. Phương pháp theo điểm 1, đặc trưng ở chỗ phần khí của hydrocacbon dễ bay hơi được đốt cháy hoàn toàn hoặc một phần.
14. Phương pháp theo điểm 13, đặc trưng ở chỗ phần khí của hydrocacbon dễ bay hơi được tinh chế từ các chất có chứa lưu huỳnh trước khi đốt cháy.
15. Phương pháp theo điểm 1, đặc trưng ở chỗ, việc đốt nóng than đá đến nhiệt độ bán cốc được thực hiện trong một buồng xoáy bằng cách trộn nó với khí nóng.
Câu trả lời cho đoạn 19
1. Những nguồn hiđrocacbon chính trong tự nhiên mà em biết là dầu mỏ, khí đốt tự nhiên, đá phiến sét, than đá.
2. Thành phần của khí thiên nhiên là gì? Chỉ ra trên bản đồ địa lý các mỏ quan trọng nhất: a) khí tự nhiên; đun sôi; c) than đá.
3. Khí thiên nhiên có ưu điểm gì so với các nhiên liệu khác? Khí thiên nhiên được sử dụng cho những mục đích gì trong công nghiệp hóa chất? So với các nguồn hiđrocacbon khác, khí thiên nhiên là loại khí dễ khai thác, vận chuyển và chế biến nhất. Trong công nghiệp hóa chất, khí thiên nhiên được sử dụng như một nguồn cung cấp các hydrocacbon có trọng lượng phân tử thấp.
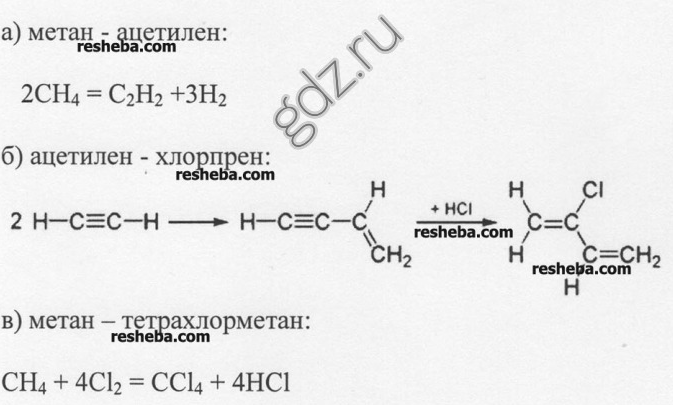
4. Viết các phương trình phản ứng thu được: a) Axetilen từ metan; b) cao su cloropren từ axetylen; c) cacbon tetraclorua từ metan.
5. Sự khác nhau giữa khí dầu mỏ và khí thiên nhiên Khí đồng hành là những hiđrocacbon dễ bay hơi hòa tan trong dầu mỏ. Sự cô lập của chúng xảy ra bằng cách chưng cất. Không giống như khí tự nhiên, nó có thể được giải phóng ở bất kỳ giai đoạn nào của quá trình phát triển mỏ dầu.
6.Mô tả các sản phẩm chính thu được từ khí đồng hành Các sản phẩm chính: metan, etan, propan, n-butan, pentan, isobutan, isopentan, n-hexan, n-heptan, hexan và các đồng phân của heptan.
7. Kể tên các sản phẩm dầu quan trọng nhất, cho biết thành phần và lĩnh vực ứng dụng của chúng.
8. Dầu bôi trơn dùng trong sản xuất nào? Dầu bánh răng, dầu công nghiệp, dầu cắt gọt cho máy công cụ, v.v.
9. Quá trình chưng cất dầu được thực hiện như thế nào?
10. Crack dầu là gì? Lập phương trình cho các phản ứng tách hydrocacbon và trong quá trình này.
11. Tại sao trong quá trình chưng cất trực tiếp dầu chỉ thu được không quá 20% xăng vì hàm lượng phần xăng trong dầu có giới hạn.
12. Sự khác nhau giữa cracking nhiệt và cracking xúc tác? Nêu mô tả về các chất khí của quá trình cracking nhiệt và xúc tác Trong crackinh nhiệt cần nung chất phản ứng đến nhiệt độ cao, trong cracking xúc tác việc đưa chất xúc tác vào làm giảm năng lượng hoạt hóa của phản ứng có thể làm giảm đáng kể phản ứng. nhiệt độ.
13. Trên thực tế, người ta có thể phân biệt xăng bị nứt với xăng chạy thẳng bằng cách nào? Xăng nứt có trị số octan cao hơn xăng chạy thẳng, tức là. khả năng chống kích nổ cao hơn và được khuyến khích sử dụng cho động cơ đốt trong.
14. Thơm hóa dầu là gì? Viết các phương trình phản ứng giải thích quá trình này.
15. Sản phẩm chính của than cốc thu được là gì? Naphtalen, antracen, phenanthren, phenol và dầu than.
16. Than cốc được sản xuất như thế nào và được sử dụng ở đâu? Than cốc là sản phẩm rắn xốp màu xám thu được khi luyện than cốc ở nhiệt độ 950-1100 mà không có ôxy. Nó được sử dụng để nấu chảy sắt, làm nhiên liệu không khói, chất khử quặng sắt và bột nở làm vật liệu nạp.
17. Sản phẩm chính thu được là gì: a) từ nhựa than đá; b) từ nước hắc ín; c) từ khí lò cốc? Chúng được áp dụng ở đâu? Khí lò luyện cốc có thể thu được những chất hữu cơ nào? A) benzen, toluen, naphtalen - công nghiệp hóa chất b) amoniac, phenol, axit hữu cơ - công nghiệp hóa học c) hiđro, metan, etilen - nhiên liệu.
18. Nhắc lại tất cả các cách chính để thu được hiđrocacbon thơm. Sự khác biệt giữa các phương pháp thu nhận hiđrocacbon thơm từ sản phẩm luyện cốc của than và dầu là gì? Viết phương trình của các phản ứng tương ứng.
19. Giải thích rằng trong quá trình giải quyết các vấn đề năng lượng trong nước, các phương thức chế biến và sử dụng tài nguyên hydrocacbon sẽ được cải thiện như thế nào. chi phí của tất cả sản xuất, v.v.
20. Triển vọng thu được nhiên liệu lỏng từ than đá Trong tương lai, việc sản xuất nhiên liệu lỏng từ than là có thể thực hiện được với điều kiện giảm chi phí sản xuất.
Nhiệm vụ 1. Biết rằng khí chứa 0,9 metan, 0,05 etan, 0,03 propan, 0,02 nitơ theo thể tích. Để đốt cháy 1 m3 khí này ở điều kiện thường cần thể tích không khí là bao nhiêu?

Nhiệm vụ 3. Tính thể tích (theo l) và khối lượng (kg) của cacbon monoxit (IV) sẽ thu được khi đốt cháy 5 mol octan (n.o.).
2 Hydro hóa
Hydro hóa than nâu là một quá trình chế biến trực tiếp than thành nhiên liệu tổng hợp ở trạng thái tập hợp lỏng và khí, xảy ra ở áp suất cao và nhiệt độ tương đối cao.
Hướng chế biến than này đang được tìm hiểu ở các nước trên thế giới.Ở nước ngoài, công nghệ này đã nhận được sự giới thiệu công nghiệp lớn nhất ở Nam Phi, nơi có bốn nhà máy hoạt động, với tổng công suất hàng năm khoảng 8 - 10 triệu tấn nhiên liệu lỏng. Công việc được thực hiện bằng công nghệ SASOL đã được cấp bằng sáng chế dựa trên phương pháp Fischer-Tropsch cải tiến. Do SASOL có chính sách duy trì các khoản thanh toán cao cho quyền sử dụng công nghệ, điều này dẫn đến chi phí triển khai công nghiệp cao ở các quốc gia khác. []
Chuẩn bị than nâu bao gồm nghiền, làm khô, chuẩn bị than đá hydrogenat. Quá trình nghiền được thực hiện đến kích thước hạt nhỏ hơn 0,1 mm - để tăng khả năng phản ứng của bề mặt, nó được thực hiện trong các thiết bị phân hủy. Trong trường hợp này, bề mặt cụ thể bên ngoài tăng lên 20-30 lần, thể tích các lỗ chân lông chuyển tiếp - gấp 5-10 lần. Sau đó than được sấy khô. Các lỗ rỗng chứa đầy hơi ẩm, ngăn cản sự xâm nhập của thuốc thử vào chất than, nó được giải phóng trong quá trình ở vùng phản ứng, làm giảm áp suất riêng phần của H2, đồng thời cũng làm tăng lượng nước thải. Để sấy khô, người ta sử dụng máy sấy hơi dạng ống, buồng xoáy, máy sấy dạng ống trong đó than được sấy khô đến độ ẩm còn lại là 1,5%. Chất mang nhiệt là các khí lò nóng có hàm lượng O2 tối thiểu (0,1-0,2%) để than không bị oxy hóa. Than không được đun nóng trên 150-200 ° C để tránh giảm khả năng phản ứng.
Yêu cầu đối với than nâu để hóa lỏng
Trên cơ sở tài liệu thực nghiệm lớn, người ta đã chứng minh được rằng than có tính thủy lực tốt chứa từ 65% đến 85% C, hơn 5% H và có năng suất bay hơi (V) hơn 30%. Độ ẩm hợp lý của than ban đầu cho quá trình hydro hóa - Wrt = 10-15%, hàm lượng tro Ad = 10-12%, giá trị d
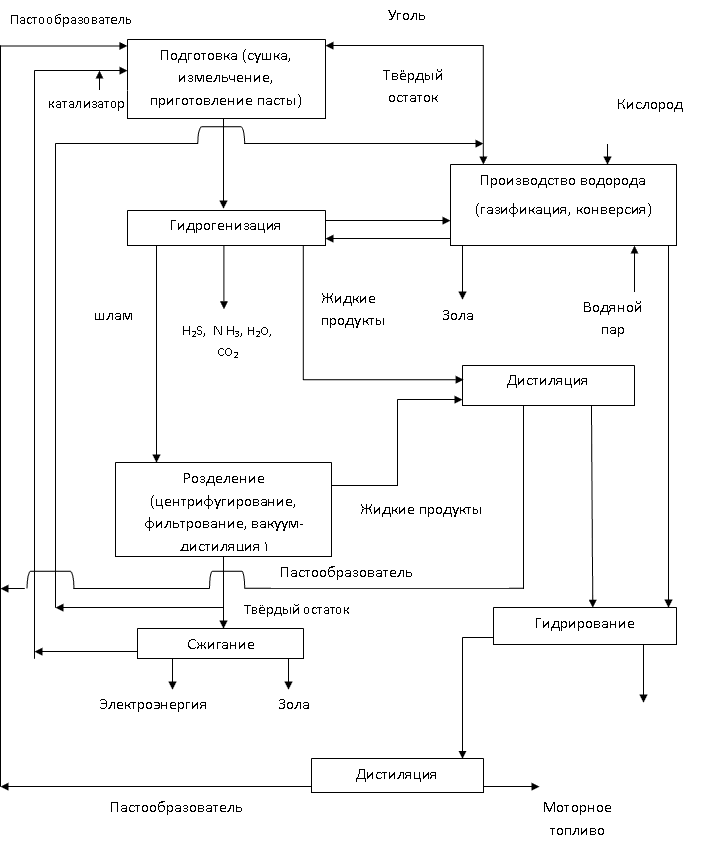
Sơ đồ hydro hóa phổ biến nhất được thể hiện trong Hình 1.2 []
Cơm. 1.2 - Đề án sản xuất nhiên liệu lỏng tổng hợp từ than nâu
Động thái tiêu thụ khí đốt than trên thế giới
| Mục đích sử dụng | Sử dụng vào năm 2001, MW cho khí đốt | Chia sẻ năm 2001,% | Được đưa vào vận hành trước cuối năm 2004, MW cho khí đốt | Mức tăng công suất hàng năm trong giai đoạn 2002-2004,% |
| Sản xuất hóa chất | 18 000 | 45 | 5 000 | 9,3 |
| Khí hóa trong chu trình (phát điện) | 12 000 | 30 | 11 200 | 31 |
| Tổng hợp Fischer-Tropsch | 10 000 | 25 | ||
| TOÀN BỘ | 40 000 | 100 | 17 200 | 14,3 |
Dữ liệu đưa ra chứng minh rõ ràng sự gia tăng của động lực tham gia vào quá trình khí hóa than trong ngành công nghiệp toàn cầu. Sự quan tâm gia tăng đối với quá trình khí hóa than trong chu trình ở các nước phát triển là do hai lý do.
Thứ nhất, các nhà máy nhiệt điện có khí hóa nội chu trình ít nguy hiểm hơn về mặt môi trường. Nhờ xử lý trước khí, lượng khí thải ôxít lưu huỳnh, ôxít nitơ và các chất dạng hạt được giảm thiểu.
Thứ hai, việc sử dụng chu trình nhị phân có thể làm tăng đáng kể hiệu suất của nhà máy điện và do đó, giảm mức tiêu thụ nhiên liệu cụ thể.
Trong bảng. Bảng 2 cho thấy các giá trị đặc trưng của lượng phát thải cụ thể và hiệu quả đối với các TPP có khí hóa trong chu trình và đối với các TPP có đốt than truyền thống.
ban 2
Hiệu quả và phát thải cụ thể đối với các nhà máy nhiệt điện có khí hóa vòng quay và đốt than thông thường
| Thông số | Nhà máy nhiệt điện than truyền thống | TPP với khí hóa trong chu trình |
| Nồng độ các chất độc hại trong khói lò (đối với nhà máy nhiệt điện than - theo tiêu chuẩn Châu Âu), mg / m3 - SOx - KHÔNGx - Các hạt rắn | 130 150 16 | 10 30 10 |
| Hiệu suất điện,% | 33-35 | 42-46 |
Cần lưu ý rằng chi phí vốn cụ thể khi sử dụng khí hóa nội vòng là khoảng 1500 đô la Mỹ trên 1 kW với triển vọng giảm xuống 1000-1200 đô la Mỹ, trong khi đối với một nhà máy nhiệt điện đốt than truyền thống, chi phí vốn cụ thể là khoảng 800-900 đô la Mỹ trên 1 kW. Rõ ràng là một nhà máy nhiệt điện có quá trình khí hóa nhiên liệu rắn trong vòng hấp dẫn hơn khi có các hạn chế về môi trường tại địa điểm và khi sử dụng nhiên liệu khá đắt tiền, do mức tiêu thụ nhiên liệu trên 1 kW giảm xuống.
Những điều kiện này là điển hình cho các nước phát triển.Hiện nay, việc sử dụng khí hóa trong các nhiên liệu rắn được coi là hướng đi có triển vọng nhất trong lĩnh vực năng lượng.
3.3 Sự phát triển kỹ thuật trong thế kỷ qua
Hiện tại, các lĩnh vực áp dụng phương pháp khí hóa hiệu quả nhất sau đây đã được xác định:
- khí hóa các nhiên liệu có lưu huỳnh và tro cao với quá trình đốt cháy các khí tạo thành sau đó tại các nhà máy nhiệt điện mạnh. Các loại than được khai thác hàng năm ở Nga chứa khoảng 10 triệu tấn lưu huỳnh, hầu hết trong số đó, khi đốt cháy, được thải vào khí quyển dưới dạng các oxit lưu huỳnh độc hại và sunfua cacbon. Trong quá trình khí hóa than lưu huỳnh, hydro sulfua được hình thành, có thể được chiết xuất tương đối dễ dàng và sau đó được chế biến thành lưu huỳnh thương mại hoặc axit sulfuric.
- khí hóa nhiên liệu rắn để sản xuất quy mô lớn thay thế khí tự nhiên. Hướng này có tầm quan trọng lớn nhất đối với việc cung cấp khí đốt cục bộ cho các khu vực xa các mỏ dầu và khí đốt tự nhiên hoặc từ các đường ống chính.
- khí hóa nhiên liệu rắn để thu được khí tổng hợp, khí khử và hydro cho nhu cầu của các ngành công nghiệp hóa chất, hóa dầu và luyện kim.
Quá trình khí hóa phụ thuộc vào nhiều yếu tố ảnh hưởng đến thành phần của khí tạo thành và nhiệt trị của nó. Về vấn đề này, vẫn chưa có một phân loại chung nào được chấp nhận chung về các phương pháp thực hiện quy trình đang được xem xét. Dưới đây là một trong những tùy chọn phân loại khả thi.
Theo loại nổ (tác nhân khí hóa): không khí, không khí-oxy, hơi nước-không khí, hơi nước-oxy.
Theo áp suất: ở áp suất khí quyển, ở áp suất cao.
· Theo kích thước của các hạt nhiên liệu: khí hóa nhiên liệu dạng hạt thô (cục), hạt mịn và dạng bột.
· Theo các tính năng thiết kế của vùng phản ứng: trong lớp nhiên liệu dày đặc cố định, trong lớp nhiên liệu sôi, trong ngọn lửa than nghiền thành bột.
bằng phương pháp loại bỏ tro: ở dạng rắn, dạng lỏng xỉ.
Theo phương pháp cung cấp nhiệt: đốt cháy một phần nhiên liệu trong máy tạo khí, trộn nhiên liệu với chất mang nhiệt rắn, lỏng hoặc khí được nung nóng trước (gia nhiệt tái sinh), cung cấp nhiệt qua thành thiết bị (gia nhiệt hồi phục).
Cacbon monoxit, cacbonyl kim loại và quy tắc 18 electron
Nhiều
tổng hợp dựa trên carbon monoxide và
hydro đại diện cho một lượng lớn
thực tế cũng như lý thuyết
lãi suất, cho phép từ hai
chất đơn giản nhất để nhận chất giá trị nhất
hợp chất hữu cơ. Và đây
xúc tác đóng một vai trò quan trọng
kim loại chuyển tiếp có khả năng
kích hoạt các phân tử CO trơ và
H2.
Kích hoạt các phân tử là quá trình dịch của chúng thành
trạng thái phản ứng hơn.
Đặc biệt cần lưu ý rằng trong các phép biến đổi
khí tổng hợp đã được phát triển rộng rãi
một loại xúc tác mới - xúc tác bằng phức
kim loại chuyển tiếp hoặc phức kim loại
xúc tác (xem bài của O.N. Temkin
).
Cho nên
Phân tử CO có trơ không? Đại diện
về tính trơ của cacbon monoxit
ký tự điều kiện. Trở lại năm 1890 Thứ Hai
thu được từ niken kim loại và
cacbon monoxit cacbonyl đầu tiên
hợp chất kim loại, chất lỏng dễ bay hơi
có nhiệt độ sôi là 43 ° C - Ni (CO)4 .
Lịch sử của khám phá này thật thú vị.
mà có thể được phân loại là ngẫu nhiên. Thứ hai,
điều tra nguyên nhân của sự ăn mòn nhanh chóng
lò phản ứng niken trong sản xuất
soda từ NaCl, amoniac và CO2,
phát hiện ra rằng nguyên nhân của sự ăn mòn là
hiện diện trong CO2 tạp chất
carbon monoxide, đã phản ứng
với niken để tạo thành tetracarbonyl
Ni (CO)4 .
Khám phá này cho phép Mond tiến xa hơn
phát triển các phương pháp làm sạch niken
thông qua việc sản xuất một cacbonyl dễ bay hơi
niken và nhiệt tiếp theo của nó
lại phân hủy thành niken và CO. Bên kia
25 năm cũng tình cờ phát hiện ra cacbonyl
sắt - Fe (CO)5.
Khi BASF mở ra một cái tên bị lãng quên từ lâu
xi lanh thép với CO, được tìm thấy ở dưới cùng
chất lỏng màu vàng - sắt pentacacbonyl,
mà dần dần phát triển thành
kết quả của một phản ứng kim loại
sắt với CO dưới áp suất cao.
Vì cacbonyl kim loại là
các hợp chất có độc tính cao, ban đầu
thái độ của các nhà hóa học đối với họ rất
tuyệt, nhưng trong tương lai đã
các thuộc tính tuyệt vời được phát hiện, bao gồm
bao gồm cả chất xúc tác, đã xác định
ứng dụng rộng rãi của chúng, đặc biệt là trong hóa học
cacbon monoxit. Lưu ý rằng nhiều
kim loại ở trạng thái phân tán mịn
có thể phản ứng trực tiếp
với carbon monoxide, nhưng theo cách này
chỉ nhận niken cacbonyl và
ốc lắp cáp. Cacbonyl của các kim loại khác
thu được bằng cách khôi phục các hợp chất của chúng
trong sự hiện diện của CO ở mức cao
áp lực.
Hợp chất
phức hợp cacbonyl chuyển tiếp
kim loại có thể được dự đoán dựa trên
Quy tắc 18 electron, theo đó
phức hợp sẽ ổn định nếu tổng
các electron hóa trị của kim loại và các electron,
được cung cấp bởi phối tử, trong trường hợp của chúng tôi
CO, sẽ bằng 18, vì trong trường hợp này
cấu hình điện tử tương ứng
cấu hình ổn định của nguyên tử
khí quý (krypton).
Phân tử
carbon monoxide có đơn độc
cặp electron, trong khi một cặp electron
về carbon có thể được cung cấp
để tạo liên kết với kim loại
loại người nhận tài trợ. Như
Ví dụ, hãy xem xét cấu trúc của cacbonyl
sắt và niken Fe (CO)5 và
Ni (CO)4.
Các nguyên tử sắt và niken lần lượt có
Các điện tử hóa trị 8 và 10, và để điền vào
lớp vỏ electron của nguyên tử trước khi cấu hình
nguyên tử khí cao quý krypton
10 và 8 điện tử bị thiếu, và do đó
trong sự hình thành cacbonyl thành nguyên tử sắt
phải cung cấp các cặp electron
năm phân tử CO và một nguyên tử niken
bốn.
chuyển tiếp
kim loại có số hóa trị lẻ
electron, hình thành hạt nhân
phức cacbonyl. Vì vậy, đối với coban,
có chín điện tử hóa trị
để cấu hình điện tử ổn định
thiếu chín electron. lõi đơn
phức hợp bằng cách lấy bốn cặp
từ các phân tử CO sẽ có
điện tử, và các hạt như vậy của gốc
các nhân vật tương tác với nhau.
để tạo thành một liên kết kim loại-kim loại, và
dẫn đến sự hình thành của một dimer
Co phức tạp2(CO)8.
Sự tương tác
hoặc sự phối hợp của carbon monoxide với
kim loại dẫn đến sự phân phối lại
mật độ electron không chỉ trên CO,
mà còn trên kim loại, điều này ảnh hưởng đáng kể đến
về khả năng phản ứng của cacbonyl
phức tạp. Phổ biến nhất là
được gọi là kiểu phối hợp tuyến tính
CO:
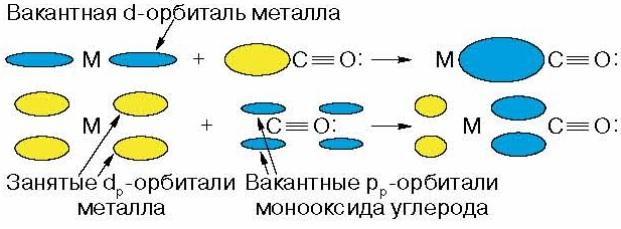
Tại
đây không chỉ là tương tác s
do một cặp êlectron tự do
cacbon, mà còn tương tác p do
sự chuyển electron từ obitan d của kim loại
để trống năng lượng
các obitan cacbon:
Sự liên quan
Vì vậy, cần phải phát triển một công nghệ như vậy để chế biến sơ cấp và kết tụ than nâu, có tính đến các đặc tính cụ thể của than nâu nguyên thủy, các điều kiện của quá trình vận chuyển thủy lực than và các yêu cầu đối với đặc điểm của nguyên liệu than trong các hoạt động chế biến tiếp theo - nhiệt phân, đốt, hóa lỏng, đóng bánh, khử nước. Giải pháp cho vấn đề này có thể kể đến công nghệ xử lý than bằng thuốc thử dầu - kết dầu.
Tập hợp dầu có chọn lọc của than kết hợp một loạt các quy trình để cấu trúc một pha than phân tán mỏng trong môi trường nước sử dụng thuốc thử dầu.Các quá trình tập hợp dầu có chọn lọc của than dựa trên cơ chế tương tác kết dính giữa bề mặt than ưa chảy và dầu, dẫn đến kết dính và thấm ướt có chọn lọc của nó trong một dòng nước rối. Các hạt ưa nước không bị dầu làm ướt không có trong cấu trúc của cốt liệu, điều này cho phép phân lập chúng ở dạng huyền phù đá.
Việc xử lý than nâu bằng cách kết hợp dầu chọn lọc giúp loại bỏ sự phân huỷ và ngâm ủ của nó, "bảo quản" các chất hữu cơ trong các tập hợp kỵ nước, dễ bị mất nước bằng phương pháp cơ học và là nguyên liệu tốt cho quá trình nhiệt phân, đóng bánh và khí hoá.
1 Briquetting
Đóng bánh than là một quá trình vật lý và hóa học để thu được một sản phẩm chất lượng cao về cơ học và nhiệt học - một viên than có hình dạng hình học, kích thước và trọng lượng nhất định.
Quy trình công nghệ đóng bánh than nâu không có chất kết dính bao gồm các công việc: chuẩn bị than về kích thước và độ ẩm, ép.
Các chỉ tiêu công nghệ mà than non đóng bánh phải tuân thủ: trọng lượng viên bánh 100-500 g, độ bền mài mòn cơ học 75-80%, nén và uốn lần lượt 70-90 và 10-15 MPa, độ hút ẩm 3-4%, nhiệt trị 24000-30000 kJ / kg, hàm lượng tro 10-25%. []