Czy muszę uziemić podgrzewany wieszak na ręczniki?
Najpierw musisz wiedzieć, że uziemienie (budowa pętli uziemienia własnymi rękami) nie jest wymagane, jeśli:
- 1. Używasz elektrycznego podgrzewanego wieszaka na ręczniki (takie podgrzewane wieszaki na ręczniki są zwykle wyposażone w specjalne wtyczki, w których znajduje się przewód uziemiający, wszystko to jest podłączone do gniazdka, a same gniazda muszą już być podłączone do pętli uziemienia) .
- 2. Mieszkasz w prywatnym domu lub mieszkaniu i masz oddzielny system ogrzewania.
Uziemienie podgrzewanego wieszaka na ręczniki jest obowiązkowe w następujących przypadkach:
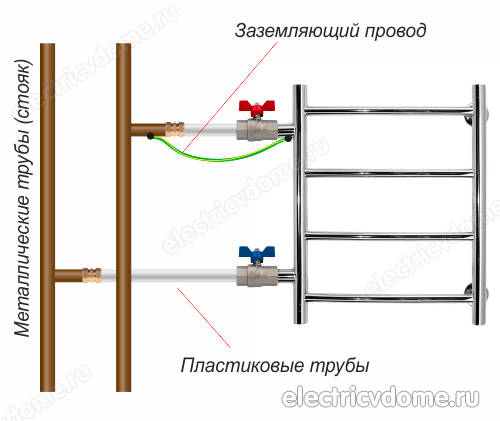
- 1. Jeśli Twoja suszarka jest podłączona do systemu grzewczego plastikową rurką. Wewnątrz metalowo-plastikowej rury znajduje się aluminium, które przewodzi prąd elektryczny: na złączach, w których znajdują się złączki, obwód elektryczny jest przerwany. W związku z tym taki podgrzewany wieszak na ręczniki musi być podłączony do pętli uziemienia lub do pionu gorącej wody.
- 2. Jeśli system ciepłej wody jest wykonany z rur z tworzywa sztucznego.
Jak uziemić podgrzewany wieszak na ręczniki?
Wszystkie podgrzewane elektrycznie wieszaki na ręczniki, jak wspomniano powyżej, są podłączone do uziemionego gniazdka, podczas gdy takie suszarki mają przewód uziemiający z oddzielnym stykiem na wtyczce. Ponieważ podgrzewane wieszaki na ręczniki są zwykle instalowane w łazience, należy sprawdzić gniazdko, do którego będą podłączone. Taki wylot musi znajdować się w specjalnej obudowie ochronnej, która zapobiega przedostawaniu się wilgoci do samego wylotu.
Istnieją 2 główne sposoby uziemienia podgrzewanego wieszaka na ręczniki:
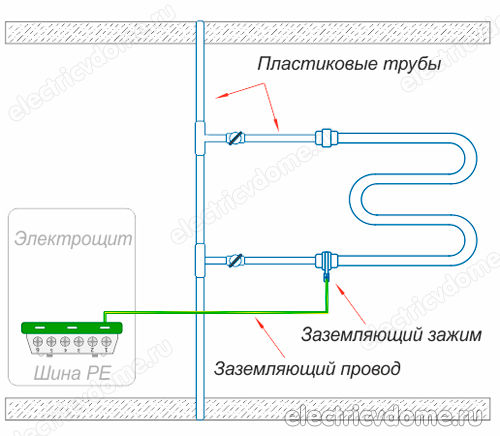
- 1. Używając systemu wyrównywania potencjałów, który należy zainstalować ręcznie, uziemić ten system do wspólnego uziemienia panelu elektrycznego. Należy to zrobić, jeśli komunikacja wykonana z polimerów (rury metalowo-plastikowe) jest używana zamiast komunikacji metalowej w domu lub mieszkaniu.
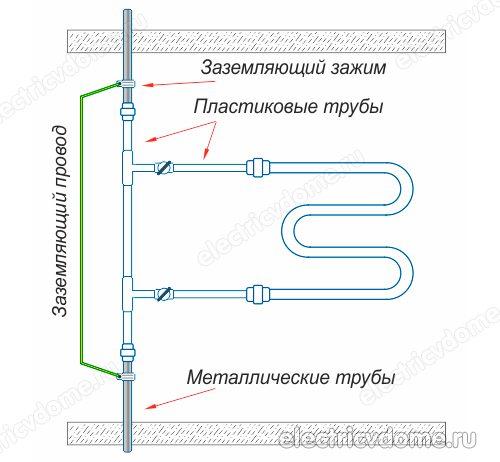
- 2. Uziemienie bezpośrednio rury korpusu podgrzewanego wieszaka na ręczniki za pomocą konwencjonalnego drutu do stalowego pionu.
Aby wykonać uziemienie podgrzewanego wieszaka na ręczniki w drugi sposób, najpierw musisz zdobyć zacisk, po usunięciu z niego wszystkich materiałów izolacyjnych. Ten zacisk musi mieć zacisk do podłączenia przewodu. Następnie zacisk jest mocowany do rury korpusu podgrzewanego wieszaka na ręczniki.
Bierze się zwykły drut miedziany, który powinien mieć przekrój 4 mm2. Ten przewód jest podłączony z jednej strony do zacisku zaciskowego, jego drugi koniec musi być podłączony do uziemienia panelu elektrycznego lub do stalowej rury nośnej. Ponadto nie zapomnij podłączyć innych urządzeń w łazience do pętli uziemienia.
| Takie metody nie wymagają dużo czasu na ich wdrożenie, ale w zamian uzyskują długą i nieprzerwaną pracę podgrzewanego wieszaka na ręczniki, a w przyszłości pytanie „jak uziemić podgrzewany wieszak na ręczniki” nie sprawi trudności. |
Przyjaciele również oglądają wideo, co jest potrzebne do uziemienia podgrzewanego wieszaka na ręczniki.
Powiązane treści na stronie:
- O uziemieniu w prostych słowach
- Dlaczego wanna jest uziemiona?
- Konstrukcja urządzenia uziemiającego
Przyczyny elektrokorozji
Pojawienie się prądów wirowych Foucaulta jest dość złożonym i nieprzewidywalnym zjawiskiem. W systemach zaopatrzenia w ciepłą wodę, a czasami w systemie grzewczym, takie prądy pojawiają się z wielu powodów, które wydają się nie mieć ze sobą związku.
Na ogół prądy wirowe powstają z różnicą potencjałów. Podczas budowy domu wszystkie konstrukcje metalowe są podłączone do wspólnej pętli uziemienia, a wcześniej w budownictwie używano uziemienia wzdłuż pętli, ale teraz są zadowoleni z metody wyrównania potencjałów.
Kiedy w mieszkaniu zamiast istniejącego systemu metalowego montuje się systemy z tworzywa sztucznego, różnica potencjałów powstaje z powodu przebicia (na przykład jeden potencjał jest na podgrzewanym wieszaku na ręczniki, a zupełnie inny na pionie). Stąd różnica potencjałów, stąd prądy błądzące. Mogą również wystąpić w wyniku zwarcia, braku uziemienia pobliskich elektrycznych urządzeń gospodarstwa domowego, czy to pralki, i tak dalej.
Ważną rolę odgrywa nawet obecność/brak torów tramwajowych w bezpośrednim sąsiedztwie. Prądy błądzące występują również w przypadku naruszenia izolacji przewodów elektrycznych, przerwy w sieci lub uziemienia systemu grzewczego.
Wszystko to prowadzi do korozji elektrycznej instalacji wodno-kanalizacyjnych, spowodowane jest również bliskością dwóch różnych materiałów, zwłaszcza stali nierdzewnej i czarnej. W miejscu, przez które ładunek przechodzi do ogrzanego wieszaka na ręczniki, w efekcie zachodzi reakcja elektrochemiczna, a więc tam dochodzi do uszkodzeń. Takie problemy są zwykle rozwiązywane przez bezpośrednie uziemienie samego podgrzewanego wieszaka na ręczniki.
Kupując wieszak na ręczniki podgrzewany wodą należy zapoznać się z zasadami jego działania, w szczególności zwrócić uwagę czy konieczne jest uziemienie wieszaka podgrzewanego czy nie, aby uwzględnić ten punkt podczas naprawy, a nie po zakończeniu naprawy
Po co uziemiać podgrzewany wodą wieszak na ręczniki?
Po tym, jak plastikowe rury zaczęły zastępować zwykłe metalowe, zaczęli ignorować ich uziemienie, błędnie wierząc, że metalowa rura i metalowo-plastikowa rura mają taką samą przewodność elektryczną. To nie jest prawda. Nie ma kontaktu między rurą metalowo-plastikową a aluminium: nie są one połączone.
Praktyka pokazuje, że 90 procent podgrzewanych wieszaków na ręczniki zaczyna przeciekać właśnie w przypadku wymiany metalowych systemów ciepłej wody na ich plastikowe odpowiedniki (na przykład polipropylen). Stare rury metalowe są zastępowane nowoczesnymi plastikowymi w celu ograniczenia prądów wirowych. Jednak korozja nadal się ujawnia.
Pierwsze objawy korozji elektrycznej to pojawienie się plam rdzy na podgrzewanym wieszaku na ręczniki, a rdza pojawia się nawet na urządzeniach wykonanych ze stali nierdzewnej. Ogólnie rzecz biorąc, wszystkie metalowe produkty elektryczne mające kontakt z wodą podlegają zarówno korozji elektrochemicznej, jak i galwanicznej. Elektrokorozja występuje w obecności prądów błądzących. W rezultacie metal jest jednocześnie wystawiony na działanie prądu elektrycznego i wody, po czym pojawiają się awarie metalu, a stamtąd zaczyna się rozprzestrzeniać korozja.
Kiedy dwa różne metale wchodzą w kontakt, z których jeden jest bardziej reaktywny niż drugi, oba metale wchodzą w reakcję chemiczną. Czysta woda jest bardzo słabym przewodnikiem prądu elektrycznego (dielektrykiem), ale ze względu na duże stężenie różnych zanieczyszczeń woda zamienia się w rodzaj elektrolitu.
Nie zapominaj, że temperatura ma duży wpływ na przewodność elektryczną: im wyższa temperatura wody, tym lepiej przewodzi prąd. Zjawisko to znane jest jako „korozja galwaniczna”, to ona metodycznie sprawia, że podgrzewany wieszak na ręczniki staje się bezużyteczny.
Konieczność ochrony antykorozyjnej
Ochrona metalu przed wpływami, które mają destrukcyjny wpływ na jego powierzchnię, jest jednym z głównych zadań stojących przed osobami pracującymi z mechanizmami, jednostkami i maszynami, statkami i procesami budowlanymi.

Im aktywniej użytkowane jest urządzenie lub część, tym bardziej narażone jest na destrukcyjne działanie warunków atmosferycznych, płynów, z którymi mamy do czynienia podczas eksploatacji.Wiele gałęzi nauki i produkcji przemysłowej pracuje nad ochroną metalu przed korozją, ale główne metody pozostają niezmienione i polegają na tworzeniu powłok ochronnych:
- metal;
- niemetalowe;
- chemiczny.
Powłoki niemetaliczne powstają przy użyciu związków organicznych i nieorganicznych, ich zasada działania jest dość skuteczna i różni się od innych rodzajów ochrony. Do tworzenia niemetalicznej ochrony w produkcji przemysłowej i budowlanej stosuje się farby i lakiery, beton i bitum oraz związki wysokocząsteczkowe, które zostały szczególnie aktywnie przyjęte w ostatnich latach, kiedy chemia polimerów osiągnęła wielkie wyżyny.

Chemia przyczyniła się do powstania powłok ochronnych metodami:
- utlenianie (tworzenie warstwy ochronnej na metalu za pomocą warstw tlenkowych);
- fosforanowanie (folie fosforanowe);
- azotowanie (nasycenie powierzchni stali azotem);
- cementacja (związki z węglem);
- niebieszczenie (związki z substancjami organicznymi);
- zmiana składu metalu poprzez wprowadzenie do niego dodatków antykorozyjnych);
- modyfikacja otaczającego środowiska korozyjnego poprzez wprowadzenie inhibitorów, które na nie wpływają.
Ochrona przed korozją elektrochemiczną jest procesem odwrotnym do korozji elektrochemicznej. W zależności od przesunięcia potencjału metalu w stronę dodatnią lub ujemną, istnieje ochrona anodowa i katodowa. Poprzez podłączenie osłony lub źródła prądu stałego do produktu metalowego, na powierzchni metalu powstaje polaryzacja katodowa, co zapobiega zniszczeniu metalu przez anodę.
Metody ochrony elektrochemicznej składają się z dwóch opcji:
- powłoka metalowa jest chroniona przez inny metal, który ma bardziej ujemny potencjał (tzn. metal ochronny jest mniej stabilny niż chroniony) i nazywa się to anodowaniem;
- powłoka jest nakładana z mniej aktywnego metalu, a następnie jest i jest nazywana katodową.

Ochroną anodową przed korozją jest na przykład żelazo ocynkowane. Dopóki cały cynk z warstwy ochronnej nie zostanie zużyty, żelazo będzie względnie bezpieczne.
Ochrona katodowa to niklowanie lub miedziowanie. W takim przypadku zniszczenie warstwy ochronnej prowadzi do zniszczenia warstwy, którą chroni. Dołączenie ochraniacza w celu ochrony produktu metalowego nie różni się od reakcji w innych przypadkach. Protektor działa jak anoda, a to, co jest pod jego protektoratem, pozostaje nienaruszone, wykorzystując stworzone dla niego warunki.
Czym jest korozja
Proces niszczenia górnej warstwy materiału metalicznego pod wpływem wpływów zewnętrznych nazywany jest szeroko korozją.

Pojęcie korozja w tym przypadku jest jedynie cechą charakterystyczną tego, że powierzchnia metalu wchodzi w reakcję chemiczną i pod jej wpływem traci swoje pierwotne właściwości.
4 główne znaki, dzięki którym możesz określić, że ten proces istnieje:
- proces, który rozwija się na powierzchni i ostatecznie przenika do produktu metalowego;
- reakcja powstaje samorzutnie z powodu naruszenia stabilności równowagi termodynamicznej pomiędzy środowiskiem a układem atomów stopu lub monolitu;
- chemia postrzega ten proces nie tylko jako reakcję zniszczenia, ale jako reakcję redukcji i utleniania: wchodząc w reakcję, niektóre atomy zastępują inne;
- właściwości i właściwości metalu podczas takiej reakcji ulegają znacznym zmianom lub są tracone tam, gdzie występuje.
Metody ochrony metali
Korozja elektrochemiczna jest jedną z głównych przeszkód napotykanych na drodze działalności człowieka. Ochrona przed wpływem procesów destrukcyjnych i ich przepływem na powierzchni konstrukcji i konstrukcji jest jednym ze stałych i pilnych zadań każdej produkcji przemysłowej i wszelkiej działalności gospodarczej człowieka.

Opracowano kilka metod takiej ochrony i wszystkie są aktywnie wykorzystywane w codziennym cyklu życia:
- Ochrona elektrochemiczna - elektrolityczna zgodnie z zasadą działania, zastosowanie praw chemicznych, zabezpiecza metal na zasadzie anody, katody i bieżnika.
- Obróbka elektroiskrowa różnymi instalacjami - bezkontaktowa, kontaktowa, anodowo-mechaniczna.
- Natryskiwanie łukiem elektrycznym jest główną zaletą w grubości nałożonej warstwy i względnej taniości procesu.
- Skuteczna obróbka antykorozyjna polega na usunięciu zanieczyszczeń i oczyszczeniu obrabianej powierzchni, a następnie nałożeniu na powierzchnię powłoki antykorozyjnej, a następnie dodatkowej warstwy ochronnej.
Wszystkie te metody zostały opracowane w procesie działalności człowieka w celu ochrony narzędzi, pojazdów i transportu na styku kilku sektorów przemysłu oraz wykorzystania dorobku naukowego.
Korozja elektrochemiczna, będąca naturalnym procesem niszczenia powierzchni metalu pod wpływem obojętnych lub agresywnych czynników środowiskowych, to złożony problem. Straty ponoszą przedsiębiorstwa maszynowe, transportowe i przemysłowe, pojazdy. I to jest problem, który wymaga codziennego rozwiązania.
Rodzaje korozji
W zależności od rodzaju metalu i zachodzącej z nim reakcji redoks, korozja może być:
- jednolite lub nierówne;
- lokalne i punktowe (niektóre sekcje z jakiegoś powodu zareagowały, a inne nie);
- wrzodziejące, znane również jako wżery;
- podpowierzchnia;
- Pękanie;
- międzykrystaliczny, powstający wzdłuż granic kryształu metalu.
Ponadto, w zależności od tego, jakie czynniki zewnętrzne wpływają na powierzchnię, korozja może mieć charakter chemiczny i elektrochemiczny. Korozja chemiczna występuje w wyniku niektórych reakcji pod wpływem oddziaływań chemicznych, ale bez udziału prądu elektrycznego, a nawet może być nieodłączna w ropie i gazie. Elektrochemiczny wyróżnia się pewnymi procesami, jest bardziej złożony niż chemiczny.

Na wideo: korozja metali.
Przyczyny i oznaki korozji elektrochemicznej
Korozja elektrochemiczna różni się od korozji chemicznej tym, że proces niszczenia zachodzi w układzie elektrolitu, co powoduje powstawanie prądu elektrycznego wewnątrz tego układu. Dwa procesy sprzężone, anodowy i katodowy, prowadzą do usunięcia niestabilnych atomów z sieci krystalicznej metalu. Podczas procesu anodowego jony przechodzą do roztworu, a elektrony z procesu anodowego wpadają w pułapkę substancji utleniającej i są wiązane przez depolaryzator.
Zatem depolaryzacja to usuwanie wolnych elektronów z miejsc katodowych, a depolaryzator jest substancją odpowiedzialną za ten proces. Główne reakcje zachodzą z udziałem wodoru i tlenu jako depolaryzatorów.
Istnieje wiele przykładów różnego rodzaju korozji elektrochemicznej, która w przyrodzie i pod wpływem różnych warunków oddziałuje na powierzchnie metali. Wodór działa w środowisku kwaśnym, natomiast tlen w środowisku obojętnym.
Prawie wszystkie metale ulegają korozji elektrochemicznej i na tej podstawie dzieli się je na 4 grupy, określa się wartość ich potencjału elektrodowego:
- aktywne korodują nawet w środowisku bez utleniaczy;
- średnio aktywne wchodzą w reakcję utleniania w środowisku kwaśnym;
- nieaktywne nie reagują pod nieobecność utleniaczy zarówno w środowisku obojętnym, jak i kwaśnym;
- nie reagują - wysoka stabilność (metale szlachetne, pallad, złoto, platyna, iryd).
Ale ta sama reakcja może zachodzić również w wodzie, w roztworach zasad, soli i kwasów. W wysoce wyspecjalizowanej różnicy w korozji atmosferycznej, glebie i napowietrzeniu wyróżnia się morską i biologiczną (występującą pod wpływem bakterii).
Występuje nawet korozja elektryczna, która występuje pod wpływem prądu elektrycznego i jest wynikiem prądów błądzących, które występują, gdy prąd elektryczny jest wykorzystywany przez osobę do wykonywania określonych czynności.
W tym przypadku jednorodna powierzchnia metalu ulega zniszczeniu z powodu niestabilności termodynamicznej w środowisku. I niejednorodny - ze względu na skład sieci krystalicznej, w której atomy jednego metalu trzymane są mocniej niż atomy obcych wtrąceń.Reakcje te różnią się szybkością jonizacji jonów i redukcji utleniających składników środowiska.
Zniszczenie powierzchni metalowych podczas korozji elektrochemicznej polega na jednoczesnym występowaniu dwóch procesów: anodowego i katodowego, przy czym różnice między tymi procesami polegają na tym, że rozpuszczanie następuje na anodach, które mają kontakt z otoczeniem poprzez wiele mikroelektrod wchodzących w skład powierzchni jakiegokolwiek metalu i są zamknięte dla siebie.