RÉCLAMER
1. La méthode de liquéfaction directe du charbon, qui comprend les étapes suivantes :
(1) préparer une bouillie de charbon à partir de charbon brut et d'un catalyseur ;
(2) mélange de la bouillie de charbon avec de l'hydrogène et prétraitement du mélange, suivi de sa fourniture au système de réaction pour effectuer la réaction de liquéfaction ;
(3) séparer les produits de réaction soutirés du réacteur dans un séparateur (9, 10) pour former une phase liquide et une phase gazeuse, la phase liquide étant soumise à un fractionnement dans une colonne de distillation (11) à pression atmosphérique pour obtenir une produit sous la forme d'une fraction de gazole et d'un produit résiduel ;
(4) introduire le produit de fond obtenu dans la colonne à pression atmosphérique dans une colonne de distillation sous vide (12) pour une séparation en distillat et résidu ;
(5) mélanger la fraction de carburant diesel et le distillat pour former un mélange, puis introduire le mélange dans le réacteur d'hydrotraitement à lit fluidisé à circulation forcée (13) pour effectuer le processus d'hydrogénation ;
(6) fractionnement des produits d'hydrogénation en produits pétroliers et un solvant donneur d'hydrogène recyclé à l'étape (1).
2. Procédé selon la revendication 1, dans lequel l'étape (1) comprend les opérations suivantes :
(a) convertir le charbon brut en poudre de charbon avec une granulométrie donnée après séchage et broyage du charbon brut dans un appareil de prétraitement ; (b) traiter la charge de catalyseur (3) et la poudre de charbon dans l'appareil de préparation de catalyseur (4) pour obtenir une poudre de catalyseur de liquéfaction de charbon ultrafine ; (c) mélanger dans l'appareil (5) pour préparer une bouillie du catalyseur de liquéfaction du charbon et de la poudre de charbon avec un solvant donneur d'hydrogène (16) pour former une bouillie de charbon.
3. Procédé selon la revendication 1, dans lequel l'étape de réaction de liquéfaction du charbon comprend les étapes suivantes :
(a) introduire la bouillie de charbon après l'avoir mélangée avec de l'hydrogène (6) et la préchauffer dans le premier réacteur à lit fluidisé (7) avec circulation forcée pour effectuer la réaction de liquéfaction pour obtenir des produits de réaction quittant le réacteur ; (b) alimenter les produits de réaction sortant du premier réacteur à lit fluidisé (7), après les avoir mélangés avec de l'hydrogène, dans le deuxième réacteur à lit fluidisé (8) à circulation forcée pour poursuivre la réaction de liquéfaction, lesdits réacteurs à lit fluidisé fonctionnant au régime de réaction suivant conditions : température de réaction 430-465°C ; pression de réaction 15-19 MPa ; le rapport des quantités de gaz et de liquide 600-1000 nl/kg ; taux volumétrique de suspension de charbon 0,7-1,0 t/m3 h ; le degré d'addition du catalyseur Fe/charbon sec = 0,5-1,0 % en poids.
4. Procédé selon l'une quelconque des revendications précédentes, dans lequel l'étape (3) comprend les opérations suivantes :
(a) introduire le courant de produits de réaction dans un séparateur à haute température (9) pour une séparation en une phase gazeuse et une phase liquide, tandis que la température dans le séparateur à haute température est maintenue à 420°C ;
(b) amener la phase gazeuse du séparateur haute température (9) au séparateur basse température (10) pour une séparation supplémentaire en gaz et liquide, tandis que la température dans le séparateur basse température est maintenue à température ambiante.
5. Procédé selon la revendication 2, dans lequel -FeOOH est utilisé comme catalyseur de liquéfaction, dont les particules ont un diamètre de 20-30 nm et une longueur de 100-180 nm, et le catalyseur contient du soufre dans un rapport molaire de S/Fe=2.
6. Procédé selon la revendication 1, dans lequel l'hydrogénation à l'étape (5) est réalisée dans les conditions suivantes : température de réaction 330-390°C ; pression de réaction 10-15 MPa ; le rapport des quantités de gaz et de liquide 600-1000 nl/kg ; vitesse spatiale 0,8-2,5 h-1.
7. Procédé selon la revendication 1, dans lequel le solvant donneur d'hydrogène recyclé est un produit pétrolier liquéfié hydrogéné avec un point d'ébullition dans la plage de 220 à 450°C.
8. Procédé selon la revendication 1, dans lequel le résidu dans la colonne de distillation sous vide (12) a une teneur en solides de 50 à 55 % en poids.
9. Procédé selon l'une quelconque des revendications précédentes, dans lequel le mélange de la fraction gazole sortant de la colonne à pression atmosphérique et du distillat issu de la colonne à vide a un point d'ébullition de C 5 dans la plage de 530°С.
dix.Procédé selon la revendication 1, dans lequel le réacteur d'hydrotraitement à lit fluidisé à circulation forcée (13) est un réacteur interne, dans lequel une pompe de circulation est installée près du fond du réacteur, et le catalyseur dans le réacteur peut être remplacé pendant le fonctionnement.
RÉCLAMER
1. Procédé pour brûler du charbon, y compris le sécher, le broyer jusqu'à un état finement dispersé, mélanger du charbon broyé avec un flux de gaz dirigé contenant de l'oxygène et le brûler, caractérisé en ce que le charbon broyé est chauffé à une température de semi-cokéfaction d'au moins 500 ° C, des hydrocarbures gazeux volatils en sont libérés, qui se divisent ensuite en fractions liquide et gazeuse par condensation, et le semi-coke obtenu en chauffant le charbon broyé est mélangé au flux de gaz dirigé contenant de l'oxygène et brûlé.
2. Procédé selon la revendication 1, caractérisé en ce que le séchage du charbon broyé est réalisé simultanément au broyage du charbon.
3. Procédé selon la revendication 1, caractérisé en ce que le charbon broyé est porté à une température de semi-cokéfaction en le mélangeant avec un caloporteur gazeux.
4. Procédé selon la revendication 1, caractérisé en ce que le charbon broyé est chauffé à la température de semi-cokéfaction en le mélangeant avec un caloporteur solide ayant une température de 800-1300°C.
5. Procédé selon la revendication 3, caractérisé en ce que les caloporteurs gazeux sont des gaz formés lors de la combustion d'au moins une partie d'hydrocarbures gazeux volatils.
6. Procédé selon la revendication 3, caractérisé en ce que le caloporteur gazeux est les gaz formés lors de la combustion d'au moins une partie du semi-coke obtenu.
7. Procédé selon la revendication 4, caractérisé en ce que le caloporteur solide est le semi-coke obtenu.
8. Procédé selon la revendication 4, caractérisé en ce que le caloporteur solide est du sable de quartz.
9. Procédé selon la revendication 4, caractérisé en ce que le caloporteur solide est un matériau céramique dispersé.
10. Procédé selon la revendication 4, caractérisé en ce que le caloporteur solide est du charbon.
11. Procédé selon la revendication 4, caractérisé en ce que le caloporteur solide est un oxyde d'une substance inorganique avec une taille de fraction de 0,5-5 mm.
12. Procédé selon la revendication 9, ou 10, ou 12, caractérisé en ce que le fluide caloporteur après utilisation est séparé du semi-coke par tamisage.
13. Procédé selon l'une des revendications 1 à 13, caractérisé en ce que la fraction gazeuse d'hydrocarbures volatils est totalement ou partiellement brûlée.
14. Procédé selon la revendication 13, caractérisé en ce que la fraction gazeuse d'hydrocarbures volatils est épurée des substances soufrées avant combustion.
15. Procédé selon la revendication 1, caractérisé en ce que le chauffage du charbon broyé à la température de semi-cokéfaction est réalisé dans une chambre à vortex en le mélangeant avec des gaz chauds.
Réponses au paragraphe 19
1. Quelles sont les principales sources naturelles d'hydrocarbures que vous connaissez : Pétrole, gaz naturel, schiste, charbon.
2. Quelle est la composition du gaz naturel ? Indiquer sur la carte géographique les gisements les plus importants : a) gaz naturel ; ébullition; c) charbon.
3. Quels sont les avantages du gaz naturel par rapport aux autres combustibles ? À quelles fins le gaz naturel est-il utilisé dans l'industrie chimique Le gaz naturel, par rapport aux autres sources d'hydrocarbures, est le plus facile à extraire, à transporter et à traiter. Dans l'industrie chimique, le gaz naturel est utilisé comme source d'hydrocarbures de faible poids moléculaire.
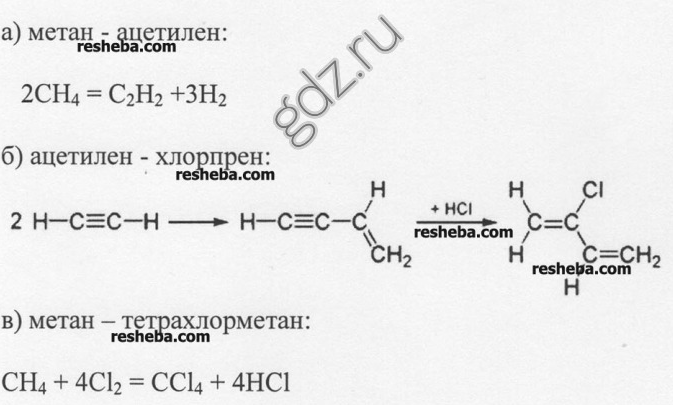
4. Écrivez les équations des réactions d'obtention : a) de l'acétylène à partir du méthane ; b) caoutchouc chloroprène à partir d'acétylène ; c) tétrachlorure de carbone à partir de méthane.
5. Quelle est la différence entre les gaz de pétrole associés et le gaz naturel Les gaz associés sont des hydrocarbures volatils dissous dans le pétrole. Leur isolement se fait par distillation. Contrairement au gaz naturel, il peut être rejeté à n'importe quel stade du développement d'un champ pétrolier.
6.Décrire les principaux produits obtenus à partir des gaz de pétrole associés Principaux produits : méthane, éthane, propane, n-butane, pentane, isobutane, isopentane, n-hexane, n-heptane, hexane et isomères de l'heptane.
7. Nommez les produits pétroliers les plus importants, indiquez leur composition et leurs domaines d'application.
8. Quelles huiles lubrifiantes sont utilisées en production : huiles pour engrenages, huiles industrielles, huiles de coupe pour machines-outils, etc.
9. Comment se déroule la distillation de l'huile ?
10. Qu'est-ce que le craquage d'huile ? Faites une équation pour les réactions de fractionnement des hydrocarbures et dans ce processus.
11. Pourquoi n'est-il pas possible d'obtenir plus de 20 % d'essence lors de la distillation directe de l'huile ?Parce que la teneur de la fraction essence dans l'huile est limitée.
12. Quelle est la différence entre le craquage thermique et le craquage catalytique ? Donner une description des essences de craquage thermique et catalytique.En craquage thermique, il est nécessaire de chauffer les réactifs à des températures élevées, en craquage catalytique, l'introduction d'un catalyseur réduit l'énergie d'activation de la réaction, ce qui peut réduire considérablement la réaction Température.
13. Comment peut-on pratiquement distinguer l'essence de craquage de l'essence de distillation directe ? L'essence de craquage a un indice d'octane plus élevé que l'essence de distillation directe, c'est-à-dire plus résistant à la détonation et recommandé pour une utilisation dans les moteurs à combustion interne.
14. Qu'est-ce que l'aromatisation de l'huile ? Écrivez les équations de réaction qui expliquent ce processus.
15. Quels sont les principaux produits obtenus par cokéfaction du charbon Naphtalène, anthracène, phénanthrène, phénols et huiles de charbon.
16. Comment le coke est-il produit et où est-il utilisé Le coke est un produit solide poreux gris obtenu par cokéfaction du charbon à des températures de 950-1100 sans oxygène. Il est utilisé pour la fonte du fer, comme combustible sans fumée, agent réducteur de minerai de fer et poudre à lever pour les matériaux de charge.
17. Quels sont les principaux produits obtenus : a) à partir de goudron de houille ; b) à partir d'eau de goudron ; c) du gaz de cokerie ? Où sont-ils appliqués ? Quelles substances organiques peuvent être extraites du gaz de cokerie a) benzène, toluène, naphtalène - industrie chimique b) ammoniac, phénols, acides organiques - industrie chimique c) hydrogène, méthane, éthylène - carburant.
18. Rappelons tous les principaux moyens d'obtenir des hydrocarbures aromatiques. Quelle est la différence entre les méthodes d'obtention d'hydrocarbures aromatiques à partir des produits de cokéfaction du charbon et du pétrole ? Écrivez les équations des réactions correspondantes.Elles diffèrent par les méthodes d'obtention: le raffinage primaire du pétrole est basé sur la différence des propriétés physiques des différentes fractions et la cokéfaction est basée uniquement sur les propriétés chimiques du charbon.
19. Expliquer comment, dans le processus de résolution des problèmes énergétiques du pays, les modes de traitement et d'utilisation des ressources naturelles en hydrocarbures seront améliorés. Recherche de nouvelles sources d'énergie, optimisation des processus de production et de raffinage du pétrole, développement de nouveaux catalyseurs pour réduire la coût de toute la production, etc.
20. Quelles sont les perspectives d'obtention de combustible liquide à partir du charbon À l'avenir, l'obtention de combustible liquide à partir du charbon est possible, à condition que le coût de sa production soit réduit.
Tâche 1. On sait que le gaz contient 0,9 méthane, 0,05 éthane, 0,03 propane, 0,02 azote en fractions volumiques. Quel volume d'air est nécessaire pour brûler 1 m3 de ce gaz dans des conditions normales ?

Tâche 3. Calculer quel volume (en l) et quelle masse (en kg) de monoxyde de carbone (IV) seront obtenus en brûlant 5 moles d'octane (n.o.).
2 Hydrogénation
L'hydrogénation du lignite est un processus de transformation directe du charbon en combustibles synthétiques à l'état liquide et gazeux d'agrégation, qui se produit à haute pression et à température relativement élevée.
Cette direction du traitement du charbon est explorée dans différents pays du monde.À l'étranger, cette technologie a reçu la plus grande introduction industrielle en Afrique du Sud, où quatre usines fonctionnent, avec une capacité annuelle totale d'environ 8 à 10 millions de tonnes de combustible liquide. Les travaux sont réalisés à l'aide de la technologie brevetée SASOL basée sur la méthode Fischer-Tropsch améliorée. Étant donné que SASOL a pour politique de maintenir des paiements élevés pour le droit d'utiliser la technologie, cela entraîne un coût élevé de sa mise en œuvre industrielle dans d'autres pays.[]
La préparation du lignite comprend le concassage, le séchage, la préparation de la pâte d'hydrogénat de charbon. Le broyage est effectué jusqu'à une granulométrie inférieure à 0,1 mm - pour augmenter la réactivité de la surface, il est mis en œuvre dans des désintégrateurs. Dans ce cas, la surface spécifique externe augmente de 20 à 30 fois, le volume des pores de transition - de 5 à 10 fois. Ensuite, le charbon est séché. Les pores sont remplis d'humidité, ce qui empêche la pénétration de réactifs dans la matière du charbon, il est libéré au cours du processus dans la zone de réaction, réduisant la pression partielle de H2, et augmente également la quantité d'eaux usées. Pour le séchage, on utilise des séchoirs à vapeur tubulaires, des chambres vortex, des tuyaux de séchoir dans lesquels le charbon est séché jusqu'à une teneur en humidité résiduelle de 1,5%. Le caloporteur est constitué de gaz de combustion chauds avec une teneur minimale en O2 (0,1-0,2 %) afin que le charbon ne subisse pas d'oxydation. Le charbon n'est pas chauffé au-dessus de 150-200 ° C pour éviter une diminution de la réactivité.
Exigences relatives au lignite destiné à la liquéfaction
Sur la base d'un grand matériel expérimental, il a été prouvé que le charbon avec une bonne hydraulicité contient de 65 à 85% de C, plus de 5% de H et a plus de 30% de rendement volatil (V). Teneur en humidité rationnelle du charbon initial pour le processus d'hydrogénation - Wrt = 10-15 %, teneur en cendres Ad = 10-12 %, valeur d
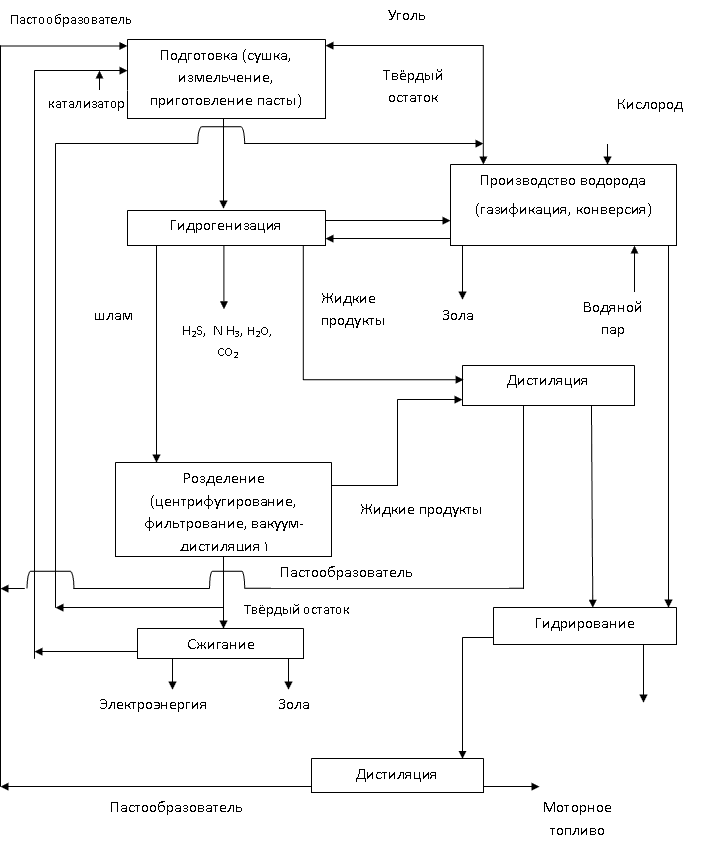
Le schéma d'hydrogénation le plus courant est illustré à la figure 1.2 []
Riz. 1.2 - Schéma d'obtention de combustible liquide synthétique à partir de lignite
Dynamique de la consommation de gaz issu du charbon dans le monde
| Utilisation prévue | Utilisation en 2001, MW pour le gaz | Part en 2001, % | Mise en service avant fin 2004, MW pour le gaz | Augmentation annuelle de la capacité en 2002-2004, % |
| Fabrication chimique | 18 000 | 45 | 5 000 | 9,3 |
| Gazéification intracycle (production d'électricité) | 12 000 | 30 | 11 200 | 31 |
| Synthèse Fischer-Tropsch | 10 000 | 25 | ||
| LE TOTAL | 40 000 | 100 | 17 200 | 14,3 |
Les données fournies démontrent clairement l'accélération de la dynamique de l'implication de la gazéification du charbon dans l'industrie mondiale. L'intérêt accru pour la gazéification intracycle du charbon dans les pays développés est dû à deux raisons.
Premièrement, les centrales thermiques à gazéification intracycle sont moins dangereuses pour l'environnement. Grâce au prétraitement des gaz, les émissions d'oxydes de soufre, d'oxydes d'azote et de particules sont réduites.
Deuxièmement, l'utilisation d'un cycle binaire peut augmenter considérablement l'efficacité de la centrale électrique et, par conséquent, réduire la consommation spécifique de carburant.
En tableau. Le tableau 2 montre les valeurs caractéristiques des émissions spécifiques et de l'efficacité pour les TPP avec gazéification intracycle et pour les TPP avec combustion traditionnelle du charbon.
Tableau 2
Émissions spécifiques et efficacité des centrales thermiques avec gazéification intercycle et combustion conventionnelle du charbon
| Paramètres | Centrale électrique traditionnelle au charbon | TPP avec gazéification intracycle |
| La concentration de substances nocives dans les gaz de combustion (pour une centrale thermique au charbon - selon la norme européenne), mg / m3 - SOX - NONX - Des particules solides | 130 150 16 | 10 30 10 |
| Efficacité électrique, % | 33-35 | 42-46 |
Il convient de noter que les coûts d'investissement spécifiques lors de l'utilisation de la gazéification intracycle sont d'environ 1500 dollars américains pour 1 kW avec la perspective de réduire à 1000-1200 dollars américains, tandis que pour une centrale thermique au charbon traditionnelle, les coûts d'investissement spécifiques sont d'environ 800-900 dollars américains pour 1 kW. Il est clair qu'une centrale thermique avec gazéification intracycle de combustible solide est plus attrayante en présence de restrictions environnementales sur le site et lors de l'utilisation de combustible plutôt coûteux, car la consommation de combustible par 1 kW est réduite.
Ces conditions sont typiques des pays développés.À l'heure actuelle, l'utilisation de la gazéification intracycle des combustibles solides est considérée comme la voie la plus prometteuse dans le secteur de l'énergie.
3.3 Développements techniques au cours du siècle dernier
À l'heure actuelle, les domaines d'application les plus rentables suivants de la méthode de gazéification ont été identifiés :
— gazéification de combustibles sulfureux et riches en cendres avec combustion ultérieure des gaz résultants dans de puissantes centrales thermiques. Les charbons extraits chaque année en Russie contiennent environ 10 millions de tonnes de soufre, dont la majeure partie, lorsqu'elle est brûlée, est rejetée dans l'atmosphère sous forme d'oxydes de soufre toxiques et de sulfure de carbone. Lors de la gazéification des charbons sulfureux, du sulfure d'hydrogène se forme, qui peut être extrait relativement facilement puis transformé en soufre commercial ou en acide sulfurique.
— gazéification de combustibles solides pour la production à grande échelle de substituts du gaz naturel. Cette direction est de la plus haute importance pour l'approvisionnement local en gaz des zones éloignées des gisements de gaz naturel et de pétrole ou des principaux pipelines.
— la gazéification de combustibles solides en vue d'obtenir du gaz de synthèse, des gaz réducteurs et de l'hydrogène pour les besoins des industries chimiques, pétrochimiques et métallurgiques.
Le processus de gazéification dépend de nombreux facteurs qui affectent la composition du gaz résultant et sa valeur calorifique. A cet égard, il n'existe pas encore de classification unique généralement admise des méthodes de mise en oeuvre du procédé considéré. Vous trouverez ci-dessous l'une des options de classification possibles.
Par type de souffle (agent de gazéification) : air, air-oxygène, vapeur-air, vapeur-oxygène.
Par pression : à pression atmosphérique, à pression élevée.
· par granulométrie du combustible : gazéification du combustible à gros grains (morceaux), à grains fins et pulvérisé.
· selon les caractéristiques de conception de la zone réactionnelle : dans une couche dense fixe de combustible, dans une couche fluidisée de combustible, dans une flamme de charbon pulvérisé.
par la méthode d'élimination des cendres : sous forme solide, sous forme de laitier liquide.
Par la méthode d'apport de chaleur: avec combustion partielle du combustible dans un générateur de gaz, avec mélange de combustible avec un caloporteur solide, liquide ou gazeux préchauffé (chauffage régénératif), avec apport de chaleur à travers la paroi de l'appareil (chauffage récupérateur).
Le monoxyde de carbone, les carbonyles métalliques et la règle des 18 électrons
Nombreux
synthèses à base de monoxyde de carbone et
l'hydrogène représente un énorme
pratiques que théoriques
intérêts, comme le permettent de deux
les substances les plus simples pour recevoir les plus précieuses
composés organiques. Et ici
la catalyse joue un rôle important
métaux de transition capables de
activer les molécules de CO inertes et
H2.
L'activation des molécules est leur traduction en
état plus réactif.
Notons en particulier que dans les transformations
le gaz de synthèse s'est largement développé
un nouveau type de catalyse - la catalyse par complexes
métaux de transition ou complexes métalliques
catalyse (voir l'article de O.N. Temkin
).
Alors
La molécule de CO est-elle inerte ? Représentation
sur l'inertie du monoxyde de carbone
caractère conditionnel. Retour en 1890 lundi
obtenu à partir de nickel métallique et
monoxyde de carbone premier carbonyle
composé métallique, liquide volatil
avec un point d'ébullition de 43 ° C - Ni (CO)4 .
L'histoire de cette découverte est intéressante.
qui peut être qualifiée d'aléatoire. Lundi,
rechercher les causes de la corrosion rapide
réacteurs nickel en production
soude à partir de NaCl, d'ammoniac et de CO2,
trouvé que la cause de la corrosion est
présence en CO2 impuretés
monoxyde de carbone, qui a réagi
avec du nickel pour former du tétracarbonyle
Nico)4 .
Cette découverte a permis à Mond d'approfondir
développer des méthodes de purification du nickel
par la production d'un carbonyle volatil
nickel et son thermique ultérieur
décomposition à nouveau en nickel et CO. De l'autre côté
25 ans ont aussi accidentellement découvert le carbonyle
fer - Fe(CO)5.
Lorsque BASF a ouvert une entreprise oubliée depuis longtemps
cylindre en acier avec CO, trouvé au fond
liquide jaune - fer pentacarbonyle,
qui s'est peu à peu transformé en
le résultat d'une réaction métallique
repasser au CO sous haute pression.
Parce que les carbonyles métalliques sont
composés hautement toxiques, initialement
l'attitude des chimistes à leur égard était très
cool, mais à l'avenir étaient
propriétés étonnantes découvertes, y compris
y compris catalytique, qui a déterminé
leur large application, notamment en chimie
monoxyde de carbone. Notez que beaucoup
métaux à l'état finement dispersé
peut réagir directement
avec du monoxyde de carbone, mais de cette façon
ne reçoivent que des carbonyles de nickel et
glande. Carbonyles d'autres métaux
obtenus en restituant leurs composés
en présence de CO à haute
pressions.
Composé
complexes carbonylés de transition
les métaux peuvent être prédits sur la base
règle des 18 électrons, selon laquelle
le complexe sera stable si la somme
les électrons de valence du métal et les électrons,
fourni par le ligand, dans notre cas
CO, sera égal à 18, puisque dans ce cas
la configuration électronique correspond
configuration stable des atomes
gaz nobles (krypton).
Molécule
le monoxyde de carbone a seul
paires d'électrons, tandis qu'une paire d'électrons
sur le carbone peut être fourni
former une liaison avec le métal
type donneur-accepteur. Comme
Par exemple, considérons la structure des carbonyles
fer et nickel Fe(CO)5 et
Nico)4.
Les atomes de fer et de nickel ont respectivement
8 et 10 électrons de valence, et pour remplir
enveloppe électronique d'un atome avant configuration
atome de gaz noble krypton
10 et 8 électrons sont manquants, et donc
dans la formation de carbonyles à l'atome de fer
doit fournir des paires d'électrons
cinq molécules de CO et un atome de nickel
quatre.
de transition
métaux qui ont un nombre impair de valences
électrons, forme binucléaire
complexes carbonylés. Ainsi, pour le cobalt,
ayant neuf électrons de valence
à une configuration électronique stable
manque neuf électrons. noyau unique
complexes en prenant quatre paires
à partir de molécules de CO aura non apparié
électrons, et de telles particules du radical
les personnages interagissent les uns avec les autres.
pour former une liaison métal-métal, et
entraînant la formation d'un dimère
Co complexe2(CO)8.
Interaction
ou la coordination du monoxyde de carbone avec
le métal conduit à une redistribution
densité électronique non seulement sur CO,
mais aussi sur le métal, ce qui affecte considérablement
sur la réactivité du carbonyle
complexe. Le plus commun est
appelé type de coordination linéaire
CO:
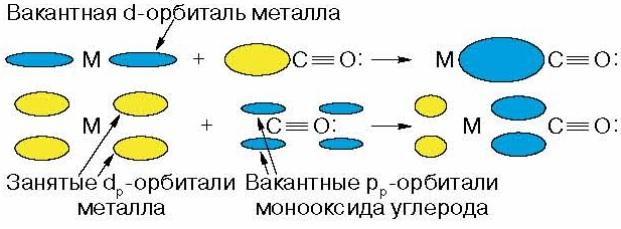
À
ce n'est pas seulement l'interaction s
dû à une paire d'électrons libres
carbone, mais aussi p-interaction due à
transfert d'électrons depuis l'orbitale d du métal
vacant énergétiquement disponible
orbitales de carbone :
Pertinence
Ainsi, il est nécessaire de développer une telle technologie pour le traitement primaire et l'agglomération du lignite, qui prendrait en compte les propriétés spécifiques du lignite d'origine, les conditions du processus de transport hydraulique du charbon et les exigences de la caractéristiques des matières premières du charbon dans les opérations ultérieures de son traitement - pyrolyse, combustion, liquéfaction, briquetage, déshydratation. La solution à ce problème peut être la technologie de traitement du charbon avec des réactifs pétroliers - agrégation d'huile.
L'agrégation sélective d'huile de charbon combine un ensemble de procédés de structuration d'une phase fine de charbon polydisperse en milieu aqueux à l'aide de réactifs pétroliers.Les processus d'agrégation sélective d'huile de charbon sont basés sur le mécanisme d'interaction adhésive de la surface oléophile du charbon avec les huiles, ce qui entraîne son mouillage sélectif et son agrégation dans un écoulement d'eau turbulent. Les particules hydrophiles non mouillées par l'huile ne sont pas incluses dans la structure des granulats, ce qui permet de les isoler sous forme de suspension rocheuse.
Le traitement du lignite par agrégation sélective d'huile élimine sa désintégration et son trempage, "préservant" la matière organique dans des agrégats hydrophobes, qui se déshydratent facilement par des méthodes mécaniques et constituent une bonne matière première pour la pyrolyse, le briquetage et la gazéification.
1 Briquetage
Le briquetage du charbon est un processus physique et chimique permettant d'obtenir un produit de haute qualité mécaniquement et thermiquement résistant - une briquette ayant une forme géométrique, une taille et un poids donnés.
Le procédé technologique de briquetage du lignite sans liant consiste en les opérations suivantes : préparation du charbon en termes de taille et d'humidité, et pressage.
Indicateurs technologiques auxquels les briquettes de lignite doivent se conformer : poids de la briquette 100-500 g, résistance mécanique à l'abrasion 75-80 %, compression et flexion 70-90 et 10-15 MPa, respectivement, absorption d'humidité 3-4 %, pouvoir calorifique 24 000-30 000 kJ / kg, teneur en cendres 10-25 %.[]